Роды через естественные родовые пути после первого кесарева сечения (КС) безопасны для большинства женщин [1–7]. Страх ведения влагалищных родов при наличии рубца на матке, как и неудачная попытка влагалищных родов при наличии рубца на матке чаще всего ассоциированы с разрывом матки. Однако, по данным мирового опыта, реализуется разрыв матки лишь в 0,2–0,5% случаях [3–5]. Ведение консервативных родов с рубцом на матке в условиях развернутой операционной указывает на то, что тактика ведения может поменяться в любую минуту; резервные возможности рубца непредсказуемы. Совершенно очевидным является учет всех факторов, влияющих на заживление рубцовой ткани миометрия после первого КС при подборе идеального кандидата для влагалищных родов с рубцом на матке [2]. Однако важно подчеркнуть, что состоятельность рубца на матке до наступления родовой деятельности является лишь потенциальной. Широко используемая в настоящее время оценка состоятельности рубца на матке по данным ультразвукового исследования (УЗИ) во время беременности дает лишь визуальную оценку.
Зачастую акушер-гинеколог опасается разрыва матки и работает на опережение. Решение о проведении интранатального КС принимается при малейшем подозрении на несостоятельность рубца на матке – появлении локальной болезненности в области рубца. Кровянистые выделения из половых путей могут отсутствовать, плод по данным кардиотокографии (КТГ) может не страдать. Результат – новорожденный с высокими баллами по шкале Апгар и допустимый объем интраоперационной кровопотери. Разрыва матки нет. Ключевой вопрос: что происходит с рубцом? Почему одни женщины с рубцом на матке после КС способны родить влагалищным путем, а другим требуется проведение повторного КС? Возможна ли доклиническая диагностика несостоятельности рубца на матке в родах? Довольно низкая частота влагалищных родов после КС в Российской Федерации (не более 1,5%) [6] связана, в том числе, с отсутствием полного понимания физиологии родового процесса при наличии рубца на матке; это остается острой проблемой современного акушерства. Все вышеизложенное подчеркивает необходимость обстоятельного рассмотрения оригинальных исследований, посвященных влагалищным родам при наличии рубца на матке, обзоров, метаанализов, мнения экспертов.
Цель настоящей работы: представить собственный опыт клиники по ведению влагалищных родов при наличии рубца на матке; представить клинические ситуации неудачной попытки влагалищных родов после КС, связанные с несостоятельностью рубца.
Материалы и методы
В ООО «Клиника профессора Буштыревой» в период с 2018 г. по 2022 г. проведено проспективное исследование, в котором приняла участие 41 беременная женщина с рубцом на матке после одного КС. Критерии включения: одноплодная доношенная беременность, головное предлежание плода, предыдущее КС проведено поперечным разрезом в нижнем маточном сегменте, состоятельный рубец на матке по данным УЗИ, локализация плаценты вне рубца на матке, отсутствие показаний для повторного КС, желание женщины родить естественным путем, спонтанное начало родовой деятельности. У всех этих женщин планировалось ведение родов через естественные родовые пути.
При поступлении в роддом состоятельность рубца на матке оценивалась клинически (пальпация области послеоперационного рубца) и с помощью УЗИ (минимальная толщина нижнего сегмента матки). УЗИ проводилось на аппарате VOLUSON E10 с применением конвексного датчика RAB 6-D и вагинального датчика RIC 6-12-D.
Статистический анализ
Сравнение медиан в группах проводилось с помощью теста Краскела–Уоллиса (попарные апостериорные сравнения производились с помощью метода Неменьи). Различия признавались статистически значимыми на уровне р<0,05. Расчеты выполнялись в R (версия 3.2, R Foundation for Statistical Computing, Vienna, Austria).
Результаты
Из 41 женщины с попыткой влагалищных родов при наличии рубца на матке 26 пациенток благополучно родили через естественные родовые пути, 15 – выполнено повторное КС.
Показаниями к повторному интранатальному КС послужили: аномалии родовой деятельности (n=7), клинически узкий таз (n=4), угроза несостоятельности рубца на матке (n=4).
При повторном КС у всех 15 женщин доступ через переднюю брюшную стенку произведен разрезом по Пфанненштилю, КС проведено в нижнем маточном сегменте. Методом обезболивания КС явилась нейроаксиальная анестезия: у 10 женщин КС проведено под эпидуральной анестезией, у 5 – под спинальной анестезией. Во время повторного КС у этих 15 женщин иссекался фрагмент рубцовой и околорубцовой ткани миометрия с целью проведения морфологического исследования. Биоматериал расправлялся на толстой бумаге, фиксировался в 10% забуференном нейтральном формалине в течение 48–72 ч, после рутинной проводки заливался в парафин; гистологические срезы толщиной не более 3 мкм окрашивались гематоксилином-эозином и по методу Ван-Гизона. Фоторегистрация гистопрепаратов выполнялась с помощью фотомикроскопа Leica1000DM (Германия). Стенка матки ушивалась двурядным непрерывным швом.
При повторном КС (n=15) у 11 пациенток интраоперационно рубец на матке был состоятельным, и лишь у 4 пациенток обнаружена несостоятельность рубца на матке, представленная неполным разрывом матки (n=2) и расползанием матки по рубцу (n=2).
Неполный разрыв матки – нарушение целостности миометрия, не проникающее в брюшную полость, без нарушения целостности пузырно-маточной складки, плодного пузыря и без выхождения частей плода в брюшную полость.
Расползание матки по рубцу – нарушение целостности миометрия, не проникающее в брюшную полость, без нарушения целостности висцеральной и париетальной брюшины, плодного пузыря и без выхождения частей плода в брюшную полость.
Учитывая, что всем женщинам при поступлении в стационар интранатально проводилась ультразвуковая оценка состоятельности рубца на матке (измерялась минимальная толщина нижнего сегмента матки), проведен анализ ультразвуковых данных. Минимальная толщина нижнего сегмента матки у женщин, благополучно родивших влагалищным путем (n=26), составила 2,35 мм [2; 2,8]. У повторно прооперированных женщин по причинам, не связанным с рубцом (n=11), минимальная толщина нижнего сегмента матки составила 2,5 мм [2,1; 2,6]; у женщин, прооперированных в связи с угрозой несостоятельности рубца на матке (n=4), – 1,9 мм [1,65; 2,05]. При попарном сравнении групп статистически значимые различия были выявлены в группах между женщинами, родившими влагалищным путем, и женщинами, которым проведено повторное КС в связи с угрозой несостоятельности рубца на матке, р=0,046.
Далее будут описаны 4 клинические ситуации с установленной несостоятельностью рубца на матке. С интраоперационной картиной будут соотнесены клинические и морфологические данные состоятельности рубца. Эта серия клинических ситуаций описана согласно требованиям PROCESS Guideline [14].
Клинические ситуации неполного разрыва матки по рубцу
Пациентка Т., 38 лет. Настоящая беременность вторая, спонтанная. Первая беременность в 2014 г. завершилась КС в связи с первичной слабостью родовой деятельности. Беременность протекала физиологически, скрининговые УЗИ – без особенностей. В 38 недель толщина рубца на матке 3 мм, предполагаемая масса плода 3600 г, состояние плода по данным допплерометрии (ДПМ) и КТГ удовлетворительное. Учитывая желание женщины родить через естественные родовые пути, отсутствие показаний для повторного КС, решено планировать роды вагинальным путем.
В 39 недель у пациентки Т. развивается спонтанная регулярная родовая деятельность. Пациентка поступает в стационар в активной фазе первого периода родов, раскрытие маточного зева 5 см. Сердцебиение плода ясное, ритмичное, 140 в 1 минуту. При наружном осмотре отмечается болезненность области послеоперационного рубца. Минимальная толщина нижнего сегмента матки по данным УЗИ составила 2,1 мм, справа визуализируется ниша размером 10×10 мм, область рубца при надавливании трансвагинальным ультразвуковым датчиком болезненна.
Учитывая наличие признаков несостоятельности рубца на матке, принято решение роды завершить путем КС в неотложном порядке. Интраоперационно под пузырно-маточной складкой справа в области послеоперационного рубца на матке обнаружена гематома размерами 15×10 мм (рис. 1). Диагностирован неполный разрыв матки.
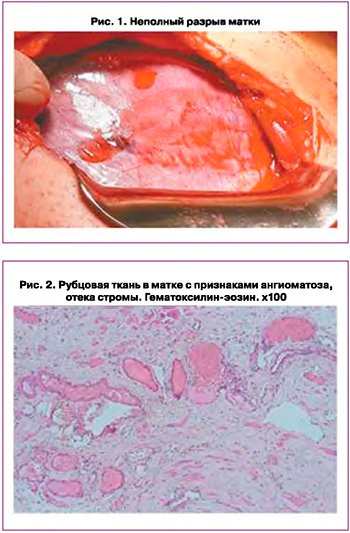
Без технических сложностей извлечен живой новорожденный массой 3800 г, длиной 52 см, оценка по шкале Апгар 10–10 баллов.
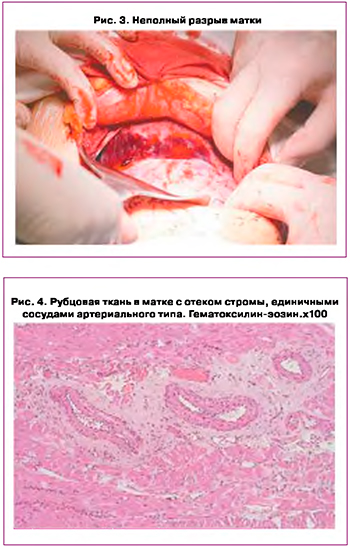
При патогистологическом исследовании рубец был представлен рыхлой волокнистой соединительной тканью. Рубцовая ткань была отечной, с признаками резко выраженного отека стромы, содержала единичные фибробласты. Обращало внимание наличие выраженного ангиоматоза за счет новообразования тонкостенных сосудов капиллярного и артериолярного типов (рис. 2).
В данном случае в зоне неполного разрыва матки имелась соединительнотканная и васкулярная перестройка с дефицитом развития коллагеновых волокон, немногочисленными фибробластами, что способствует нарушению трофики миометрия в условиях тканевой гипоксии.
Послеоперационный период протекал без осложнений, пациентка выписана домой на 3-и сутки.
Пациентка Щ., 39 лет. Настоящая беременность вторая, наступила с помощью вспомогательных репродуктивных технологий (ЭКО ИКСИ – экстракорпоральное оплодотворение, инъекция сперматозоида в цитоплазму). Первая беременность в 2019 г. наступила также с помощью ЭКО ИКСИ. Родоразрешена в доношенном сроке путем КС в связи с первичной слабостью родовой деятельности.
Первая половина настоящей беременности у пациентки Щ. протекала без особенностей, во второй половине выявлена анемия легкой степени. Скрининговые УЗИ – без особенностей. В 38 недель толщина рубца на матке 4 мм, предполагаемая масса плода 3200 г, состояние плода по данным ДПМ и КТГ удовлетворительное. Учитывая желание женщины родить влагалищным путем, отсутствие показаний для повторного КС, решено планировать роды через естественные родовые пути.
В 38 недель 5 дней у пациентки Щ. развивается спонтанная регулярная родовая деятельность. Пациентка поступает в стационар в латентной фазе первого периода родов, раскрытие маточного зева 4 см. Сердцебиение плода ясное, ритмичное, 146 в 1 минуту. При наружном осмотре область послеоперационного рубца болезненна. При проведении УЗИ минимальная толщина нижнего сегмента матки составила 2 мм, появляется болезненность в области рубца при надавливании трансвагинальным ультразвуковым датчиком.
Учитывая угрозу несостоятельности рубца на матке, принято решение роды завершить путем КС в неотложном порядке. Интраоперационно на всем протяжении рубца на матке отмечалось истончение тканей, посередине больше справа обнаружен дефект тканей размерами 5×5 мм, откуда истекала кровь (рис. 3). Диагностирован неполный разрыв матки.
Без технических сложностей извлечен живой новорожденный массой 3260 г, длиной 50 см, оценка по шкале Апгар 10–10 баллов.
При патогистологическом исследовании рубец был представлен рыхлой волокнистой соединительной тканью, содержащей артерии мышечного типа. В строме отмечался выраженный отек с формированием пористых структур за счет выраженного отека (рис. 4).
В данном случае перечисленные морфологические признаки указывали на компенсаторную перестройку соединительной ткани и сосудов, вероятнее всего, в условиях тканевой гипоксии.
Послеоперационный период протекал без осложнений, пациентка выписана домой на 3-и сутки.
Резюмируя вышеописанные клинические ситуации, можно сделать вывод о том, что своевременная клиническая диагностика несостоятельности рубца на матке (болезненность при пальпации рубца на матке) позволила выбрать тактику оперативного родоразрешения, способствуя благоприятным материнским и перинатальным исходам. УЗИ в данных клинических примерах явилось дополнительным методом диагностики несостоятельности рубца.
Клинические ситуации расползания матки по рубцу
Пациентка С., 41 год. Настоящая беременность вторая, спонтанная. Первая беременность в 2018 г. завершилась КС в связи со слабостью родовой деятельности. Течение настоящей беременности в сроке 10 недель осложнилось острой респираторной вирусной инфекцией без повышения температуры тела. Скрининговые УЗИ – без особенностей. В 38 недель толщина рубца на матке 2,8 мм, предполагаемая масса плода 3000 г, состояние плода по данным ДПМ и КТГ удовлетворительное. Учитывая желание женщины родить влагалищным путем, отсутствие показаний для повторного КС, решено планировать роды через естественные родовые пути.
В 39 недель 2 дня у пациентки С. развивается спонтанная регулярная родовая деятельность. Пациентка поступает в стационар в латентной фазе первого периода родов, раскрытие маточного зева 3 см. Сердцебиение плода ясное, ритмичное, 140 в 1 минуту. При наружном осмотре область послеоперационного рубца безболезненна при пальпации.
При выполнении УЗИ при поступлении в стационар отмечается истончение толщины нижнего сегмента матки до 1,8 мм, появляется болезненность в области рубца при надавливании трансвагинальным ультразвуковым датчиком, подозрение на несостоятельность рубца на матке, в связи с чем принято решение о завершении родов путем операции КС.
Интраоперационно нижний маточный сегмент был представлен висцеральной брюшиной, через которую просвечивали части плода (рис. 5). Диагностировано расползание матки по рубцу.
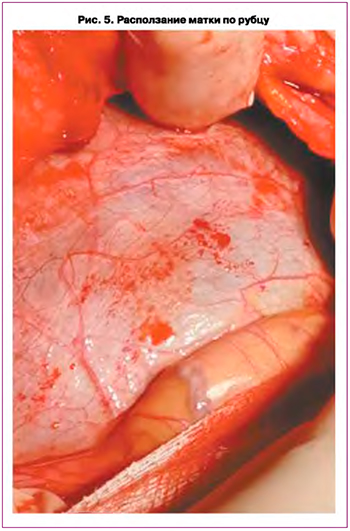
Без технических сложностей извлечен живой новорожденный массой 3050 г, длиной 50 см, оценка по шкале Апгар 9–10 баллов.
При патогистологическом исследовании иссеченный рубец был представлен рыхлой волокнистой соединительной тканью с выраженным отеком, ангиоматозом, отмечалось образование щелевидных полостей стромы (рис. 6).
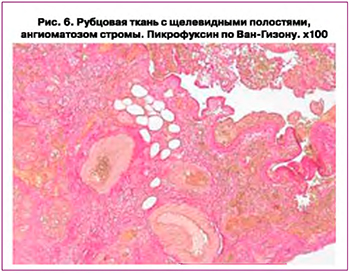
Особенностью морфологического строения расползания матки по рубцу была неполноценность развития соединительной ткани, сосудов артериального типа, которая встречается при дисплазии.
Послеоперационный период протекал без осложнений, пациентка выписана домой на 3-и сутки.
Пациентка Г., 33 года. Настоящая беременность вторая, спонтанная. Первая беременность в 2014 г. завершилась плановой операцией КС в связи с биологической незрелостью родовых путей, крупным плодом.
В сроке беременности 12 недель установлен угрожающий выкидыш, выявлена ретрохориальная гематома, проведено амбулаторное лечение. Скрининговые УЗИ II и III триместров без особенностей. В 38 недель толщина рубца на матке 3 мм, предполагаемая масса плода 3800 г, состояние плода по данным ДПМ и КТГ удовлетворительное. Учитывая желание женщины родить влагалищным путем, отсутствие показаний для повторного КС, решено планировать роды через естественные родовые пути.
В 39 недель 1 день пациентка Г. поступает в стационар в латентной фазе первого периода родов, раскрытие маточного зева 2 см. Сердцебиение плода ясное, ритмичное, 140 в 1 минуту. Область послеоперационного рубца безболезненна при пальпации.
При выполнении УЗИ при поступлении в стационар отмечается истончение рубцовой ткани до 1,5 мм, появляется болезненность в области рубца при надавливании трансвагинальным ультразвуковым датчиком, подозрение на несостоятельность рубца на матке, в связи с чем принято решение о завершении родов путем операции КС.
Интраоперационно нижний маточный сегмент был представлен висцеральной брюшиной, через которую просвечивали части плода (рис. 7). Диагностировано расползание матки по рубцу.
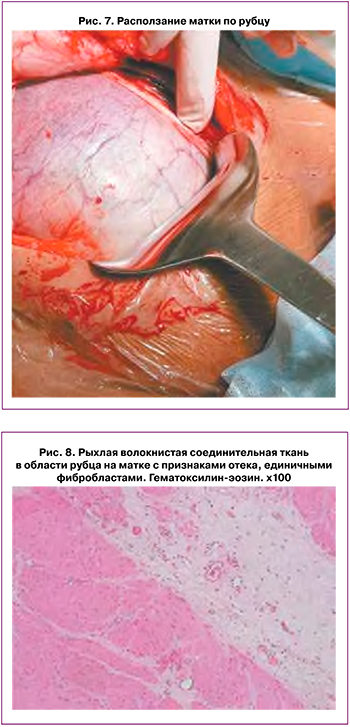
Без технических сложностей извлечен живой новорожденный массой 3850 г, длиной 53 см, оценка по шкале Апгар 10–10 баллов.
При патогистологическом исследовании рубец был представлен рыхлой волокнистой соединительной тканью с признаками выраженного отека стромы, отмечались единичные тонкостенные сосуды, единичные фибробласты (рис. 8).
В представленном наблюдении в зоне расползания матки по рубцу имелись признаки неполноценного созревания соединительной ткани (дисплазии) с нарушением клеточно-васкулярных взаимоотношений.
Послеоперационный период протекал без осложнений, пациентка выписана домой на 3-и сутки.
Резюмируя вышеописанные клинические случаи, можно сделать вывод о том, что своевременному изменению тактики ведения родов в пользу оперативного родоразрешения путем КС способствовали именно данные УЗИ. Клинических признаков несостоятельности рубца на матке у пациенток не было (болезненность области рубца при пальпации, кровянистые выделения из половых путей, гипоксия плода по данным КТГ).
Обсуждение
Задаваясь вопросом, почему одни женщины с рубцом на матке после кесарева сечения способны родить через естественные родовые пути, а другим требуется проведение повторного КС, первое, о чем мы думаем, – о несостоятельности рубца. Ультразвуковая оценка толщины нижнего сегмента матки в III триместре является одним из немногих инструментов объективной оценки состояния рубца на матке, однако толщина рубца не определяет успех попытки влагалищных родов после КС [8]. Неудачная попытка влагалищных родов после одного КС не всегда связана с наличием рубца [9]. Описаны случаи успешных влагалищных родов и после двух КС [10]. Существенное значение имеют не количество рубцов, а морфологическая полноценность рубцовой ткани миометрия, ее способность к растяжению.
Что мы получили исходя из собственных данных: из 15 женщин с неудачной попыткой влагалищных родов при наличии рубца на матке несостоятельным рубец оказался лишь у 4 женщин (26,6%). Клинические признаки угрозы несостоятельности рубца на матке (болезненность области послеоперационного рубца при пальпации) появились только у двух женщин, у них же интраоперационно диагностирован неполный разрыв матки, морфологически несостоятельность рубца подтверждена. Две пациентки с расползанием матки по рубцу прооперированы в связи с истончением рубца по данным УЗИ и появлением болезненности в области рубца при надавливании трансвагинальным ультразвуковым датчиком, морфологически несостоятельность рубца также подтвердилась.
Проведенное морфологическое исследование с применением гистологических и гистохимических методик (гематоксилин-эозин, пикрофуксин по Ван-Гизон) рубцовой ткани матки в представленных случаях выявило своеобразные особенности ее строения.
В основе строения рубца на матке при неполном разрыве была рыхлая волокнистая соединительная ткань, содержащая небольшое количество фибробластов, тонких коллагеновых волокон, окруженных большим количеством сосудов артериолярного, артериального типов (ангиоматоз). Подобные патологические изменения могут возникать в условиях тканевой гипоксии миометрия с развитием компенсаторного ангиоматоза, что затрудняет нормальное формирование плотной волокнистой соединительной ткани.
В случаях расползания матки по рубцу мы обнаружили морфологические признаки соединительнотканной дисплазии с нарушением стромально-васкулярных взаимоотношений, что, на наш взгляд, может иметь большое значение в патогенезе и морфогенезе подобного патологического процесса.
Заключение
Возвращаясь к клиническим ситуациям, становится понятным, что изменение тактики ведения родов у всех четырех женщин в пользу повторного КС оказалось своевременным и абсолютно оправданным. Роды с рубцом на матке после КС зачастую начинаются спонтанно. При появлении клинических признаков несостоятельности рубца на матке в родах метод родоразрешения очевиден – КС. Если при поступлении роженицы в стационар клинических признаков несостоятельности рубца на матке нет, целесообразно оценить состоятельность рубца на матке с помощью УЗИ для определения дальнейшей тактики ведения родов.
Изучение патогенетических механизмов развития неполного разрыва матки и расползания матки по рубцу с учетом морфологической оценки миометрия позволит дать прогностическую оценку их полноценности после операций КС.



