1 N.I. Pirogov Russian National Research Medical University, Moscow, Russia
2 Stavropol State Medical University, Stavropol, Russia
3 Kuban State Medical University, Krasnodar, Russia
4 Krasnoyarsk State Medical University named after prof. V.F. Voyno-Yasenetskii, Krasnoyarsk, Russia
5 Ural Research Institute of Maternal and Infant Care, Yekaterinburg, Russia
6 Nizhny Novgorod State Medical Academy, Nizhny Novgorod, Russia
7 South-Ural State Medical University, Chelyabinsk, Russia
8 Rostov State Medical University, Rostov-on-Don, Russia
9 Tula State Medical Institute, Tula, Russia
10 Yaroslavl State Medical Academy, Yaroslavl, Russia
11 Siberian State Medical University, Tomsk, Russia
12 Orenburg State Medical Academy, Orenburg, Russia
13 Voronezh State Medical University, Voronezh, Russia
14 Omsk State Medical University, Omsk, Russia
15 Irkutsk State Medical University, Irkutsk, Russia
16 Novosibirsk State Medical University, Novosibirsk, Russia
17 Kazan State Medical Academy, Kazan, Russia
18 Moscow State University of Medicine and Dentistry named after A.I. Evdokimov, Moscow, Russia
19 Regional Perinatal Center, Yekaterinburg, Russia
20 Perm State Medical University named after acad. E.A. Vagner, Perm, Russia
21 Baltic State University named after Immanuel Kant, Kaliningrad, Russia
22 Saratov State Medical University, Saratov, Russia
23 Bashkir State Medical University, Ufa, Russia
24 Volgograd State Medical University, Volgograd, Russia
25 Moscow Regional Perinatal Center, Balashikha, Russia
26 Astrakhan State Medical University, Astrakhan, Russia
27 St. Petersburg State Pediatric Medical University, St. Petersburg, Russia
28 D.O. Ott Scientific Research Institute of Obstetrics and Gynecology, St. Petersburg, Russia
Objective. To evaluate the first half of pregnancy (from 8 weeks 0 days to 22 weeks 0 days) during micronized progesterone (Utrogestan) administration in women with recurrent pregnancy loss, who had and did not have pregravard preparation with micronized progesterone in the multicenter Tristan-1 study.
Subject and methods. The study involved 800 women with recurrent pregnancy loss (2 or more consecutive interruptions of pregnancy in history). 383 patients in group 1 started taking micronized progesterone from pregravid preparation before conception during luteal phase of menstrual cycle and during pregnancy (intravaginally 200-400 mg per day), 417 pregnant women (group 2) started taking micronized progesterone only after clinical confirmation of pregnancy, from 8 weeks 0 days (intravaginally 200-400 mg per day). Observation of patients of both groups continued in the first half of pregnancy from 8 weeks 0 days until 22 weeks and 0 days of gestation. Current pregnancies were observed during the study: the use of additional drugs, the presence of complications, hospitalizations and their duration, as well as adverse events that occur in patients throughout the observation period. All performed medical research and procedures in the study were routine, used in everyday clinical practice. The statistical analysis of the data was performed using IBM SPSS 23.
Results. The main criterion for the therapy effectiveness was prolongation of current pregnancy from 8 weeks 0 days up to 22 weeks 0 days. In group 1 (who had micronized progesterone pregravid preparation), the frequency of pregnancy loss was 2.3%, while in group 2 (who start taking micronized progesterone only after clinical confirmation of pregnancy) – 7.7% (p <0.001). The analysis of the obtained data showed effectiveness and safety of micronized progesterone administration from pregravid stage for the therapy of recurrent pregnancy loss. It can be concluded that the relative risk of interruption of pregnancy decreases with the use of micronized progesterone during pregravid preparation and during pregnancy compared with the use of micronized progesterone only after clinical confirmation of gestation (from 8 weeks 0 days), RR = 0.306 (95% CI 0.148-0.633), p < 0.001. The frequency and nature of adverse events in the groups was statistically comparable (p> 0.05).
Conclusion. Results of the study demonstrate effectiveness and safety of micronized progesterone (Utrogestan) administration during pregravid preparation and during pregnancy up to 22 weeks 0 days of gestation in case of recurrent pregnancy loss. The use of micronized progesterone after clinical confirmation of pregnancy (from 8 weeks 0 days) is less effective.
recurrent pregnancy loss
habitual miscarriage
micronized progesterone
Utrozestan
pregravid preparation
Несмотря на успехи современной медицины в лечении невынашивания беременности, привычный выкидыш продолжает оставаться серьезной социальной проблемой [1–3]. В проведенных ранее социо-эпидемилогических исследованиях было показано, что около 15–25% всех клинически установленных беременностей заканчиваются самопроизвольным прерыванием [4]. Также имеются данные, что до 30–60% всех зачатий заканчиваются самопроизвольным прерыванием беременности [5]. Установлено, что риск потери повторной беременности после первого выкидыша составляет 13–17% (соответствует частоте спорадического выкидыша в популяции), тогда как после 2 предшествующих самопроизвольных прерываний риск потери желанной беременности возрастает более чем в 2 раза и составляет 36–38% [1].
По классификации, принятой ВОЗ, привычный выкидыш – это самопроизвольное прерывание беременности до 22 недель гестации 3 и более раз. Ранее принятые критерии, включающие не менее трех выкидышей, пересмотрены вследствие сопоставимой частоты повторного выкидыша после двух и трех потерь беременности [6]. На данный момент многие медицинские ассоциации (например, Американское общество репродуктивной медицины) считают, что данный диагноз правомочен при 2 и более самопроизвольных прерываний беременности до 22 недель гестации [4, 7, 8]. Российская ассоциация акушеров-гинекологов рекомендует считать привычным выкидышем 3 и более потерь беременности до 22 недель, но дополнительное обследование проводить уже после второго [9]. Учитывая это, большинство специалистов, занимающихся проблемой невынашивания, в настоящее время считают, что при 2 последовательных выкидышах следует отнести супружескую пару к категории привычного выкидыша с последующим обязательным обследованием и проведением комплекса мер по подготовке к беременности.
Привычный выкидыш полиэтиологичен. В структуре привычных потерь беременности выделяют генетические, анатомические, эндокринные, иммунологические, инфекционные и тромбофилические факторы [1]. Негативную роль играет курение, алкоголь, прием наркотический средств, низкий социально-экономический статус, недостаток массы тела, ожирение и стресс. Прегравидарная подготовка проводится с целью исключения или минимизации их неблагоприятного воздействия на будущую беременность. При исключении всех вышеперечисленных причин, ведущих к потере беременности, остается группа пациенток, генез привычного выкидыша у которых представляется неясным (идиопатические). В 50–70% случаев привычного выкидыша не удается выявить этиологическую причину данного заболевания [1, 4, 5].
По данным различных авторов, эндокринные причины привычного выкидыша отмечаются в 20% случаев [1]. Своевременное выявление и коррекция заболеваний эндокринных органов является одним из ключевых компонентов повышения эффективности прегравидарного и антенатального наблюдения. Нарушение образования или функции желтого тела, сопровождаемое снижением выработки прогестерона и формированием неполноценного эндометрия, называется недостаточностью лютеиновой фазы (НЛФ). Причины НЛФ у женщин репродуктивного возраста многообразны. НЛФ ассоциируется с недостаточным питанием, ожирением, чрезмерной физической нагрузкой, стрессом, возрастом, СПКЯ, эндометриозом, дисфункцией коры надпочечников, заболеваниями щитовидной железы, гиперпролактинемией, сахарным диабетом, использованием ВРТ, а также возникает в послеродовом периоде. Отмечается неблагоприятное воздействие на органы репродуктивной системы ряда лекарственных средств, радиации, алкоголя, курения, употребления наркотиков. Кроме того, НЛФ может иметь идиопатический характер [10, 11].
Наиболее значима прогестероновая поддержка в период прегравидарной подготовки. Прием прогестерона во вторую фазу менструального цикла до наступления беременности и на протяжении гестации эффективно снижает риск прерывания беременности до 20 недель в случае привычного выкидыша, а также статистически значимо увеличивает процент живорождения у данной категории пациенток, что продемонстрировано в двойном слепом рандомизированном плацебо-контролируемом исследовании [12]. Данный вопрос является одним из наиболее обсуждаемых в научном мире и представляет огромный интерес [13]. Для получения новых данных в отношении применения микронизированного прогестерона в рутинной клинической практике с целью профилактики и терапии привычного выкидыша было проведено многоцентровое наблюдательное исследование Тристан-1. Цель данного исследования – оценить течение первой половины беременности (до 22 недель 0 дней) на фоне применения препарата микронизированного прогестерона у женщин с привычным выкидышем, получавших и не получавших прегравидарную подготовку препаратом микронизированного прогестерона в рамках многоцентрового исследования Тристан-1.
Материал и методы исследования
В рамках многоцентрового наблюдательного исследования Тристан-1 было включено 800 беременных женщин с диагнозом привычный выкидыш (2 и более последовательных прерываний беременности в анамнезе). Для определения размера выборки использовалась формула расчета при сравнении двух частот (M. Bland, 2000). При этом расчет объема выборки проводился с учетом необходимой мощности 80% (β-ошибка 20%) и допустимой α-ошибки 5%, а также возможным 10% выбывании пациенток в группах. Клинически значимым эффектом в исследовании было принято снижение частоты прерывания беременности на 10% в исследуемой группе, что определило значение ожидаемой частоты явления в контрольной группе. Из числа общей выборки в анализ эффективности и безопасности были включены 383 пациентки группы 1, которые получали прегравидарную подготовку препаратом микронизированного прогестерона (утрожестан) до зачатия в лютеиновой фазе менструального цикла и в течение беременности (интравагинально 200–400 мг/сут.). Средняя продолжительность прегравидарной подготовки микронизированным прогестероном составила 3 менструальных цикла до планируемой беременности. 417 беременных, вошедших в группу 2, начали прием препарата микронизированного прогестерона только после клинического подтверждения наступления беременности, после 8 недель 0 дней гестации (интравагинально 200–400 мг/сут.). Набор пациентов велся в 31 исследовательском центре России.
Критериями включения в исследование служили: пациентки с диагнозом привычный выкидыш (имеющие в анамнезе 2 и более самопроизвольных выкидыша), в возрасте от 18 до 35 лет включительно, с прогрессирующей маточной беременностью на момент включения в исследование (с 8 недель 0 дней до 10 недель 6 дней беременности), наступившей на фоне или без прегравидарной подготовки препаратом микронизированного прогестерона спонтанно, подтвержденной УЗ-визуализацией плодного яйца в полости матки и с наличием сердцебиения эмбриона; информированное согласие пациентки на участие в исследовании. Решение врача о назначении пациентке препарата микронизированного прогестерона согласно утвержденной инструкции, а также о тактике дальнейшего ведения беременности принималось до включения пациентки в исследование и независимо от него.
Критерии исключения были следующими: применение любых гестагенов (за исключением микронизированного прогестерона) при прегравидарной подготовке и во время настоящей беременности; стимуляция овуляции, применение вспомогательных репродуктивных технологий; аномалии строения матки; ампутация шейки матки; миома матки с подслизистым расположением узла (клинически значимого размера); аномалии кариотипа родителей (если применимо); анеуплоидии, анэмбриония, пороки развития плода, как установленные причины потери предшествующих беременностей; врожденные тромбофилии: мутация гена фактора V (Лейденовская мутация), мутация гена протромбина (если применимо); прочие выявленные в процессе обследования клинически значимые причины невынашивания (включая, но не ограничиваясь): сахарный диабет, существующий до беременности, некомпенсированное нарушение функции щитовидной железы до беременности, злокачественные заболевания в анамнезе или в настоящее время, психиатрические заболевания; ИППП на момент включения в исследование; прием фермент-индуцирующих препаратов (антиконвульсанты, нейролептики, антидепрессанты, транквилизаторы), употребление психоактивных веществ до и во время беременности; многоплодная беременность; противопоказания к вынашиванию беременности.
Наблюдение за пациентками обеих групп продолжалось в первой половине беременности с момента включения в исследование до 22 недель и 0 дней гестации. В ходе исследования оценивалось течение текущей беременности: применение дополнительных лекарственных средств, наличие осложнений, госпитализации и их продолжительность, а также нежелательные явления, возникающие у пациенток в течение всего периода наблюдения. Все выполняемые медицинские исследования и процедуры в рамках проведения исследования были рутинными, используемыми в повседневной клинической практике, что определило неинтервенционный (наблюдательный) характер исследования.
Первичной конечной точкой, на основании которой оценивалась эффективность проводимой терапии, было пролонгирование текущей беременности с 8 недель 0 дней до срока 22 недель и 0 дней. Безопасность оценивалась по анализу всех нежелательных явлений (НЯ) и серьезных нежелательных явлений (СНЯ), начиная с момента подписания участницей исследования информированного согласия до момента окончания участия в исследовании.
Статистический анализ данных выполнялся с использованием программ IBM SPSS 23 и MS Excel 2016. Демографические данные, данные исходного состояния рассчитывались в виде частот или процентного отношения, или при помощи среднего значения (стандартного отклонения), медианы (межквартильного размаха), минимума и максимума, в зависимости от типа переменной. Для проверки гипотезы об исходной однородности групп исследования было проведено тестирование нулевых гипотез при помощи t-критерия Стьюдента (для количественных показателей между независимыми выборками с нормальным распределением в исследуемой популяции), критерия Манна–Уитни (для ординальных показателей или для интервальных показателей с распределением, отличающимся от нормального) или критерия χ2 (для качественных признаков). Если предпосылки применения критерия χ2 не выполнялись, применялся точный двусторонний критерий Фишера.
Для сравнительного анализа данных о нежелательных явлениях были подвергнуты анализу следующие параметры: количество, выраженность и длительность НЯ/СНЯ на фоне применения препаратов исследования, в группах исследования (на основании случаев НЯ, зафиксированных в формах отчета о НЯ в ИРК). Для сравнения частоты возникновения НЯ в группах исследования применялся критерий χ2, для сравнения степени выраженности (а также возможной причинно-следственной связи между препаратом и НЯ) применялся критерий Манна–Уитни.
Результаты исследования и обсуждение
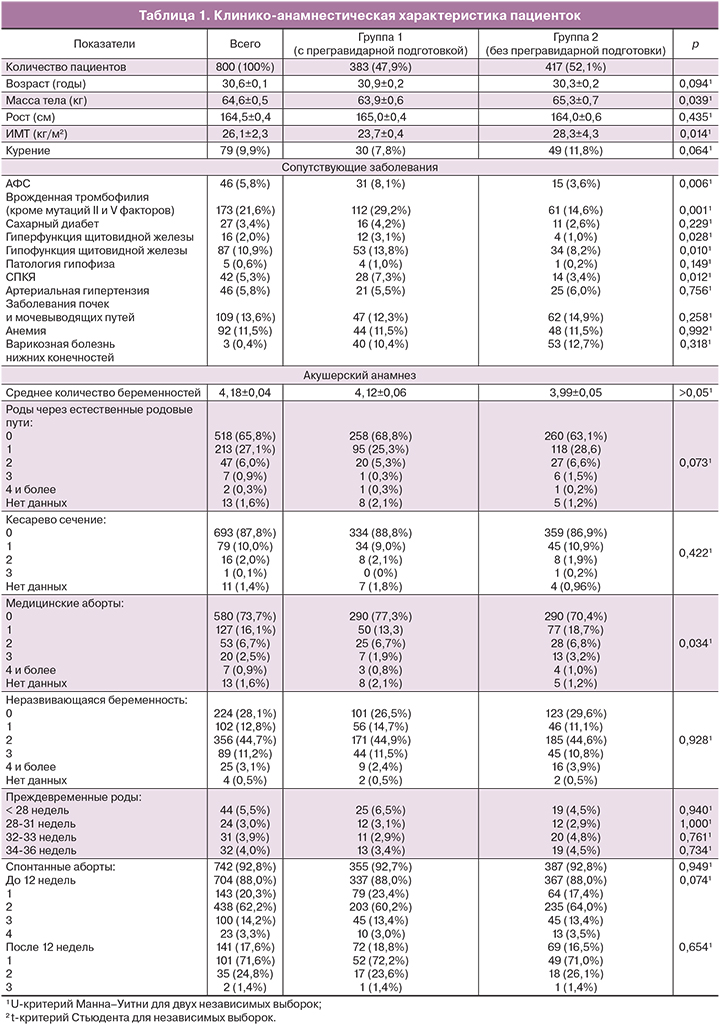
Пациентки обеих групп были однородны по ряду клинико-анамнестических характеристик, однако пациентки группы 2 имели статистически значимо большую массу тела на момент включения в исследовании (табл. 1). Также в группе 1 чаще встречались сопутствующие заболевания, такие как антифосфолипидный синдром, врожденные тромбофилии (кроме мутаций II и V факторов), патология щитовидной железы, синдром поликистозных яичников. Данный факт можно объяснить более тщательной диагностикой и верификацией патологии у пациенток, обратившихся к врачу с целью подготовки к беременности. Кроме того, пациентки группы 1 статистически реже переносили медицинские аборты в анамнезе, что, возможно, можно связать с социально-нравственными аспектами данной категории пациенток, заинтересованных в успешном течении гестации и своевременно обратившихся к врачу на этапе планирования данной беременности.
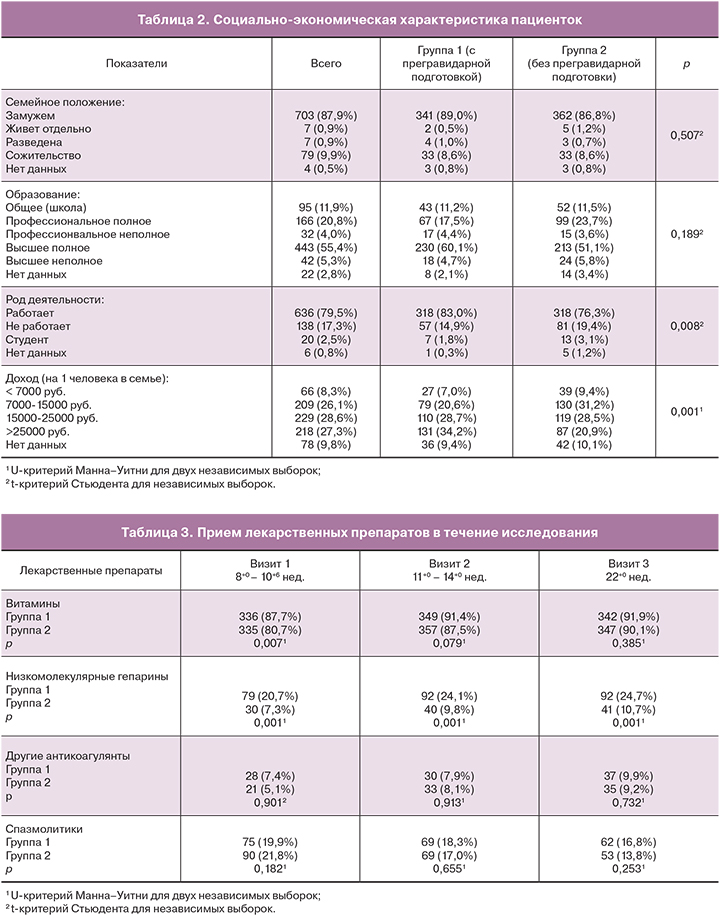
По социально-экономическим показателям пациентки различались в зависимости от группы исследования. Пациентки группы 1 (проходящие подготовку на прегравидарном этапе) чаще имели постоянную работу и более высокий материальный уровень, по сравнению с пациентками группы 2 (табл. 2). Кроме этого, пациентки группы 2 существенно реже проходили медико-лабораторное и генетическое обследование на выявление возможных причин привычного невынашивания (p<0,05). Таким образом, отсутствие прегравидарной подготовки микронизированным прогестероном у женщин с привычным выкидышем можно связать с более низким социально-экономическим статусом, а также меньшей заинтересованностью в текущей беременности по сравнению с пациентками группы 1.
Статистический обзор сопутствующей терапии показал, что пациентки группы 1 раньше начинали прием витаминно-минерального комплекса (p=0,007), а также чаще получали терапию низкомолекулярными гепаринами (p=0,001), что, вероятно, связано с верифицированной соматической патологией пациенток этой группы (тромбофилия) (табл. 3).
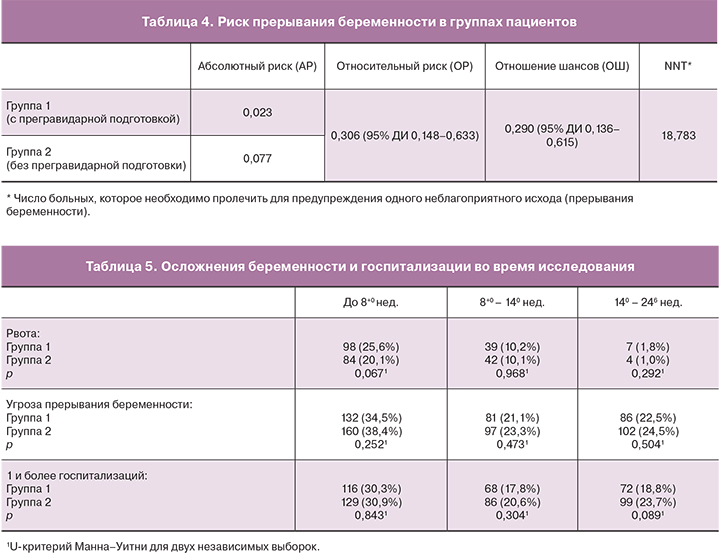
Анализ эффективности проведенной терапии показал, что частота прерываний беременности в группе 1 (прошедших прегравидарную подготовку препаратом микронизированного прогестерона) составила 2,3%, тогда как в группе 2 (начавших прием микронизированного прогестерона только после клинического подтверждения наступления беременности, с 8 недель 0 дней) – 7,7% (p<0,001). Генетический анализ абортусов прервавшихся беременностей в рамках исследования не выполнялся. Относительно низкий процент прерываний беременности в исследуемых группах по сравнению с популяционными значениями можно объяснить искусственными ограничениями на этапе включения пациентов в исследование, определенными критериями включения и невключения (в частности, включение беременных в исследование на сроке более 8 недель 0 дней и не старше 35 лет, что нивелирует большое число генетических причин выкидыша). Таким образом, можно сделать вывод о снижении относительного риска прерывания беременности при применении препарата микронизированного прогестерона во время прегравидарной подготовки и в течении беременности по сравнению с применением микронизированного прогестерона только после клинического подтверждения гестации, после 8 недель 0 дней, ОР=0,306 (95% ДИ 0,148–0,633) (табл. 4).
Полученные данные согласуются с ранее проведенными исследованиями, где также была показана эффективность микронизированного прогестерона во время прегравидарной подготовки и в течение ранних сроков гестации в случае привычного выкидыша [12, 14]. Достаточный уровень прогестерона на прегравидарном этапе обеспечивает полноценную секреторную трансформацию эндометрия, способствует успешной и полноценной имплантации, а также предупреждает запуск патологических процессов, способствующих прерыванию беременности на следующих этапах гестации. Начало терапии микронизированным прогестероном после клинического подтверждения наступления беременности менее эффективно, что также продемонстрировало международное исследование PROMISE [15].
По характеру и количеству осложнений беременности, а также по количеству госпитализаций и их продолжительности обе группы были статистически сопоставимы (табл. 5).
Оценка безопасности терапии, проводимая по анализу всех нежелательных явлений (НЯ) и серьезных нежелательных явлений (СНЯ), начиная с момента подписания участницей исследования информированного согласия до момента окончания участия в исследовании, показала, что две группы пациентов статистически однородны по изучаемым признакам (p>0,05).
Заключение
Представленные результаты исследования демонстрируют эффективность и безопасность применения микронизированного прогестерона (препарата утрожестан) при привычном выкидыше во время прегравидарной подготовки и в течение беременности до 22 недель 0 дней гестации. Применение микронизированного прогестерона после клинического подтверждения наступления беременности (после 8 недель 0 дней) менее эффективно. Продолжение данного исследования до момента родоразрешения всех пациенток (исследование Тристан-2) позволит достичь жесткой конечной точки (процент живорождения) и с высокой достоверной точностью оценить эффективность проводимой терапии на прегравидарном этапе и в течение беременности. Согласно полученным результатам исследования Тристан-1 назначение микронизированного прогестерона в программе прегравидарной подготовки женщинам с привычным выкидышем позволяет снизить риск потерь беременности с 8 до 22 недель.
1. Савельева Г.М., Сухих Г.Т., Серов В.Н., Радзинский В.Е., ред. Акушерство. Национальное руководство. 2-е изд. М.: ГЭОТАР-Медиа; 2015: 189-98. [Savelyeva G.M., Sukhikh G.T., Serov V.N., Radzinsky V.E., ed. Obstetrics. National guideline. 2nd ed. Moscow: GEOTAR-Media; 2015: 189-98. (in Russian)]
2. Сарибегова В.А., Тетруашвили Н.К., Кречетова Л.В., Агаджанова А.А., Вторушина В.В. Течение и исходы беременностей у женщин с идиопатическим привычным выкидышем при использовании иммуноцитотерапии. Акушерство и гинекология. 2017; 8: 68-73. https://dx.doi.org/10.18565/aig.2017.8.68-73 [Saribegova V.A., Tetruashvili N.K., Krechetova L.V., Agadzhanova A.A., Vtorushina V.V. The course and outcomes of pregnancy in women with idiopathic recurrent miscarriage during immunocytic therapy. Akusherstvo i Ginekologiya/Obstetrics and Gynecology. 2017; (8): 68-73. (in Russian) https://dx.doi.org/10.18565/aig.2017.8.68-73]
3. Трифонова Е.А., Ганьжа О.А., Габидулина Т.В., Девятьярова Л.Л., Сотникова Л.С., Степанов В.А. Генетические факторы в развитии привычного невынашивания беременности: обзор данных мета-анализов. Акушерство и гинекология. 2017; 4: 14-20. https://dx.doi.org/10.18565/aig.2017.4.14-20 [Trifonova E.A., Ganzha O.A., Gabidulina T.V., Devyatyarova L.L., Sotnikova L.S., Stepanov V.A. Genetic factors in the development of recurrent miscarriage: An overview of the data of meta-analyses. Akusherstvo i Ginekologiya/Obstetrics and Gynecology. 2017; (4): 14-20. (in Russian) https://dx.doi.org/10.18565/aig.2017.4.14-20]
4. The Practice Committee of the American Society for 4. Reproductive Medicine. Evaluation and treatment of recurrent pregnancy loss: a committee opinion. Fertil. Steril. 2012; 98(5): 1103-11.
5. Stephenson M.D., Awartani K.A., Robinson W.P. Cytogenetic analysis of miscarriages from couples with recurrent miscarriage: a case–control study Hum. Reprod. 2002; 17(2): 446-51.
6. Jaslow C.R., Carney J.L., Kutteh W.H. Diagnostic factors identified in 1020 women with two versus three or more recurrent pregnancy losses. Fertil. Steril. 2010; 93(4): 1234-43.
7. Oates-Whitehead R.M., Haas D.M., Carrier J.A. Progestogen for preventing miscarriage. Cochrane Database Syst. Rev. 2003; (4): CD003511.
8. Daya S. Efficacy of progesterone support for pregnancy in women with recurrent miscarriage. A meta-analysis of controlled trials. Br. J. Obstet. Gynaecol. 1989; 96: 275-80.
9. Серов В.Н., Сухих Г.Т., ред. Клинические рекомендации. Акушерство и гинекология. 4-е изд. М.: ГЭОТАР-Медиа; 2014: 62-104. [Serov V.N., Sukhikh G.T., ed. Clinical recommendations. Obstetrics and gynecology. 4th ed. Moscow: GEOTAR-Media; 2014: 62-104. (in Russian)]
10. Smith M.L., Schust D.J. Endocrinology and recurrent early pregnancy loss. Semin. Reprod. Med. 2011; 29(6): 482-90.
11. American Society for Reproductive Medicine. Current clinical irrelevance of luteal phase deficiency. A committee opinion. Fertil. Steril. 2015; 103(4): e27-32.
12. Ismail A.M., Abbas A.M., Ali M.K., Amin A.F. Peri-conceptional progesterone treatment in women with unexplained recurrent miscarriage: a randomized double-blind placebo-controlled trial. J. Matern. Fetal Neonatal Med. 2017; Feb. 15. doi: 10.1080/14767058.2017.1286315.
13. Christiansen O.B. Epidemiology of recurrent pregnancy loss. In: Carp H.J.A., ed. Recurrent pregnancy loss. Causes, controversies and treatment. 2nd ed. CRC Press; 2015: 1-16.
14. Stephenson M.D., McQueen D., Winter M., Kliman H.J. Luteal start vaginal micronized progesterone improves pregnancy success in women with recurrent pregnancy loss. Fertil. Steril. 2016; 107(3): 684-90.
15. Coomarasamy A., Williams H., Truchanowicz E., Seed P.T., Small R., Quenby S. A randomized trial of progesterone in women with recurrent miscarriages. N. Engl. J. Med. 2015; 373(22): 2141-8.
Received 01.09.2017
Accepted 22.09.2017
Saveleva Galina Mihaylovna, Doctor of Medicine, Professor, academician of the Russian Academy of Sciences, Department of Obstetrics and Gynecology, N.I. Pirogov
Russian National Research Medical University. 117997, Russia, Moscow, Ostrovityanova str. 1 Tel.: +74954329897. E-mail:
agpf-gms@rambler.ru
Aksenenko Viktor Alekseevich, Doctor of Medicine, professor, Department of Obstetrics and Gynecology, Stavropol State Medical University.
355017, Russia, Stavropol, Mira str. 310. Tel.: +79624026899. E-mail:
aksenenko.vic@yandex.ru
Andreeva Margarita Darchoevna, Doctor of Medicine, Professor, department of obstetrics, gynecology and perinatology, Faculty of advanced training and professional retraining of specialists. Kuban state medical university. 350063, Russia, Krasnodar, Sedina St., 4. E‑mail:
andreeva_md@mail.ru.
Bazina Marina Ivanovna, Doctor of Medicine, Professor, Department of Obstetrics and Gynecology, Krasnoyarsk State Medical University named
after prof. V.F. Voyno-Yasenetskii. 660034, Russia, Krasnoyarsk, Krasnoyarskiy rabochiy pr. 170
Bashmakova Nadezda Vasilievna, Doctor of Medicine, Professor, Director of Ural Research Institute of Maternity and Child Care, Ministry of Health of Russia.
620028, Russia, Ekaterinburg, Repina str. 1. Tel.: +73433718768. E-mail:
dr@niiomm.ru
Borovkova Lyudmila Vasilevna, Doctor of Medicine, Professor, Department of Obstetrics and Gynecology, Nizhniy Novgorod State Medical Academy.
603950, Russia, Nizhniy Novgorod, Minin and Pozharskiy Square, 10/1. Tel. +79519137727. E-mail:
BorovcovaLV@yandex.ru
Bryuhina Elena Vladimirovna, Doctor of Medicine, Professor, Department of Obstetrics and Gynecology South-Ural State Medical University.
454080, Russia, Chelyabinsk, Vorovskogo str. 64. E-mail:
elena-bruhina@rambler.ru
Bushtyreva Irina Olegovna, Doctor of Medicine, Professor, the Head of the Department of Obstetrics, Gynecology and Reproduction № 4, Rostov State Medical University, Ministry of Health of Russia; leading researcher, Research Center of Obstetrics, Gynecology and Perinatology, Ministry of Health of Russia.
344022, Russia, Rostov-on-Don, Nakhichevan lane 29. Tel.: +7928770972. E-mail:
kio4@mail.ru
Volkov Valeriy Georgievich, Doctor of Medicine, Professor, Department of Obstetrics and Gynecology, Tula State Medical Institute.
300012, Russia, Tula, pr. Lenina, 92. E-mail:
valvol@yandex.ru
Gurev Dmitriy Lvovich, assistant professor, Department of Obstetrics and Gynecology Yaroslavl State Medical Academy, Yaroslavl, Russia, Chief Obstetrician-Gynecologist
of the Department of Health and Pharmacy of the Yaroslavl Region. 150003, Yaroslavl, Z. Kosmodemyanskoy, 9. Tel. +74852729279. E-mail:
d_guriev@mail.ru
Dankova Irina, candidate of medical science, senior researcher, Research Department of Preservation of Reproductive Function, Ural Research Institute
for Maternity and Infancy. 620028, Russia, Yekaterinburg, Repina str. 1
Yuliya E. Dobrokhotova, Doctor of Medicine, Professor, Department of Obstetrics and Gynecology, N.I. Pirogov Russian National Research Medical University,
Ministry of Health of Russia. 117997, Russia, Moscow, Ostrovityanova str. 1. Tel.: +74952374033. E-mail:
pr.dobrohotova@mail.ru
Egorova Antonina Timofeevna, Doctor of Medicine, Professor, Department of Obstetrics and Gynecology,
Krasnoyarsk State Medical University named after prof. V.F. Voyno-Yasenetskii. 660034, Russia, Krasnoyarsk, Krasnoyarskiy rabochiy pr. 170
Ivanova Tatyana Vasilevna, assistant professor Department of Obstetrics and Gynecology, Siberian State Medical University.
634050, Russia, Tomsk, Moskovskiy trakt, 2. Tel.: +73822530423. E-mail:
office@ssmu.ru
Konstantinova Olga Dmitrievna, Doctor of Medicine, Professor, Department of Obstetrics and Gynecology, Orenburg State Medical University.
460000, Russia, Orenburg, Sovetskaya str. 6. Tel.: +73532520612. E-mail:
const55@mail.ru
Korotkih Irina Nikolaevna, Doctor of Medicine, Professor, Department of Obstetrics and Gynecology, Voronezh State Medical University.
394036, Russia, Voronezh, Studencheskaya str. 10. E-mail:
korotkikh_1950@mail.ru
Kravchenko Elena Nikolaevna, Doctor of Medicine, Professor, Department of Obstetrics and Gynecology, Omsk State Medical University.
644099, Russia, Omsk, Lenina str. 12. E-mail:
kravchenko.en@mail.ru
Kramarskiy Vladimir Aleksandrovich, Doctor of Medicine, Professor, Department of Obstetrics and Gynecology, Irkutsk State Medical University.
664000, Russia, Irkutsk, Krasnogo Vosstaniya, 1. E-mail:
kramarskye@mail.ru
Kuleshov Vitaliy Mihaylovich, Doctor of Medicine, Professor of the Department of Obstetrics and Gynecology, Novosibirsk State Medical University.
630091, Russia, Novosibirsk, Krasnyiy prospekt, 52. Tel.: +73833410436. E-mail:
kuleshov_vm@mail.ru
Lebedenko Elizaveta Yurevna, Doctor of Medicine, Professor of the Department of Obstetrics and Gynecology, Rostov State Medical University.
344022, Russia, Rostov-on-Don, per. Nahichevanskiy, 29. Tel.: 8 (863) 252-24-65. E-mail:
Lebedenko08@mail.ru
Maltseva Larisa Ivanovna, Doctor of Medicine, Professor, Department of obstetrics and gynecology № 1, Kazan State Medical Academy.
420012, Russia, Kazan, Mushtari str. 11. Tel.: +78432333487. E-mail:
laramalc@mail.ru
Manukhin Igor Borisovich, Honored Doctor of Russia, Doctor of Medicine, Professor, Department of Obstetrics and Gynecology, Medical Faculty, Moscow State University of Medicine and Dentistry, Ministry of Health of Russia. 127473, Russia, Moscow, Delegatskaya str. 20, bld. 1. Tel.: +74991782831. E-mail:
mgmsugyn@mail.ru
Martirosyan Sergey Valerevich, candidate of medical science, chief doctor of the regional perinatal center.
620000, Russia, Ekaterinburg, Serafimyi Deryabinoy, 32k2. E-mail:
smart.75@list.ru
Aleksandr Feliksovich Mihelson, Doctor of Medicine, Professor, Department of Obstetrics and Gynecology, Rostov State Medical University.
344022, Russia, Rostov-on-Don, per. Nahichevanskiy, 29. Tel: +78632522465
Olina Anna Aleksandrovna, Doctor of Medicine, Professor of the Department of Obstetrics and Gynecology, Academician E.A. Wagner Perm State Medical University, Ministry of Health of Russia. 614000, Russia, Perm, Petropavlovskaya str. 26. Tel.: +73422364472. E-mail:
olina29@mail.ru
Pashov Aleksandr Ivanovich, Doctor of Medicine, Professor of the Department of Obstetrics and Gynecology, Baltic State University named after Immanuel Kant.
236000, Russia, Kaliningrad, Aleksandra Nevskogo, 14. E-mail:
pachov@mail.ru
Rogozhina Irina Evgenevna, Doctor of Medicine, Professor, Department of Obstetrics and Gynecology, Saratov State Medical University.
410012, Russia, Saratov, Bolshaya Kazachya, 112. E-mail:
itg.r@yandex.ru
Sahautdinova Indira Venerovna, Doctor of Medicine, Professor, Department of Obstetrics and Gynecology, Bashkir State Medical University.
450000, Russia, Ufa, Lenina str. 3. Tel.: +73472721160. E-mail:
bgmu.ag@yandex.ru
Selikhova Marina, Doctor of Medicine, professor of the department of obstetrics and gynecology, Volgograd State Medical University.
400131, Russia, Volgograd, Pavshih boytsov sq. 1. Tel.: +78442417002. E-mail:
selichovamarina@yandex.ru
Serova Olga Fedorovna, Doctor of Medicine, professor, chief physician of the Moscow Regional Perinatal Center.
143900, Russia, Moscow Region, Balashikha, sh. Enthusiasts, 12
Sinchihin Sergey Petrovich, Doctor of Medicine, Professor, Department of Obstetrics and Gynecology, Astrakhan State Medical University.
414000, Russia, Astrakhan, Bakinskaya, 121. E-mail:
Doc_sinchihin@rambler.ru
Sichinava Lali Grigorevna, Doctor of Medicine, Professor, Department of Obstetrics and Gynecology, N.I. Pirogov Russian National Research Medical University.
117997, Russia, Moscow, Ostrovityanova str. 1
Tapilskaya Natalia Igorevna, Doctor of Medicine, Professor of the Department of Obstetrics and Gynecology, St Petersburg State Pediatric Medical University.
194100, Russia, St. Petersburg, Lithuanian str. 2
Tskhay Vitaliy Borisovich, Doctor of Medicine, Professor, Department of Perinatology, Obstetrics and Gynecology Medical Faculty,
V.F. Voyno-Yasenetsky Krasnoyarsk State Medical University. 660022, Russia, Krasnoyarsk, P. Geleznyaka str. 1. Tel.: +79232872134. E-mail:
tchai@yandex.ru
Yarmolinskaya Maria, Doctor of Medicine, Leading researcher of the Department of Reproduction Endocrinology, D.O. Ott Research Institute of Obstetrics, Gynecology,
and Reproductology; Professor in the Department of obstetrics and gynecology № 2, North-Western Federal Medical Research Center, Ministry of Health of Russia.
199034, Russia, Saint-Petersburg, Mendeleevskaya line 154. Tel.: +78123289849. E-mail:
m.yarmolinskaya@gmail.com
For citations: Saveleva G.M., Aksenenko V.A., Andreeva M.D., Bazina M.I., Bashmakova N.V., Borovkova I.V., Bryuhina E.V., Bushtyireva I.O., Volkov V.G., Gurev D.L., Dankova I.V., Dobrohotova Yu.E., Egorova A.T., Ivanova T.V., Konstantinova O.D., Korotkih I.N., Kravchenko E.N., Kramarskiy V.A., Kuleshov V.M., Lebedenko E.Yu., Maltseva L.I., Manuhin I.B., Martirosyan S.V., Mihelson A.F., Olina A.A., Pashov A.I., Rogozhina I.E., Sahautdinova I.V., Selihova M.S., Serova O.F., Sinchihin S.P., Sichinava L.G., Tapilskaya N.I., Tshay V.B., Yarmolinskaya M.I. Micronized progesterone therapy of recurrent pregnancy loss (results of multicenter Tristan-1 study). Akusherstvo i ginekologiya/Obstetrics and Gynecology. 2017; (11): 44-55. (in Russian)
https://dx.doi.org/10.18565/aig.2017.11.44-55






