В современном акушерстве cуществует стойкая тенденция к увеличению частоты органосберегающих операций на матке при неотложных состояниях – гипотоническом кровотечении, аномалии прикрепления плаценты, разрыве матки, акушерском перитоните после кесарева сечения и др. [1]. В последние годы все более актуальной становится проблема истинного врастания плаценты (placenta accreta), что связано с неуклонным ростом числа операций кесарева сечения, диагностических и лечебных внутриматочных вмешательств [1, 2]. Частота врастания плаценты, по данным разных авторов, колеблется от 1 случая на 540 родов до 1 случая на 70 000 родов с тенденцией к возрастанию частоты встречаемости этой патологии [2, 3].
Родоразрешение пациенток с предлежанием и врастанием плаценты сопровождается массивной кровопотерей, однако в последние годы применение кровесберегающих технологий (Cell-Saver и др.) позволило проводить интраоперационную реинфузию аутоэритровзвеси. Уменьшение интраоперационной кровопотери достигается экстравазальными методами (перевязка магистральных сосудов таза) или эндоваскулярными методами (эмболизация или баллонная окклюзия с эмболизацией или без) [4, 5].
Эндоваскулярная блокада кровотока (в маточных, общих подвздошных артериях) является современным методом предупреждения интраоперационной кровопотери и лечения массивных послеродовых кровотечений [6, 7].
Методика временной баллонной окклюзии подвздошных артерий изначально применялась для уменьшения кровопотери при миомэктомии, что способствовало уменьшению кровопотери и времени оперативного вмешательства [8, 9]. В акушерской практике метод используется для уменьшения кровопотери у пациенток с врастанием плаценты. Рост частоты кесарева сечения и органосохраняющих операций на матке создает проблему ведения последующих беременностей и родов у женщин с рубцом на матке. На формирование полноценного рубца влияет наличие адекватного кровоснабжения тканей в этой области, так как на фоне оптимальной микроциркуляции происходит полное восстановление мышечных волокон [10].
Целью нашего исследования было изучение состояния рубца после оперативного родоразрешения при врастании плаценты.
Материал и методы исследования
На клинических базах кафедры акушерства и гинекологии лечебного факультета РНИМУ им. Н.И. Пирогова за период 2010–2016 гг. было родоразрешено 17 пациенток с предлежанием и врастанием плаценты.
Проведен сравнительный анализ исходов 17 наблюдений оперативного родоразрешения путем операции кесарева сечения по поводу врастания плаценты. В зависимости от выбора метода проведения операции все пациентки были разделены на две группы. В 1-ю группу вошли 8 пациенток (47%) которым применялась стандартная методика кесарева сечения в нижнем маточном сегменте c последующим иссечением миометрия с вросшей плацентой и метропластикой. Во 2-ю группу вошли 9 пациенток (53%), у которых была применена методика, основными хирургическими этапами которой явились: срединная лапаротомия; донное кесарево сечение – продольный разрез в дне матки для извлечения плода (плацента остается in situ); зашивание разреза на матке; разрез в нижнем маточном сегменте, удаление плаценты с иссечением скомпрометированного миометрия с вросшей плацентой, метропластика. Выбор техники зависел от своевременности и правильности постановки диагноза. Пациенткам 1-й группы по различным причинам не был своевременно поставлен диагноз врастания плаценты.
Во 2-й группе диагноз врастания предлежащей плаценты установили во время беременности по данным ультразвукового исследования (УЗИ) и допплерографии. В нескольких наблюдениях для подтверждения диагноза беременным в плановом порядке проводили магнитно-резонансную томографию.
При гистологическом исследовании иссеченного миометрия во всех случаях отмечено врастание ворсин.
Ведение послеоперационного периода у всех пациенток осуществлялось по общепринятым правилам.
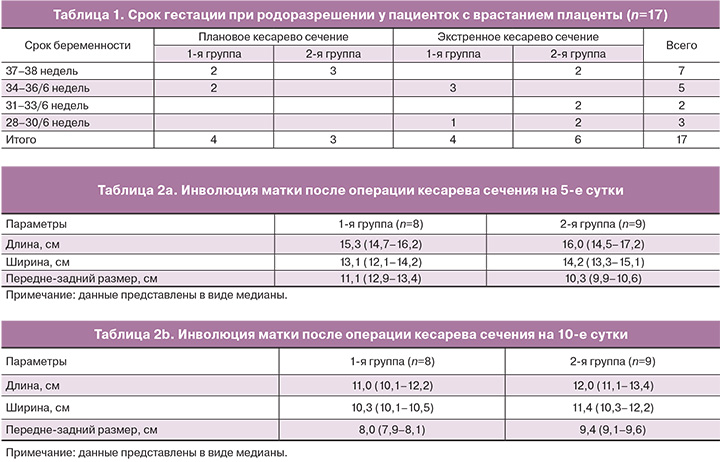
С помощью УЗИ проводилась сравнительная оценка инволюции матки: определялись длина, передне-задний размер, ширина на 5-е и 10-е сутки после абдоминального родоразрешения. Характер и особенности кровотока в области шва на передней стенке матки оценивались ультразвуковым методом с использованием цветного допплеровского картирования. Исследование проводилось в амбулаторных условиях на 14-е сутки послеоперационного периода, когда активное формирование капиллярной сети считается завершенным [11].
Через 8 месяцев проводилось повторное УЗИ для оценки состоятельности сформировавшегося рубца на передней стенке матке. Для определения жесткости ткани в области рубца применялся метод эластографии. Все исследования проведены с помощью ультразвуковой системы Aplio™ 500 компании Toshiba.
Статистический анализ полученных данных проводили с помощью современного пакета прикладных программ. Нормальность распределения показателей в группах проверяли с применением критерия Колмогорова – Смирнова. При малочисленности групп и неясности закона распределения величин использовали непараметрические критерии Манна–Уитни (U). Описательная статистика включала в себя определение медианы (Me). Определение значимости различий между качественными показателями проводилась с помощью критерия χ2, χ2 с поправкой Йейтса, точному критерию Фишера. Статистические гипотезы считались подтвержденными при уровне значимости р<0,05.
Результаты исследования и обсуждение
Все обследованные пациентки находились в возрасте от 21 до 38 лет, в 1-й группе (кесарево сечение в нижнем маточном сегменте) средний возраст беременных составил 28,8±4,5 года, во 2-й группе (донное кесарево сечение) – 31,0±3,9 года (p>0,05). Соматический анамнез у беременных обеих групп не был отягощен, в акушерско-гинекологическом анамнезе обращала внимание высокая частота самопроизвольных и искусственных абортов. Так, в 1-й группе частота самопроизвольных абортов в анамнезе составила 37,5%, во 2-й группе – 33,3% (p>0,05), неразвивающихся беременностей – соответственно 25 и 16,7% (p>0,05), искусственных абортов – 37,5 и 33,3% (p>0,05). В обеих группах у всех обследованных пациенток в анамнезе было кесарево сечение, что подтверждает данные литературы о роли рубца на матке в возникновении врастания плаценты. Предыдущее кесарево сечение у 5 пациенток было проведено в плановом порядке (36% всех пациенток с рубцом на матке), у 12 пациенток (64%) – в экстренном порядке. В 1-й группе показаниями к родоразрешению путем операции кесарева сечения были: острая гипоксия плода (n=2), клинически узкий таз (n=2), не готовность родовых путей (n=2); у двух пациенток – 1-я операция кесарева сечения в анамнезе (показания – преэклампсия (n=1), слабость родовой деятельности (n=1)). Во 2-й группе у всех обследованных пациенток рубец после одной операции имел место у 5 пациенток (показания – отсутствие эффекта от родовозбуждения (n=1), предлежание плаценты (n=1), крупный плод (n=1), тазовое предлежание (n=1), преждевременная отслойка нормально расположенной плаценты (n=1)); после 2 операций кесарева сечения – 4 пациентки (показание к первому кесареву сечению – острая гипоксия плода, ко второму – преэклампсия (n=1), синдром задержки роста плода (n=2), преждевременная отслойка нормально расположенной плаценты (n=1)).
Данная беременность у всех пациенток в обеих сравниваемых группах была одноплодной, протекала с угрозой прерывания у 9, с анемией – у 3, с плацентарной недостаточностью – у 4, многоводием – у 2 пациенток.

Диагноз врастания плаценты был поставлен 13 беременным из 17 при УЗИ и допплерографии (в 1-й группе – у 4 пациенток, во 2-й группе – у 9 обследуемых, p<0,05). У 4 (50%) беременных из 1-й группы до родоразрешения эхографических признаков врастания плаценты не было выявлено, placenta accreta диагностирована при вскрытии брюшной полости – обнаружен выраженный сосудистый рисунок в области нижнего сегмента матки. Истончение или отсутствие миометрия над плацентой – «маточная грыжа» – имело место у 8 из 17 пациенток.
Все беременные родоразрешены путем кесарева сечения (табл. 1) в различные сроки гестации. Следует отметить, что более точная диагностика врастания плаценты во 2-й группе способствовала применению методики донного кесарева сечения. В 1-й группе кесарево сечение было произведено в экстренном порядке у половины пациенток (n=4), а во 2-й группе – в 66,7% (n=6) случаях (p>0,05). Проведение кесарева сечения по экстренным показаниям, а также несвоевременная диагностика врастания плаценты повлияли на выбор методики родоразрешения: чрезплацентарный разрез на матке.
Всего в плановом порядке родоразрешены 7 (35,7%) пациенток, в экстренном – 10 (64,3%), показанием к экстренной операции явилось кровотечение (n=4), декомпенсированная плацентарная недостаточность (n=2), несостоятельность рубца на матке (n=4). При кровотечении объем кровопотери до родоразрешения составил 200 (100–300) мл.
При кесаревом сечении были извлечены 16 живых детей (доношенных – 6, недоношенных – 10) и 1 мертвый недоношенный ребенок (антенатальная гибель плода с множественными пороками развития).
У пациенток 1-й группы лапаротомия проводилась по старому рубцу, кесарево сечение в нижнем маточном сегменте (традиционный способ), чрезплацентарное вскрытие матки.
Во 2-ю группу были включены 9 пациенток, которым было произведено донное кесарево сечение. Преимуществом донного кесарева сечения является проведение метропластики после извлечения ребенка и перевязки внутренних подвздошных артерий или баллонной окклюзии общих подвздошных артерий, что позволяет более тщательно произвести отсепаровку мочевого пузыря для визуализации нижнего края неизмененного миометрия и минимизировать кровопотерю при иссечении маточной грыжи.
У всех пациенток применялись дополнительные методы: перевязка маточных артерий (9 наблюдений), внутренних подвздошных артерий (7 наблюдений), и в 1 случае – профилактическая окклюзия баллонными катетерами общих подвздошных артерий. Во всех случаях использовался аппарат Cell Saver и проводилась интраоперационная реинфузия аутоэритровзвеси. В 1-й группе объем кровопотери составил от 800 до 5000 мл, средний объем кровопотери 3037,5±150 мл, максимальный объем у 2 из 8 (25%) пациенток составил 5000 мл. Степень гиповолемии оценена как тяжелая у 5 пациенток (62,5%), средне тяжелая – у 1 (12,5%), легкая – у 2 пациенток (25%). Средний шоковый индекс в данной группе составил 1,2. У всех пациенток производилась катетеризация центральной вены, осуществлялся адекватный объем инфузионно-трансфузионной терапии под контролем центрального венозного давления, проводилась аппаратная реинфузия аутоэритровзвеси объемом 270 – 1750 мл (средний объем реинфузии составил 1117,1 мл), трансфузионная терапия свежезамороженной плазмы в объеме от 500 до 2300 мл и донорской эритромассы в 1 случае – 260 мл.
Во 2-й группе пациенток (донное кесарево сечение) объем кровопотери составил 900–3300 мл, (средний объем кровопотери 2083,3±150 мл), что статистически значимо отличалось от аналогичного показателя в 1-й группе (p<0,05). В данной группе степень гиповолемии расценена как тяжелая у 2 пациенток (22%), средне тяжелая – у 3 (33%), легкая у 4 пациенток (45%). Средний шоковый индекс в данной группе составил 1,1. Как и в 1-й группе, у всех пациенток перед операцией катетеризировалась центральная вена, осуществлялась адекватная инфузионно-трансфузионная терапия под контролем центрального венозного давления. У всех родильниц проводилась аппаратная реинфузия аутоэритровзвеси объемом 850–1700 мл (средний объем реинфузии – 1278,8 мл).
При гистологическом исследовании иссеченного миометрия передней стенки матки и плаценты отмечено врастание ворсин в мышечную ткань.
На следующем этапе мы оценивали характер инволюции матки. УЗИ проводилось на 5-е и 10-е сутки послеоперационного периода. Определялись длина, ширина и передне – задний размер матки. Были рассчитаны средние значения для каждой группы. При оценке параметров в обеих группах отмечалась субинволюция матки (табл. 2 a и b).
При сравнении полученных данных отмечено замедление процессов восстановления размеров в группе с двумя швами на матке.
Для оценки местного кровотока в послеоперационной области на передней стенке матки было проведено исследование в режиме цветного допплеровского картирования с определением количества визуализируемых сосудов в данной зоне на 14-е сутки. Во время данного исследования во 2-й группе наблюдалось выраженное увеличение количества визуализируемых сосудов в области послеоперационного рубца, что свидетельствует о запуске процесса неоангиогенеза и восстановлении адекватного кровоснабжения данной области (рис. 1а и б). Сниженное количество визуализируемых сосудов может быть обусловлено возникновением стойкой ишемии в тканях, приводящей к длительному нарушению микроциркуляции.
Последующие УЗИ производились через 8 месяцев после оперативного родоразрешения для оценки состоятельности сформировавшегося рубца на матке. В качестве критериев состоятельности определялись: положение рубца, наличие деформаций и «ниш», адекватный кровоток, толщина миометрия в области рубца, данные эластографии.
В группе с применением методики донного кесарева сечения дефектов миометрия в виде «ниш» обнаружено не было. В группе, где родоразрешение по поводу врастания плаценты проводилось стандартным способом, у 1 пациентки был обнаружен дефект миометрия в области рубца в виде «ниши» со стороны полости матки с истончением маточного сегмента до 4 мм (рис. 2а и б).
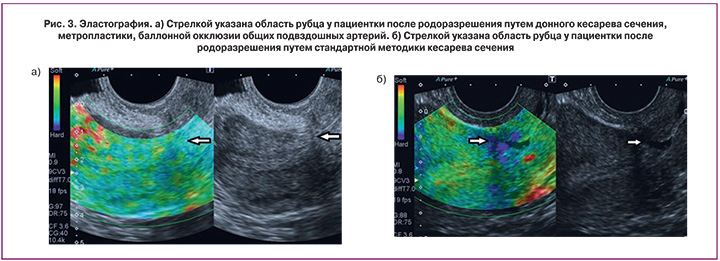
С помощью эластографии в режиме реального времени с цветовым кодированием изображения была исследована область послеоперационного рубца в обеих группах. Данная методика дает возможность определять эластические (упругие) свойства ткани в дополнение к данным об эхоструктуре. Синим цветом на изображении отмечаются участки более плотные по своей структуре. При изучении эластичности тканей миометрия в области рубца получены следующие результаты: в 1-й группе в области рубца ткань по структуре очень жесткая (синий цвет) в 5 (62,5%) наблюдениях, менее жесткая (зеленый цвет) – в 2 (25%), в 1 (12,5%) наблюдении зафиксирован миометрий желтого цвета. Во 2-й группе в 5 (56%) наблюдениях миометрий в области рубца желтого цвета, в 2 (22%) – зеленого, в 2 (22%) наблюдениях – красного цвета. Преобладание красного и желтого цвета свидетельствует о наличии более эластичной ткани в зоне исследования (рис. 3а). Наличие синего и зеленого цвета свидетельствует о повышенной жесткости в области рубца (рис. 3б). Отсюда следует, что у этих пациенток в зоне исследования повышено содержание соединительной ткани, а не мышечной, что в дальнейшем может привести к несостоятельности рубца. Полученные данные объединены в табл. 3.
Данные приведенные в таблице показывают, что процесс формирования рубца у пациенток, перенесших донное кесарево сечение, происходит с преобладанием эластичных мышечных волокон.
Заключение
Анализ проведенной работы позволяет заключить, что беременность с рубцом на матке после кесарева сечения и предлежанием плаценты входит в группу риска по ее врастанию. Повторное оперативное родоразрешение и выполнение кесарева сечения по экстренным показаниям повышают риск врастания.
Своевременная диагностика этого осложнения позволяет подготовиться к операции, применить новые технологии, сформировать высоко профессиональную бригаду. Это дает возможность снизить интраоперационную кровопотерю, оперировать в спокойной, рабочей обстановке, что будет способствовать лучшей визуализации тканей, тщательному сопоставлению их, позволит избежать излишнего перетягивания тканей и попадания в шов большей части мышечных волокон, создавая тем самым ишемию.
Ранний послеоперационный период у пациенток с донным кесаревым сечением характеризуется несколько отсроченной инволюцией матки. Такая субинволюция, на наш взгляд, объясняется наличием двух швов (в последствие формирующихся рубцов). Однако это не нарушает процессы репарации и заживления тканей, что доказывается лейкоцитарной, температурной реакцией и общим состоянием родильниц.
Тщательный гемостаз и сопоставление тканей обеспечивает правильное формирование рубца, микроинвазию сосудов (ангиогенез), отсутствие ишемии. Эти процессы способствуют образованию полноценного рубца, что определяется в дальнейшем при помощи различных методов УЗИ.
Полученные данные следует учитывать у беременных, входящих в группу риска по врастанию плаценты.



