Артериальная гипотония является одним из распространенных патологических состояний у новорожденных в отделениях интенсивной терапии и реанимации (ОРИТН), в особенности это касается недоношенных пациентов [1, 2]. На основании ряда исследований предполагается причинно-следственная связь между системной гипотензией и рядом тяжелых осложнений неонатального периода, таких как внутрижелудочковые кровоизлияния (ВЖК) и неблагоприятные неврологические исходы [1, 3, 4]. Частота артериальной гипотонии среди пациентов ОРИТН по данным разных авторов составляет 16–52%. [1–4]
Существует несколько алгоритмов терапии артериальной гипотонии у новорожденных, включающих введение объемзамещающих растворов с последующим назначением кардиотонических препаратов. В подавляющем большинстве клиник в качестве первого шага в терапии артериальной гипотонии используется инфузия физиологического раствора в дозе 10–15 мл/кг/ч [5–7]. Значительно реже с этой целью используются другие растворы – ГЭК и альбумин [8]. Вопрос об использовании альбумина в неонатологии остается до настоящего времени весьма спорным. Отсутствие убедительных данных о его преимуществах перед физиологическим раствором (ФР), большое число осложнений, связанных с его применением, привели к тому, что в последние годы альбумин не используется в мировой неонатальной практике в качестве объемзамещающего раствора.
 ГЭК, напротив, доказали свою эффективность и безопасность в экспериментальных работах, они широко используются в педиатрической и взрослой практике, в особенности у хирургических пациентов [9]. Однако отношение к использованию ГЭК в неонатальной практике оставалось до сих пор настороженным, несмотря на то что ряд препаратов этого класса зарегистрирован для применения по этим показаниям у новорожденных. Одним из наиболее современных препаратов этого класса, разрешенных для применения в неонатологии, является волювен (ГЭК 130/0,4 – 6% гидроксиэтилкрахмал; Fresenius Kabi, Германия). Волювен является раствором ГЭК, который получают из амилопектина, средний молекулярный вес составляет 130 000 Да, а степень замещения – 0,38–0,45 (130/0,4), что означает, что на 10 глюкозных остатков амилопектина приходится около 4 гидроксиэтиловых групп. Волювен 6% структурно родственен гликогену, что объясняет его высокую толерантность и низкий риск анафилактических реакций. Фармакокинетика ГЭК зависит от молекулярного веса и степени молекулярного замещения вещества. После внутривенного введения гидроксиэтилкрахмалов молекулы размером менее 60 000–70 000 Да (порога почечной фильтрации) быстро выводятся с мочой, а более крупные молекулы, в том числе и волювен, расщепляются α-амилазой плазмы крови, после чего тоже выводятся через почки. Средний молекулярный вес волювена в первые минуты после инфузии составляет в плазме крови in vivo 70 000–80 000 Да и остается выше порога почечной фильтрации в течение всего периода лечения.
ГЭК, напротив, доказали свою эффективность и безопасность в экспериментальных работах, они широко используются в педиатрической и взрослой практике, в особенности у хирургических пациентов [9]. Однако отношение к использованию ГЭК в неонатальной практике оставалось до сих пор настороженным, несмотря на то что ряд препаратов этого класса зарегистрирован для применения по этим показаниям у новорожденных. Одним из наиболее современных препаратов этого класса, разрешенных для применения в неонатологии, является волювен (ГЭК 130/0,4 – 6% гидроксиэтилкрахмал; Fresenius Kabi, Германия). Волювен является раствором ГЭК, который получают из амилопектина, средний молекулярный вес составляет 130 000 Да, а степень замещения – 0,38–0,45 (130/0,4), что означает, что на 10 глюкозных остатков амилопектина приходится около 4 гидроксиэтиловых групп. Волювен 6% структурно родственен гликогену, что объясняет его высокую толерантность и низкий риск анафилактических реакций. Фармакокинетика ГЭК зависит от молекулярного веса и степени молекулярного замещения вещества. После внутривенного введения гидроксиэтилкрахмалов молекулы размером менее 60 000–70 000 Да (порога почечной фильтрации) быстро выводятся с мочой, а более крупные молекулы, в том числе и волювен, расщепляются α-амилазой плазмы крови, после чего тоже выводятся через почки. Средний молекулярный вес волювена в первые минуты после инфузии составляет в плазме крови in vivo 70 000–80 000 Да и остается выше порога почечной фильтрации в течение всего периода лечения.
По сравнению с ГЭК 200/0,5 (рефортан, инфукол) волювен обладает оптимизированной фармакокинетикой при сопоставимом плазмозамещающем эффекте. Кроме того, волювен в меньшей степени влияет на систему гемостаза, чем ГЭК 200/0,5.
Целью нашего проспективного рандомизированного открытого исследования была оценка эффективности применения ГЭК 130/0,4 (волювен 6%) как стартового препарата для терапии артериальной гипотонии в раннем неонатальном периоде.
Материал и методы исследования
Исследование проводилось в период с января 2010 г. по сентябрь 2011 г. на базе ФГБУ Научный Центр акушерства, гинекологии и перинатологии им. академика В.И. Кулакова Минздрава России (ФГБУ НЦ АГиП МЗ РФ), директор – академик РАМН Г.Т. Сухих. В исследование включались новорожденные, поступившие в отделение реанимации и интенсивной терапии отдела неонатологии и педиатрии ФГБУ НЦ АГиП МЗ РФ, заведующий О.В. Ионов. Дизайн исследования был одобрен этическим комитетом Центра.
Критерии включения: все новорожденные, поступавшие в отделение интенсивной терапии и реанимации новорожденных, независимо от диагноза и гестационного возраста (ГВ), у которых диагностировали артериальную гипотонию в первые сутки жизни. Критерии артериальной гипотонии: среднее артериальное давление (мм рт. ст.), измеренное осциллометрическим методом на правом или левом плече манжетой соответствующего размера в трех последовательных измерениях – меньше ГВ в неделях.
Критерии исключения: Активное кровотечение у новорожденного: желудочно-кишечное кровотечение, легочное кровотечение, свежее (менее 24 ч) ВЖК, кровоточивость из мест инъекций, кефалогематома.
Исключение из исследования новорожденных с геморрагическим синдромом было обусловлено отсутствием достоверных данных о безопасности применения гидроксиэтилкрахмалов у новорожденных при нарушениях гемостаза.
Рандомизация проводилась с помощью календаря на основании даты включения в исследование:
Четные числа (2, 4, 6… и т. д.) – вводился волювен 6% в объеме 10 мл/кг в течение 1 ч.
Нечетные числа (1, 3, 5… и т. д.) – вводился физиологический раствор (ФР) в объеме 10 мл/кг в течение 1 ч.
Последующее ведение пациентов строго соответствовало принятому в исследовании протоколу: если через 30 мин после начала введения объемзамещающего раствора (волювен или ФР) не происходило нормализации среднего АД, в терапию включался допамин в дозе 2 мкг/кг/мин (для новорожденных с экстремально низкой массой тела (ЭНМТ) – с 1 мкг/кг/мин) с увеличением дозы на 1–2 мкг/кг/мин каждые 15 мин до нормализации АД.
Всем новорожденным, включенным в исследование, проводился мониторинг артериального давления, ЧСС, диуреза. До начала терапии и после инфузии объемзамещающего раствора исследовался рН крови, уровень рСО2, рО2, глюкозы, лактата, ВЕ, а также проводилось эхокардиографическое исследование. Оценивались следующие параметры: фракция выброса, фракция укорочения, сердечный выброс, в передней мозговой артерии (ПМА) и почечной артерии (ПА) – индекс сосудистой резистентности (Ri), усредненная по времени максимальная линейная скорость кровотока (Tамx), в верхней брыжеечной артерии – индекс сосудистой резистентности, пульсативный индекс, конечная диастолическая скорость (MD). В протокол обследования после применения объемзамещающего раствора входили следующие исследования: исследование гемостаза (фибриноген, активированное частичное тромбопластиновое время (АЧТВ), протромбиновый индекс (ПТИ), протеин С), биохимический анализ крови, клинический анализ крови. Мониторировалось также время нормализации АД и продолжительность регистрации стабильного АД после введения препарата.
В дальнейшем оценивались следующие показатели: продолжительность эпизода гипотонии, суммарная доза кардиотоников за сутки, за 7 сут и длительность применения кардиотоников.
Статистический анализ. Для исследования различий средних значений показателей в группах использовался непараметрический критерий Манна–Уитни для количественных значений, а также критерии Фишера и χ2 для сравнения количественных значений. При значении р<0,05 отмечаемые различия в средних значениях показателя между сравниваемыми группами считались достоверными. Числовые данные в таблицах указаны по единому принципу – это либо абсолютные числа с указанием процента от общего числа, либо М±SD, где М – среднее значение, SD – стандартное отклонение.
Результаты исследования и обсуждение
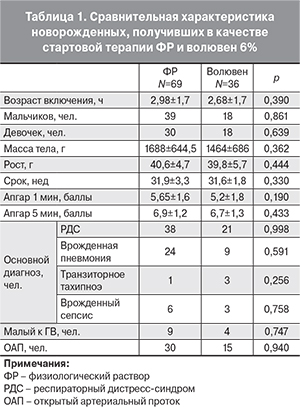
В результате рандомизации в группу, получившую в качестве стартовой терапии артериальной гипотонии ФР, были включены 69 новорожденных. В группу, получившую в качестве стартовой терапии волювен, были включены 36 новорожденных. В табл. 1 представлена характеристика новорожденных, включенных в исследование. Группы были сопоставимы по весу, росту, гестационному возрасту, распределению по полу, оценке по шкале Апгар, количеству новорожденных с задержкой внутриутробного развития, а также возрасту включения в исследование (возрасту регистрации артериальной гипотонии). Распределение основных диагнозов в группах также достоверно не отличались.
 В качестве критерия эффективности оценивалась потребность в последующей инфузии допамина, ее объем и последующая продолжительность кардиотонической поддержки. Изолированное применение волемической нагрузки (без возникновения потребности в кардиотонической терапии) было эффективно в отношении нормализации АД в 69,4% случаев при применении волювена 6% и в 52% случаев при применении ФР.
В качестве критерия эффективности оценивалась потребность в последующей инфузии допамина, ее объем и последующая продолжительность кардиотонической поддержки. Изолированное применение волемической нагрузки (без возникновения потребности в кардиотонической терапии) было эффективно в отношении нормализации АД в 69,4% случаев при применении волювена 6% и в 52% случаев при применении ФР.
В группе волювена достоверно меньше была потребность в допамине и суммарная продолжительность кардиотонической поддержки. Суммарная доза (в мкг/кг веса) допамина оценивалась за сутки и за 7 сут. В группе ФР она составила 3139±2596 мкг/кг и 14449±1415,6 мкг/кг соответственно, в группе волювена – 740±98,9 мкг/кг и 9866±1052 мкг/кг (р<0,0001 в обоих случаях). Суммарная продолжительность кардиотонической поддержки составила 110±15,3 ч в группе ФР и 65±58 ч в группе волювена (р<0,0001).
Кроме того, потребность в инфузии допамина возникала достоверно позже в группе волювена – через 6,6±3,67 ч, чем в группе ФР – через 2,3±0,6 ч (р<0,0001). Данные демонстрируют значительное преимущество применения волювена в качестве стартовой терапии новорожденных в отношении снижения потребности в последующей кардиотонической поддержке.
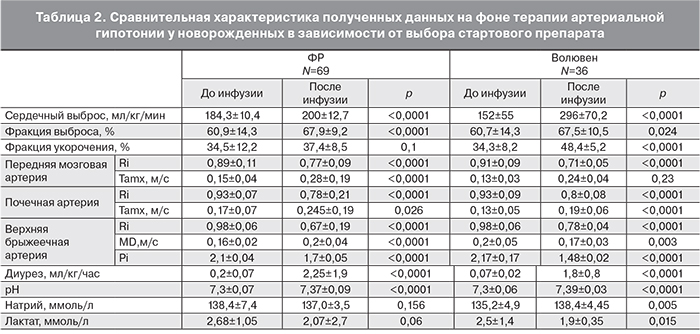
При сравнительном анализе показателей центральной и регионарной гемодинамики у новорожденных (табл. 2), получавших в качестве стартовой терапии артериальной гипотонии волювен и ФР, выяснилось следующее. На фоне инфузии обоих растворов отмечалось достоверное увеличение фракции выброса, достоверное увеличение сердечного выброса. При этом увеличение сердечного выброса при инфузии волювена 6% значительно выше в сравнении с ФР, что может иметь решающее значение при шоках. Достоверное увеличение фракции укорочения на фоне инфузии отмечено только при использовании волювена 6%.
На основании полученных нами данных можно говорить о том, что инфузия обоих препаратов нормализует регионарный кровоток, увеличивая объемные скорости мозгового, почечного и кишечного кровотока, снижая индекс сосудистой резистентности в передней мозговой и почечной артериях, в верхней брыжеечной артерии отмечалось достоверное снижение индекса сосудистой резистентности и пульсативного индекса.
После инфузии обоих препаратов отмечалось достоверное увеличение диуреза. Исследование уровня рН и лактата до и после инфузии препарата показало достоверное увеличение рН при использовании обоих растворов. Однако достоверное снижение уровня лактата до нормальных значений регистрировалось только после инфузии волювена 6% (табл. 2), что может играть решающую роль при выборе препарата при терапии артериальной гипотонии, сопровождающейся снижением перфузии тканей (шоке). Несмотря на содержание натрия в обоих растворах, достоверного увеличения уровня натрия в сыворотке крови при применении обоих препаратов отмечено не было.
С целью оценки выраженности прибавки массы и косвенной оценки развития отечного синдрома мы проанализировали также объемы вводимой жидкости, суточный диурез и данные об изменениях массы тела в первые 72 ч жизни у новорожденных с артериальной гипотонией, терапия которой проводилась ФР или волювеном.
Выяснилось, что в первые сутки жизни детям, получившим в качестве стартовой терапии волювен, потребовался достоверно больший объем жидкости в пределах средних нормативных для этого возраста и веса значений (97,9±20,06 мл/кг против 87,8±17,3 мл/кг, р=0,009). Вероятно, это было обусловлено более высоким в сравнении с группой ФР диурезом (4,3 мл/кг/час против 2,45 мл/кг/час, р<0,0001). Объем жидкости на 2-е и 3-е сутки жизни достоверно не различался в обеих группах, в то время как диурез оставался более высоким в группе волювена в сравнении с группой ФР.
Учитывая, что для новорожденных первых 24 ч жизни характерна потеря массы тела, мы проанализировали долю новорожденных, прибавивших в массе в каждой группе.
Несмотря на то что количество новорожденных, прибавивших в весе, достоверно не различалось в обеих группах (около 30%), средняя прибавка массы в 1-е сутки была достоверно ниже в группе волювена и составила 22,0±10,0 г, в то время как прибавка веса в группе ФР была 42,0±36 г, р=0,002.
Таким образом, можно говорить о том, что при применении волювена в качестве препарата для терапии артериальной гипотонии не происходит патологической задержки жидкости и достоверно увеличивается диурез.
С целью изучения профиля безопасности применения препарата волювен 6% всем новорожденным исследовался гемостаз и биохимический анализ крови после инфузии.
При исследовании гемостаза после применения препаратов (ФР и волювен) у новорожденных группы волювена отмечено умеренное удлинение АЧТВ в сравнении с группой ФР (77,9±22,9 с против 68,2±18 с, р=0,019). Также у новорожденных группы волювена отмечено увеличение уровня креатинина. Достоверных отличий в содержании печеночных ферментов, уровня протеина С и показателях протромбинового индекса выявлено не было.
Учитывая удлинение АЧТВ после терапии волювеном 6%, было решено проанализировать особенности новорожденных с удлинением АЧТВ. Подавляющее большинство из них относились к новорожденным с ЭНМТ. В связи с этим было решено проанализировать уровень АЧТВ и креатинина отдельно по группам в зависимости от веса при рождении.
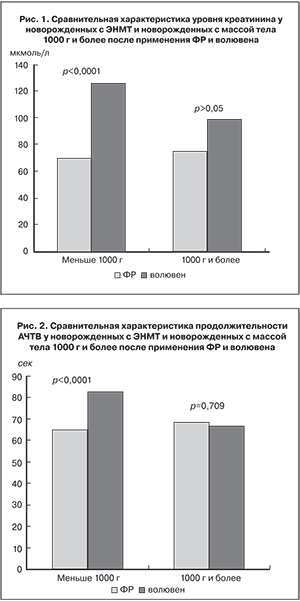
Как видно из диаграммы (рис. 1), достоверных различий в уровне креатинина до и после инфузии волювена в сравнении с ФР не было выявлено в группе новорожденных с массой при рождении 1000 г и более. С другой стороны, в группе пациентов с ЭНМТ отмечался достоверно более высокий уровень креатинина плазмы.
Достоверное удлинение АЧТВ при применении волювена (рис. 2) отмечается только в группе новорожденных с ЭНМТ (65,33±11,06 с в группе ФР и 82,8±22,9 с в группе волювена), в то же время отсутствуют достоверные различия в продолжительности АЧТВ у новорожденных весом 1000 г и более (68,7±19,3 с в группе ФР и 67,1±16,14 с в группе волювена).
Потребность в допамине у пациентов массой более 1000 г в группе ФР была достоверно выше (41,6%), чем в группе волювена (22,2%), р=0,03. В то же время при анализе потребности в инфузии допамина у пациентов массой менее 1000 г достоверных отличий выявлено не было (группа ФР – 45,8%, группа волювена – 66,6%, р=0,735). Таким образом, преимущество волювена перед ФР в отношении снижения потребности в кардиотонической поддержке отмечено только у пациентов с массой тела 1000 г и более.
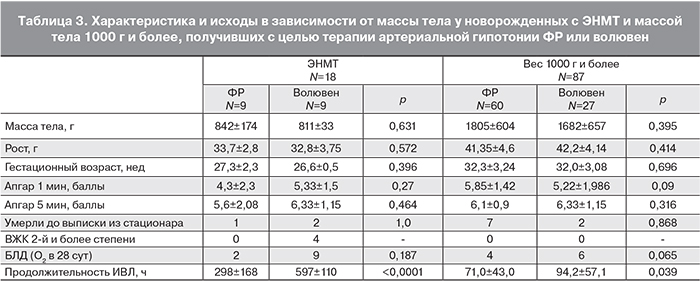
Исходы анализировались отдельно в весовой группе до 1000 г (ЭНМТ) и 1000 г и более (табл. 3). Внутри групп новорожденные, получившие волювен и ФР, были сопоставимы по весу, росту, ГВ и оценке по шкале Апгар, они достоверно не различались по летальности до выписки из стационара.
В группе новорожденных с ЭНМТ имелись достоверные различия по исходам – чаще дети, получившие волювен, развивали тяжелые ВЖК и дольше они требовали ИВЛ (расшифровка). В группе с массой тела 1000 г и более различий в отношении потребности в ИВЛ и частоте ВЖК отмечено не было.
Заключение
В результате проведенного исследования выяснилось следующее. Инфузия ФР и волювена у новорожденных с артериальной гипотонией достоверно увеличивает диурез, объемную скорость мозгового, почечного и кишечного кровотока, снижает индекс сосудистой резистентности в описанных артериях.
На фоне терапии обоими препаратами достоверно увеличивается фракция выброса и сердечный выброс. При этом влияние на сердечный выброс в большей степени выражено при инфузии волювена.
Применение волювена в сравнении с ФР с целью терапии артериальной гипотонии имеет ряд преимуществ: отмечается улучшение сократительной способности миокарда (выражающееся в увеличении фракции укорочения), эффективность препарата в терапии артериальной гипотонии была выше (52 против 69,4%). При этом потребность в присоединении инфузии допамина у новорожденных, получивших волювен, возникала достоверно позже, была достоверно меньше выражена, кроме того, достоверно меньше была продолжительность кардиотонической поддержки.
К очевидным преимуществам волювена можно отнести достоверное снижение уровня лактата до нормальных значений на фоне его инфузии, более выраженное влияние на уровень сердечного выброса и уровень суточного диуреза, что может иметь решающее значение при терапии шока.
В результате проведенного детального анализа выяснилось, что осложнения от введения волювена (увеличение частоты тяжелых ВЖК, высокий уровень креатинина и АЧТВ) отмечаются только у категории пациентов с ЭНМТ, у которой не отмечено преимуществ от его введения.
При этом следует отметить, что число пациентов с ЭНМТ, получивших волювен и ФР, было невелико (18 человек), поэтому для получения более достоверной информации о применении ГЭК у детей с ЭНМТ, вероятно, требуются более масштабные исследования. Однако в настоящее время препарат не может быть рекомендован как стартовая терапия артериальной гипотонии у новорожденных с ЭНМТ.
Таким образом, волювен может быть рекомендован для терапии артериальной гипотонии у новорожденных наряду с ФР, в особенности в ситуациях, когда помимо нормализации АД необходимо быстрое и эффективное увеличение СВ и нормализация перфузии тканей – при шоковых состояниях.



