Бременем современного урогинекологического сообщества является вопрос использования синтетических материалов в хирургии тазового дна. Непрекращающиеся дискуссии и споры о целесообразности применения имплантов в условиях генитального пролапса, недержания мочи до сих пор не привели к формированию универсального алгоритма или тактики ведения пациентов с дисфункцией тазового дна [1]. С одной стороны, коррекция пролапса тазовых органов за счет сетчатых протезов сопряжена с риском возникновения mesh-ассоциированных (связанных с имплантацией протеза – mesh) осложнений, с другой – пластика стенок влагалища собственными тканями имеет больший процент возникновения рецидивных форм [2, 3].
Несмотря на определенные недоговоренности среди различных международных и отечественных медицинских сообществ, хирургическое лечение стрессового недержания мочи с помощью установки уретральных слингов в большинстве случаев признается в качестве наиболее эффективного и безопасного метода коррекции [4, 5]. Казалось бы, оптимальный доступ и оперативная техника в данном сегменте урогинекологии найдены; однако в последнее время накапливаются данные многоцентровых исследований, свидетельствующих о возникновении хронической тазовой боли; также выполнение традиционной кольпоррафии несет в себе определенные риски за счет вероятности возникновения послеоперационных гематом и несостоятельности собственных тканей в отдаленном периоде [6, 7].
Возвращаясь к проблеме послеоперационных осложнений, следует отметить, что данное понятие включает симптомокомплекс, значительно снижающий качество жизни и способствующий социальной дезадаптации, психоэмоциональной дестабилизации, помимо ярко выраженной или латентной клинической симптоматики [8, 9]. К таким осложнениям, как правило, относят экспозицию импланта при его визуальном определении, сморщивание импланта, хроническую тазовую боль, возникновение гематом [10]. Безусловно, развитие таких неблагоприятных проявлений не только снижает удовлетворенность качеством оказанной медицинской помощи, но и требует дополнительного воздействия, нередко при помощи повторного оперативного вмешательства с иссечением сетчатого импланта и решением вопроса о дальнейшей тактике ведения в послеоперационном периоде.
Также актуальной является и проблема развития осложнений инфекционного генеза, что, как правило, проявляется патологическими выделениями из половых путей, локальной болезненностью, уплотнением, припухлостью и отеком, покраснением и различными общеклиническими симптомами [11]. Частота возникновения таких осложнений в литературе варьирует от 1 до 68% в зависимости от вида хирургического вмешательства, типа синтетического материала, выраженности ответной реакции организма и наличия сопутствующей коморбидной патологии [12].
Попытки изучить взаимосвязь влагалищной микробиоты и риска развития инфекционно-воспалительных заболеваний после коррекции генитального пролапса привели к выводам о том, что исходно основную часть микробиома составляют лактобактерии, конкурентно ингибирующие рост остальных условно-патогенных микроорганизмов [13]. При сравнении изменений микробиома среди пациентов, у которых развились осложнения преимущественно в виде экструзии и сморщивания импланта, и пациентов с неосложненным течением послеоперационного периода было выявлено, что рост колоний вейлонеллы и актиномицета является фактором риска неблагоприятных исходов хирургического лечения [14]. При этом авторы исследования отмечают, что достоверных признаков ассоциации влагалищного дисбиоза и осложнений выявлено не было, однако нельзя не отметить тесную взаимосвязь диссоциации нормальной микробиоты влагалища у пациентов с развитием экструзии или сморщивания сетчатого протеза.
Таким образом, хирургия генитального пролапса и недержания мочи находится в постоянном движении и совершенствовании, вследствие чего изучение факторов риска и механизмов развития осложнений позволит улучшить и модернизировать имеющиеся алгоритмы ведения. При этом важными элементами рационального лечения пациентов с пролапсом тазовых органов являются не только обеспечение оптимального хирургического воздействия, но и грамотное выстраивание послеоперационного периода с целью наиболее благоприятного восстановления тканей и улучшения репаративных свойств.
Цель исследования: улучшение исходов коррекции генитального пролапса с использованием собственных тканей за счет минимизации риска осложнений путем модификации техники кольпоррафии и назначения в послеоперационном периоде спрея «Эпиген Интим» в качестве иммуностимулирующего, противовоспалительного и регенерирующего средства.
Материалы и методы
Исследование включило 60 пациенток перименопаузального периода с признаками генитального пролапса 2-й и более стадии по классификации POP-Q по переднему и заднему компартментам тазового дна.
Критерии включения: цистоцеле и/или ректоцеле 2-й и более стадии по POP-Q.
Критерии исключения: мультикомпартментное поражение тазового дна (с поражением апикального отдела); предшествующая хирургическая коррекция пролапса с использованием синтетических материалов.
Всем пациенткам проводилось стандартное обследование в рамках предоперационной подготовки: сбор анамнестических данных, клинический анализ крови, биохимический анализ крови, коагулограмма, электрокардиографическое исследование, консультация терапевта, гинекологический осмотр, двуручное влагалищно-абдоминальное обследование, ультразвуковое исследование органов малого таза и молочных желез.
Госпитализация пациентов осуществлялась за день до предполагаемого вмешательства. В условиях стационара проводили стратификацию риска тромбоэмболических осложнений и соответствующую профилактику в объеме механической компрессии вен нижних конечностей и подкожного введения профилактических доз низкомолекулярного гепарина в зависимости от индекса массы тела. Накануне вечером пациентам проводили механическую подготовку кишечника с помощью очистительной клизмы. Проводили антибиотикопрофилактику: за 1 ч до начала операции вводили внутривенно препараты цефалоспоринового ряда (преимущественно цефтриаксон в дозировке 1–2 г); при наличии аллергической реакции в анамнезе назначали амоксициллина клавуланат (1 г) или ципрофлоксацин (200 мг) [15–17]. Тактика послеоперационного периода основывалась на обеспечении ранней активизации и ускоренного восстановления.
В зависимости от методики кольпоррафии и тактики послеоперационного ведения пациенты разделены на 2 группы (рис. 1).
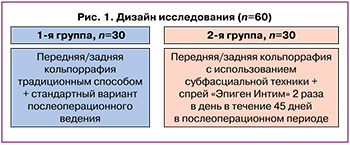
Коррекция цисто- или ректоцеле в 1-й группе осуществлялась по традиционной технике влагалищным доступом с использованием собственных тканей и расслаиванием в подслизистом слое. В качестве шовного материала использовали рассасывающиеся нити полипропиленовой конструкции. Ушивание краев слизистой выполняли с помощью наложения узловых швов, а заднюю кольпоррафию дополняли выполнением перинеоррафии с целью восстановления нормальной анатомической структуры тазового дна.
Среди пациенток 2-й группы диссекция осуществлялась субфасциально с целью отделения не только слизистой оболочки, подслизистого слоя, но и эндопельвикальной фасции. Ушивание проводили в несколько этапов: на фасцию швы накладывались изнутри-наружу, после чего сопоставлялись края слизистой и подслизистого слоя. В отношении используемого шовного материла и техники перинеоррафии разницы между группами не было.
Стандартный вариант послеоперационного ведения включал обработку наружных половых органов и послеоперационных швов с помощью водного раствора хлоргексидина биглюконата 2 р/сут в течение 10 дней, половой и физический покой 30 дней, наблюдение гинеколога по месту жительства. В модифицированной схеме среди пациентов 2-й группы использовали спрей «Эпиген Интим» в пролонгированном режиме – 2 р/сут в течение 45 дней. Спрей «Эпиген Интим» был выбран нами, учитывая наличие в его составе активированной глицирризиновой кислоты, обладающей иммуностимулирующими, регенерирующими и противовоспалительными свойствами за счет стимуляции выработки интерферонов, повышения активности Т-клеточного звена иммунитета, ингибирующего воздействия на выработку кининов и простагландинов в зоне воспаления [18, 19].
Пациентки обеих групп не различались по возрасту и индексу массы тела, а среднее значение продолжительности госпитализации составило не более 4 койко-дней; при этом во 2-й группе отмечалось незначительное уменьшение длительности госпитализации (в 1-й группе среднее значение – 3,8, во 2-й – 3,3) (табл. 1).
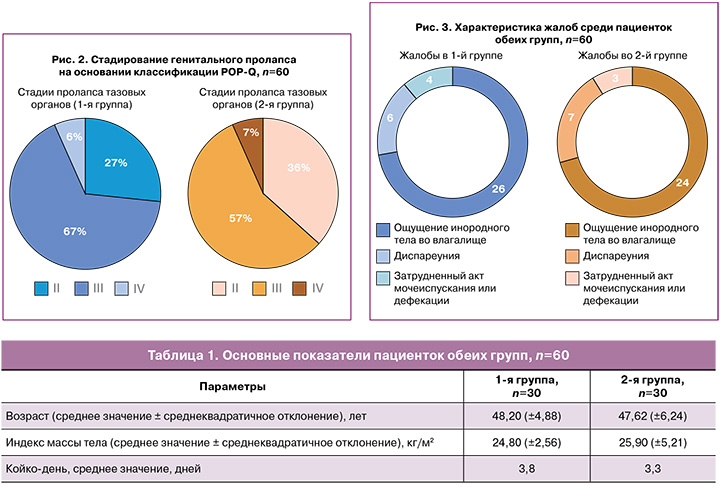
На основании классификации Pelvic Organ Prolapse Quantification System (POP-Q) в структуре генитального пролапса у 20/30 (67%) пациенток 1-й группы и 17/30 (57%) пациенток 2-й группы определялись признаки опущения передней и/или задней стенок влагалища 2-й стадии (рис. 2). Генитальный пролапс 3-й стадии обнаруживался в 27% (8/30) случаев в 1-й группе и в 36% (11/30) – во 2-й группе.
Основными жалобами среди пациенток обеих групп явились: ощущение инородного тела во влагалище или промежности (26/30 (87%) — в 1-й группе, 24/30 (80%) – во 2-й группе), хроническая тазовая боль в виде диспареунии (6/30 (20%) и 7/30 (23,3%) соответственно), а также констипация и/или дизурические явления обструктивного типа (4/30 (13,3%) и 3/30 (10%) соответственно) (рис. 3).
С целью обнаружения взаимосвязи между изменениями микробиома влагалища и риском возникновения осложнений нами был проведен сравнительный анализ исходов послеоперационного периода и данных микроскопического исследования влагалищного отделяемого и биоценоза влагалища методом полимеразной цепной реакции (ПЦР) у пациенток как с осложненным, так и неосложненным течением послеоперационного периода.
Статистический анализ
Результаты числовых данных представлены с применением пакета прикладных программ STATISTICA 10 (StatSoft, 2012), Office Excel (Microsoft, 2019). Статистически значимыми считались изменения показателей с вероятностью ошибки менее 0,05.
Результаты и обсуждение
На основании проведенного хирургического лечения в объеме передней и/или задней кольпоррафии проводили оценку динамики жалоб и периоперационных показателей на момент выписки из стационара и через 45 дней после проведенного лечения (табл. 2, 3).
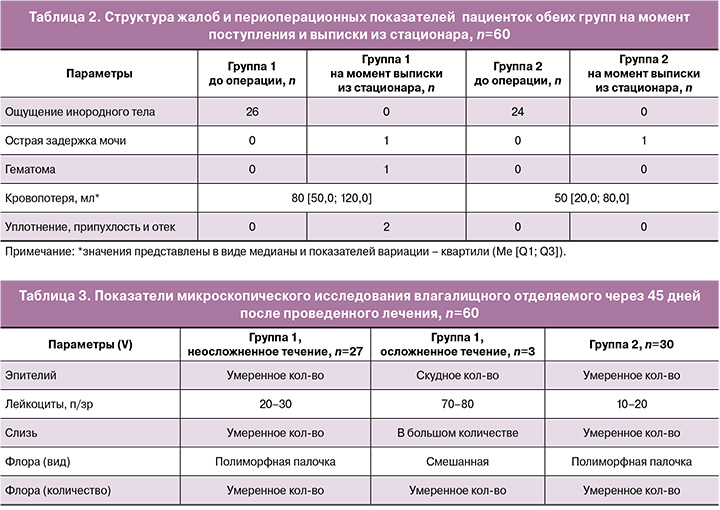
Согласно анализу клинических проявлений по выписке из стационара следует отметить, что в 2/30 (6,7%) случаях среди пациентов 1-й группы отмечались признаки недержания мочи смешанного характера легкой степени выраженности, которые не повлияли на удовлетворенность пациентами качеством жизни. Однако эти пациенты были направлены под амбулаторное наблюдение уролога. Также в единичных случаях как в 1-й, так и во 2-й группе отмечались признаки острой задержки мочи на 1–2-е сутки послеоперационного периода, что потребовало катетеризации мочевого пузыря и стимуляции диуреза с полностью обратимым течением.
В 3/30 (10%) случаях среди пациенток 1-й группы отмечалось наличие осложнений в виде гематомы, уплотнения и припухлости в области послеоперационных швов, что также сопровождалось патологическими выделениями из половых путей. При этом пациенткам была назначена антибактериальная терапия цефалоспоринами в пролонгированном режиме на 5 дней до момента купирования указанных жалоб. Также следует отметить, что величина кровопотери среди пациенток 1-й группы составила 80 мл [50,0; 120,0], а во 2-й группе – 50 [20,0; 80,0] мл.
В результате оценки жалоб и клинической картины через 45 дней после проведенного хирургического лечения отмечалось, что у 3 (10%) пациенток 1-й группы имелись жалобы на тазовую боль, при этом во 2-й группе – лишь в 1 случае (3,3%). В 2 (6,7%) случаях среди пациенток 1-й группы наблюдались симптомы в виде ощущения инородного тела и в 1 (3,3%) случае – в виде затрудненного акта дефекации, мочеиспускания.
При проведении микроскопического исследования среди пациенток обеих групп было выявлено, что наличие осложнений сопряжено с увеличением как количества лейкоцитов, так и соотношения лейкоцитов к эпителиальным клеткам при сравнении с неосложненным течением послеоперационного периода в 1-й группе и пациентами из 2-й группы (табл. 3).
При исследовании данных биоценоза влагалища методом ПЦР через 45 дней после проведенного лечения было выявлено, что у пациенток с осложненными формами из 1-й группы (n=3) имелись признаки неспецифического вагинита, проявляющегося снижением количества нормофлоры в виде лактобактерий, повышением концентрации как факультативно-анаэробных, так и облигатно-анаэробных микроорганизмов (табл. 4).
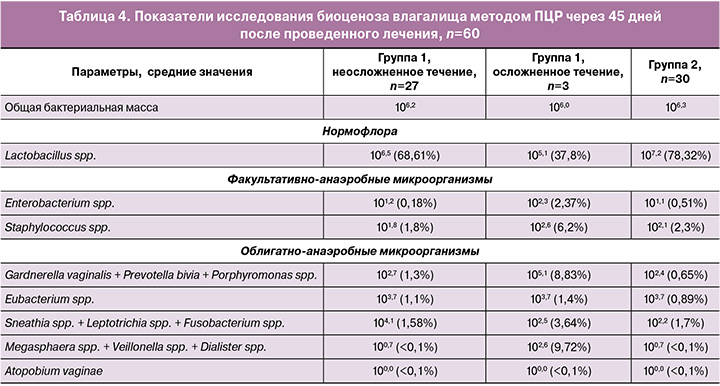
При сравнительном анализе результатов ПЦР среди пациенток обеих групп отмечается, что соотношение нормофлоры к остальным условно-патогенным микроорганизмам более благоприятное у пациенток 2-й группы, которым проводилась пролонгированная обработка послеоперационной зоны с помощью спрея «Эпиген Интим» в течение 45 дней.
Также нельзя не отметить повышение концентрации облигатно-анаэробной флоры при осложненном течении послеоперационного периода.
В последнее время накапливаются данные о более предпочтительном использовании субфасциальной техники диссекции, что характеризуется меньшей кровопотерей и более эффективной коррекцией цисто- и ректоцеле [20].
В нашем исследовании мы провели сравнительный анализ результатов хирургического лечения опущения передней/задней стенок влагалища при помощи традиционного и модифицированного способа периоперационного ведения. Модификация тактики заключалась в использовании субфасциальной техники выполнения кольпоррафии и пролонгированном воздействии иммуностимулирующего, противовоспалительного, регенерирующего спрея «Эпиген Интим» в течение 45 дней послеоперационного периода среди пациенток 2-й группы с целью улучшения репаративных свойств тканей и благоприятного воздействия на микробиом влагалища.
Нами отмечена определенная взаимосвязь между состоянием влагалищного микробиома и репарацией тканей после традиционного способа кольпоррафии, что находится в прямой ассоциации с риском развития осложнений. При этом содержание Lactobacillus spp. в 1-й группе с неосложненным течением составило 106,5 (68,61%), во 2-й группе – 107,2 (78,32%), что также свидетельствует о более благоприятном воздействии модифицированной схемы послеоперационной тактики с использованием спрея «Эпиген Интим» в пролонгированном режиме.
Заключение
Хирургическая коррекция генитального пролапса требует рационализированного подхода, что определяет не только обеспечение оптимальной техники кольпоррафии за счет субфасциальной диссекции тканей, но и грамотно выстроенную послеоперационную тактику.
Использование специализированных препаратов, например спрея «Эпиген Интим» с противовоспалительным, иммуностимулирующим и регенерирующим действием, в пролонгированном режиме после операции позволяет адаптировать состояние влагалищного микробиома и ускорить регенерацию тканей, что сопряжено со снижением риска послеоперационных осложнений.
Дальнейшие исследования по анализу микрофлоры влагалища в послеоперационном периоде могут позволить дифференцировать профиль микробиома у здоровых, бессимптомных пациентов и лиц с предрасположенностью к осложнениям.



