Бактерии, продуцирующие биопленки, являются серьезной проблемой во всех областях медицины во всем мире. Образование устойчивых бактериальных, грибковых или смешанных ассоциаций и окружающего их органического матрикса (биопленок) представляет собой универсальный механизм формирования резистентности микроорганизмов к различным антимикробным препаратам. Иными словами, биопленки представляют собой структурированный консорциум бактериальных и/или грибковых клеток, окруженных полимерным матриксом собственного производства [1]. Биопленки на слизистой влагалища блокируют воспалительный ответ женского организма, снижают активность иммуноцитов, позволяя бактериям достигать высоких концентраций. Нарушение экосистемы влагалища у женщин репродуктивного возраста является одной из наиболее актуальных проблем в акушерско-гинекологической практике [2].
Часто заболевание не ограничивается только нижними отделами половых путей. Восходящая инфекция приводит к развитию воспалительных заболеваний шейки матки (цервицит), а также полости матки (эндометрит) и ее придатков (сальпингоофорит). У пациенток с вагинальными инфекциями значительно повышена частота инфекционных осложнений после выполнения гинекологических манипуляций (аборт, гистероскопия, лапароскопия). Неудачные попытки ЭКО наблюдаются чаще у женщин с сопутствующим бактериальным вагинозом [3].
Инфекции, вызванные микроорганизмами, способными образовывать пленки, плохо поддаются лечению антимикробными препаратами и часто рецидивируют, несмотря на защитные механизмы макроорганизма. Состав биопленок может быть монобактериальным и смешанным. Широкий спектр молекулярных механизмов способствует высокой степени сопротивляемости, характерной для биопленочных сообществ. Эти механизмы включают, среди прочего, взаимодействие противомикробных препаратов с компонентами матрикса биопленок, снижение скорости роста и различные действия специфических генетических детерминант устойчивости и толерантности к препаратам. По отдельности каждый из этих механизмов лишь частично объясняет повышенную резистентность к противомикробным препаратам, наблюдаемую в биопленках. Однако, действуя согласованно, эти защитные механизмы помогают обеспечить выживание микробных клеток в составе биопленки даже перед лицом самых агрессивных схем антимикробного лечения [4].
Поэтому проводится поиск альтернативных препаратов, которые могут использоваться в качестве дополнительных средств в комплексной терапии биопленочных инфекций. Одним из таких средств может рассматриваться экстракт корня солодки (Glycyrrhiza glabra). Применение корня солодки в качестве лечебного средства известно с давних времен. Например, в Кодексе Хаммурапи (2100 г. до н.э.) он упоминается, а китайская медицина в течение тысячи лет признает его средством улучшения качества жизни.
В корневище и корнях солодки содержатся тритерпеноидные сапонины (4–20%). Важным сапонином корня солодки является водорастворимая молекула – глицирризин, соли глицирризиновой кислоты (глицирризиновая кислота (ГК) также известна как глицирретиновая, гликозидная кислота, 18-β-глицирретиновая кислота и гликозид глицирретиновой кислоты) [5].
ГК, выделенная из корней солодки, является основным биоактивным ингредиентом, обладающим широким спектром биологической активности, включая противовоспалительное, противовирусное, противоязвенное, противоопухолевое и гепатопротекторное действие. Активированная ГК является действующим веществом препарата спрей «Эпиген Интим» 0,1%.
Целью исследования является оценка in vitro действия препарата спрей «Эпиген Интим» 0,1% на бактериальные пленки, сформированные вагинальными микроорганизмами.
Материалы и методы
В исследование включены 72 клинических изолята чистых культур микроорганизмов, выделенных из вагинального биотопа: G. vaginalis (3 изолята), E. faecalis (9 изолятов), E. coli (18 изолятов), K. pneumoniae (15 изолятов), K. aerogenes (3 изолята), L. crispatus (3 изолята), S. pyogenes (3 изолята), A. baumannii (3 изолята), S. aureus (3 изолята), C. albicans (3 изолята), E. faecium (3 изолята), S. agalactiae (3 изолята), L. acidophilus (3 изолята).
Для культивирования, хранения и дальнейшего исследования использовали плотные и жидкие питательные среды: кровяной агар с 5% дефибринированной крови (КА), среду Сабуро (агар и бульон), триптиказо-соевый агар (ТСА), триптиказо-соевый бульон (ТСБ), триптиказо-соевый бульон с 10% глицерина (ТСБ-Г), сердечно-мозговой бульон (СМБ), агар Мюллера–Хинтона (МХА) простой и с добавлением 5% дефибринированной крови. Идентификация микроорганизмов проводилась серологическими методами (реакция латекс-агглютинации) и методом MALDI-TOF спектрометрии на масс-спектрометре Bruker Microflex (Германия).
Способность к образованию биопленок была оценена по модифицированному протоколу Christensen et al. [6].
В зависимости от отношения оптической плотности (ОП) контроля к ОП образца изоляты микроорганизмов были разделены на 4 категории:
1) изоляты, не образующие биопленку, – ОП образца на уровне ОП контроля;
2) изоляты, слабо образующие биопленку (1+), – ОП образца превышала ОП контроля не более чем в 2 раза;
3) изоляты, умеренно образующие биопленку (2+), – ОП образца превышала ОП контроля в 2–4 раза;
4) изоляты, образующие выраженную биопленку (3+), – ОП образца превышала ОП контроля более чем в 4 раза.
В исследовании использовали спрей «Эпиген Интим» 0,1% (производство по заказу «Хемигруп Франс С.А.», Франция («Б. Браун Медикал С.А.», Хаен, Испания) для ООО «Инвар», Россия). Действующее вещество препарата «Эпиген Интим» – активированная ГК (0,1 г на 100 мл). Вспомогательные вещества – яблочная кислота, фумаровая кислота, аскорбиновая кислота, фолиевая кислота, пропиленгликоль, твин-80 (полисорбат-80), вода очищенная.
Результаты
Исследование основано на количественном определении биопленок в полистироловых плоскодонных планшетах по модифицированному методу Christensen et al. (1985) [6].
Лунки полистиролового планшета (24-луночного) асептически заполняли 450 мкл питательной среды (ТСБ) с добавлением 1% глюкозы. В каждую лунку вносили по 50 мкл суспензии микроорганизмов, получая концентрацию микроорганизмов 106 КОЕ/мл. Лунки отрицательного контроля (К-) содержали 500 мкл ТСБ с 1% глюкозы и не содержали микроорганизмов. Лунки с биопленками и отрицательным контролем заполняли ТСБ (450 мкл) и вносили 50 мкл препарата. Конечная концентрация препарата – 1:10. Инкубировали 24 ч при 37°С. После второй инкубации лунки опорожняли, трехкратно промывали фосфатно-солевым буфером комнатной температуры (PSB; pH 7,2) и окрашивали 2% генцианвиолетом. Краситель элюировали 96% этанолом и измеряли ОП раствора в каждой лунке при 570 нм с помощью спектрофотометра. Пороговое значение определяли как 3 стандартных отклонения выше средней ОП отрицательного контроля. Окончательное значение ОП выражалось как среднее значение ОП штамма, уменьшенное на величину порогового значения (рассчитывается для каждого микроорганизма отдельно). Если получено отрицательное значение, оно представляется как ноль, любое положительное значение указывает на образование биопленки. Одна лунка из засеянных предназначалась для контроля жизнеспособности и чистоты культуры путем высева на плотную питательную среду и дальнейшей инкубации в течение 24 ч при 37°С.
Тестируемые изоляты L. crispatus, L. acidophilus, C. albicans, S. agalactiae, S. pyogenes (34 изолята из 72) биопленки не образовывали. Таким образом, в исследование по действию препарата спрей «Эпиген Интим» 0,1% на бактериальные пленки были включены 38 изолятов биопленкообразующих микроорганизмов, что составило 53%.
Результаты измерений ОП и их интерпретация по исследованию воздействия препарата спрей «Эпиген Интим» 0,1% на бактериальные пленки, сформированные разными микроорганизмами, представлены в таблице.
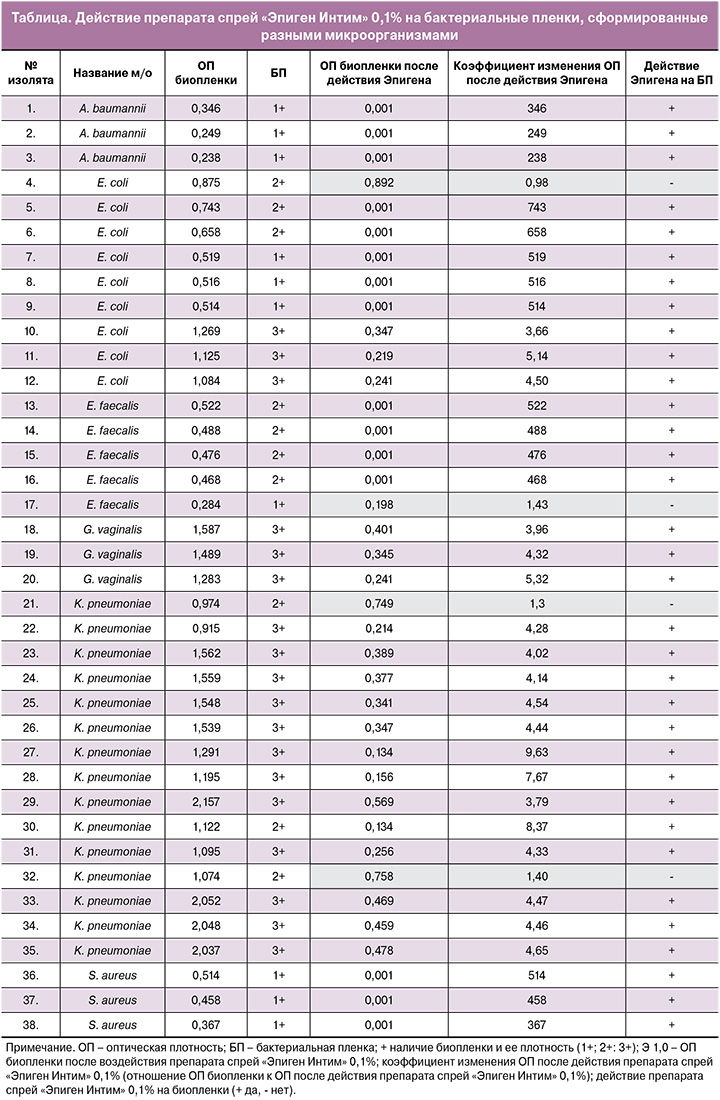
Как видно из данных, приведенных в таблице, из 38 клинических изолятов микроорганизмов высокая способность к образованию плотной биопленки (3+) была у 18. Это были все G. vaginalis (3), K. pneumoniae (12), а также 3 изолята E. coli. Их ОП была в пределах 1,125–2,157, т.е. превышала ОП контроля более чем в 4 раза и была выше 0,8 оптических единиц (о.е.). Среднее биопленкообразование (2+) было у 10 изолятов бактерий (3 изолята E. coli, 4 изолята E. faecalis и 3 изолята K. pneumoniae), т.к. ОП образца превышала ОП контроля в 2–4 раза; их ОП была в диапазоне от 0,4 до 0,8 о.е. Ряд изолятов микроорганизмов, их 10, такие как S. aureus, A. baumannii, E. coli, E. faecalis, обладали слабой способностью образовывать биопленки (1+). Их ОП была выше ОП контроля не более чем в 2 раза и составляла 0,2–0,4 о.е.
Из 38 изолятов микроорганизмов, образующих биопленки, препарат спрей «Эпиген Интим» 0,1% оказал разрушающее действие на 34, что составило 89,48%. Здесь следует подчеркнуть, что снижение ОП биопленки более чем в 3 раза (коэффициент изменения ОП после воздействия препаратом спрей «Эпиген Интим» 0,1% был более 3) указывает на разрушающее биопленки действие препарата. Для 34 изолятов коэффициент изменения ОП составил от 3,66 до 743. На биопленки, сформированные четырьмя изолятами микроорганизмов (2 изолята K. pneumoniae, E. coli и E. faecalis), препарат спрей «Эпиген Интим» 0,1% не оказал разрушающего действия.
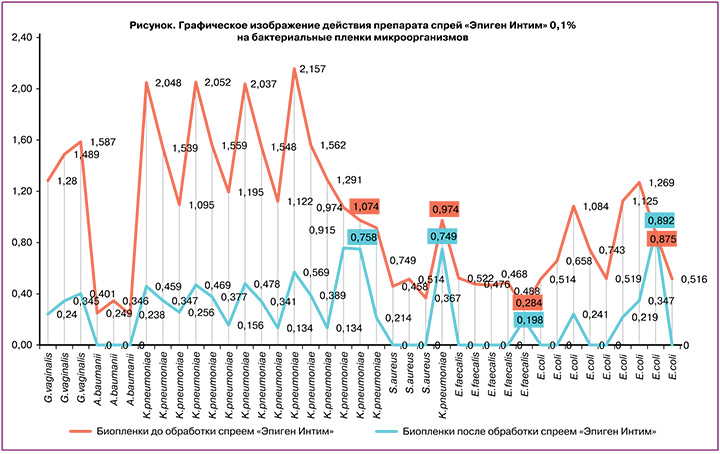
На рисунке представлена диаграмма, иллюстрирующая данные таблицы. Красные линии показывают ОП биопленочной культуры: чем выше ОП, тем более плотная биопленка образована. Синим цветом показана ОП культуры в биопленке после действия препарата спрей «Эпиген Интим» 0,1%. Чем больше расхождение красной и синей линий, тем более выраженное действие оказывает препарат спрей «Эпиген Интим» 0,1% на биопленки.
Обсуждение
В настоящее время идет поиск новых препаратов с противобиопленочной активностью. Представлен обзор некоторых из последних отчетов о природных ингибиторах биопленок. Эти метаболиты могут использоваться в качестве мощных терапевтических средств для повышения эффективности антибиотиков против заболеваний, связанных с биопленками. Значительный антибиопленочный потенциал был обнаружен у фенольных соединений, полиацетиленов, терпеноидов, алкалоидов, лектинов и полипептидов. Конденсированные танины, особенно среди фенольных соединений, продемонстрировали антибиопленочную активность [7]. Корень солодки содержит 20 тритерпеноидов и почти 300 флавоноидов. Наиболее важным веществом в этом отношении является ГК. Исследования in vitro и in vivo показали, что ГК ингибирует репликацию ДНК или РНК некоторых вирусов, поражающих людей или животных [8, 9]. Предыдущие исследования показали, что 80% бактериальных инфекций и лекарственной устойчивости связаны с образованием бактериальных биопленок [10]. Как показало исследование, ГК эффективно ингибирует образование биопленок S. аureus, в том числе MRSA, что способствует снижению риска лекарственной устойчивости [11]. Механизмы ГК против MRSA в основном включают подавление генов вирулентности, ингибирование продукции α-гемолизина и образования биопленок [12–14]. Гидрогели производных ГК первоначально прилипают к поверхности и проникают в бактерии, затем влияют на биосинтез и метаболизм аргинина, что в конечном итоге приводит к гибели бактерий [15, 16]. Однако детали механизмов требуют дальнейшего изучения.
Образованные биопленки монокультурой Enterococcus faecalis с кинетикой роста через 24 и 48 ч при обработке экстрактом солодки продемонстрировали снижение КОЕ/мл энтерококков, что было проверено методом подсчета жизнеспособных микроорганизмов, и скудность архитектуры биопленок по сравнению с контрольной группой [17]. В нашем исследовании эффективность разрушающего действия препарата «Эпиген Интим» на биопленки оценивалась и регистрировалась по изменению ОП (в 3 и более раз). В биопленках, сформированных четырьмя из пяти изолятов E. faecalis, ОП уменьшилась более чем в 400 раз.
Образование биопленки также является важной физиологической особенностью P. aeruginosa, которая позволяет ей выживать и сопротивляться даже в присутствии противомикробных агентов. Экстракты трав и ГК эффективны в воздействии на физиологические и биохимические параметры бактерий, которые включают проницаемость клеточных мембран и образование биопленок. Рост P. aeruginosa значительно подавлялся экстрактом корня солодки и его чистым соединением, ГК [18]. Чтобы выяснить антибиопленочную активность, был проведен анализ образования биопленки на микротитровальном планшете, и было обнаружено, что тестируемые образцы (ципрофлоксацин, экстракт корня солодки и ГК) ингибировали образование биопленки в 65,06–83,35% случаев в диапазоне концентраций 50–200 мкг/мл. Ингибирующий эффект постепенно возрастал с увеличением концентрации препарата [18]. ГК повреждала полисахариды структуры внеклеточного матрикса и белки системы кворум-сенсинга, препятствуя способности бактерий определять плотность популяции, а также продуцировать факторы вирулентности и подвижности микроорганизмов; она вызывает сапонификацию мембран бактериальных клеток, что нарушает стабильность биопленки и снижает экспрессию генов, ответственных за формирование биопленки [19].
Образование биопленки микроорганизмами позволяет им выживать и избегать агрессивного воздействия окружающей среды, включая воздействие антимикробных химиопрепаратов, в течение длительного времени. Следовательно, это может привести к сохранению тяжести заболевания, хронизации и рецидивированию инфекционного процесса. Персистенция биопленки, состоящей из ассоциированных с бактериальным вагинозом микроорганизмов, является одним из самых вероятных путей возникновения рецидивов и важным диагностическим маркером заболевания [20]. Несмотря на применение антибиотиков, поиск эффективных средств все еще продолжается. Сообщается, что среди альтернатив антибиотикам в качестве применимой стратегии можно использовать растительные экстракты и натуральные растительные продукты в качестве добавок, иммуностимуляторов для усиления неспецифического защитного механизма хозяина и ингибирования биопленкообразования.
Мы исследовали влияние активированной ГК на биопленки, созревающие в течение 48 ч, на поверхности полистиролового планшета, чтобы имитировать образование биопленок на поверхностях органов макроорганизма, в частности на слизистой влагалища. Препарат подействовал на 34 из 38 изолятов микроорганизмов, образующих биопленки. Эффективность действия активированной ГК в составе препарата спрей «Эпиген Интим» 0,1% мы оценили в 89,47%. Исключение составили 2 изолята K. pneumoniae и изоляты E. coli и E. faecalis. Действие активированной ГК против микробной биопленки является штаммоспецифичным. Тестируемые нами штаммы дрожжеподобных грибов C. albicans биопленки не образовывали. Cуществует лишь несколько сообщений о влиянии соединений корня солодки на C. albicans. Эти исследования ограничивались влиянием экстракта корня солодки на рост C. albicans. Было обнаружено, что экстракт Glycyrrhiza glabra L. глабридин ингибирует рост C. albicans. ГК не проявляла никакого эффекта в концентрациях до 200 мкг/мл [21].
В ранее проведенном нами исследовании был показан эффективный опыт комбинированной терапии бактериального вагиноза. В данном исследовании мы применяли препарат спрей «Эпиген Интим» 0,1%, содержащий активированную ГК. Исследование было двойным слепым плацебо-контролируемым. Рассмотрение динамики изменения использованных в работе показателей позволяет констатировать благоприятное влияние спрея «Эпиген Интим» 0,1% в комплексном лечении бактериального вагиноза: в более короткий срок исчезают неприятный запах влагалищных выделений, жалобы пациенток на дискомфорт в области влагалища, быстрее снижаются значения рН влагалищных выделений и исчезают «ключевые» клетки, которые выявляются при микроскопическом исследовании вагинальных выделений. Микроскопическое и культуральное исследования выявляют значительное увеличение числа лактобацилл у женщин, которым проведено комбинированное лечение с использованием препарата спрей «Эпиген Интим» 0,1% по сравнению с теми пациентками, которым заменен этот препарат на плацебо, и с теми, которые получали только антибиотик [22].
Поскольку одним из основных биопленкообразующих микроорганизмов, входящих в состав вагинального биотопа, является Gardnerella vaginalis, нами в настоящем исследовании было показано, что спрей «Эпиген Интим» разрушает биопленки, образованные этими микроорганизмами. Это необходимо учитывать при назначении препаратов для лечения бактериального вагиноза. Кроме того, нами показано действие препарата спрей «Эпиген Интим» 0,1% на биопленки, сформированные и другими микроорганизмами, возможными возбудителями аэробного (неспецифического) вагинита, такими как K. pneumoniae, E. coli, E. faecalis. Этот факт нужно учитывать при выборе препаратов для комплексной терапии аэробного вагинита. В многоцентровом исследовании с участием пациенток с аэробным вагинитом, кандидозным вульвовагинитом и бактериальным вагинозом было показано, что при включении в комплексное лечение препарата на основе активированной ГК 0,1% в форме спрея для местного и наружного применения было отмечено исчезновение жалоб на выделения из половых путей [23].
В данном исследовании мы не обнаружили биопленкообразования лактобациллами и дрожжеподобными грибами. Это побуждает нас провести дальнейшие исследования.
Таким образом, препарат спрей «Эпиген Интим» 0,1% показал высокую эффективность in vitro в отношении исследованных нами микроорганизмов.
Заключение
Препарат спрей «Эпиген Интим» 0,1%, содержащий в своем составе активированную ГК, оказывает разрушающее действие на биопленки, образованные вагинальными микроорганизмами, такими как G. vaginalis, K. pneumoniae, E. coli, E. faecium, с эффективностью in vitro 89,48%. Следует подчеркнуть, что снижение ОП биопленки более чем в 3 раза указывает на разрушающее биопленки действие препарата. Для 34 изолятов микроорганизмов коэффициент изменения ОП после воздействия препаратом спрей «Эпиген Интим» 0,1% составил от 3,66 до 743.



