Несмотря на достижения фундаментальной науки, концептуальное переосмысление в последние годы принципов асептики, антисептики и динамического развития фармакологии, одной из проблем, неизменно сохраняющих свою актуальность для акушерства, гинекологии и перинатологии, являются воспалительные заболевания вульвы и влагалища [1, 2]. С 2012 г. после обнародования результатов Национального проекта Института здоровья США «Микробиом человека» мировое сообщество было вынуждено признать, что безальтернативной перспективой оздоровления человеческой популяции является профилактика инфекционных заболеваний, в основу которой, наряду с постулатами здорового образа жизни, должно быть положено поддержание нормоценоза естественных биосистем организма [1–3]. Кандидозное поражение слизистой оболочки вульвы и влагалища – вульвовагинальный кандидоз (ВВК) – самая распространенная форма урогенитального кандидоза. Частота регистрации ВВК за последние 10 лет почти удвоилась и в настоящее время составляет 30–45% в структуре инфекционных поражений вульвы и влагалища. По данным исследователей, 70–75% женщин в течение жизни имеют хотя бы один эпизод ВВК, при этом в 5–10% случаев заболевание становится рецидивирующим. ВВК редко встречается у девочек до наступления менархе, однако к 25 годам уже около 50% женщин, а к началу периода менопаузы около 75% женщин имеют хотя бы один диагностированный врачом эпизод заболевания. Также известно, что ВВК почти не встречается в постменапаузе, за исключением женщин, получающих заместительную гормональную терапию [2, 4, 5]. Наряду с клинически выраженным заболеванием существует бессимптомная колонизация влагалища дрожжеподобными грибами. Следует подчеркнуть, что около 20% здоровых женщин являются носителями дрожжеподобных грибов во влагалище, что не требует лечения. Частота ВВК у больных с эндокринопатиями составляет 30%, у беременных женщин – 30–35%, у ВИЧ-инфицированных – до 40% случаев [2, 6, 7].
В настоящее время большинство специалистов придерживается мнения, что многократное назначение имидазолов, в частности флуконазола в дозе 150 мг внутрь еженедельно в течение не менее 6 месяцев, позволяет предотвратить развитие рецидивов ВВК. Однако частое применение противогрибковых препаратов ведет к развитию резистентности штаммов Candida к терапии [6–9]. Тем не менее, результаты доклинических и ряда сравнительных клинических исследований свидетельствуют о том, что отдельные штаммы лактобактерий, в том числе L. casei rhamnosus Doderleini, способны подавлять адгезию Candida albicans к вагинальному эпителию и/или пролиферацию Candida albicans [10–12], а также предотвращать рецидивы, и могут применяться в качестве профилактики рецидивов ВВК [10–13].
Цель проведенного исследования – оценить эффективность и безопасность применения препарата, содержащего культуру L. casei rhamnosus Doderleini (лактожиналь, капсулы вагинальные), для профилактики рецидивов вульвовагинального кандидоза после антимикотического лечения препаратом сертаконазол (залаин).
Материал и методы исследования
В рамках международного (Россия, Украина) многоцентрового, открытого, сравнительного исследования по оценке эффективности и безопасности препарата лактожиналь, капсулы вагинальные, для профилактики обострений вагинального кандидоза планировалось включить 160 пациенток с рецидивирующим процессом, после курса местной терапии антимикотиком сертаконазолом (залаин). Расчет объема выборки осуществлялся исходя из того, что пропорция пациенток без рецидива в группе сравнения приблизительно составит 30%. Предполагаемое различие между группами – 20%. Расчет объема выборки проводился с учетом необходимой мощности 80% (β-ошибка 20%) и допустимой α-ошибки 5%, а также возможным 10% выбывании пациенток в группах.
Всего в анализ эффективности и безопасности были включены данные 154 пациенток (6 женщин из 160 преждевременно выбыли из исследования в связи с потерей контакта). Возраст включенных пациенток составил 20–45 лет (31,3±6,9), средний индекс массы тела – 21,9 кг/м2 (19,8–23,8). У всех 154 женщин на момент включения в исследование имел место диагноз – рецидивирующий вульвовагинальный кандидоз, обусловленный Саndida albicans, по данным анамнеза (медиана количества обострений ВВК за прошедший календарный год, включая текущее обострение 5 (4,0–5,0)) и подтвержденный данными микроскопического и микробиологического исследования. Согласно дизайну исследования пациентки были разделены на две группы в зависимости от способа лечения ВВК: основную группу составили 74 женщины, принимавших после терапии сертаконазолом (залаин, суппозиторий 300 мг однократно и 2% крем 2 раза в сутки в течение 8 дней) препарат L. casei rhamnosus Doderleini (лактожиналь) в течение 21 дня по 1 капсуле в сутки, группу сравнения – 80 человек только с монотерапией антимикотиком (залаин, суппозиторий 300 мг однократно и 2% крем 2 раза в сутки в течение 8 дней).
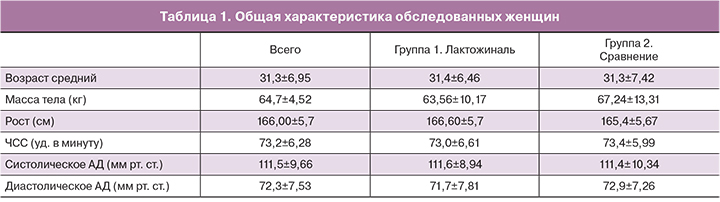
По антропометрическим показателям, АД и ЧСС группы пациентов были статистически однородны и сопоставимы (табл. 1).
При проведении исследования соблюдались следующие критерии включения/исключения пациентов.
Критерии включения в исследование:
- Наличие хронического рецидивирующего вульвовагинального кандидоза (РВВК) по данным анамнеза (начало заболевания, частота обострений, результаты лабораторного исследования, лечение), а именно, наличие не менее 4 эпизодов обострения за календарный год, включая текущее обострение; лабораторное подтверждение хотя бы одного эпизода ВВК в течение последних 2 лет;
- Обострение ВВК на момент включения в исследование (не менее двух локальных признаков и симптомов: зуд, жжение, отек слизистой, обильные выделения «творожистого характера»);
- Данные лабораторного исследования (выявление бластоспор и псевдомицелия дрожжеподобных грибов рода Candida при микроскопическом исследовании клинических материалов из влагалища, окрашенных по Граму);
- Возраст от 18 лет до 45 лет;
- Использование надежных методов контрацепции, исключая резиновые и латексные изделия и спермициды, в течение всего периода исследования;
- Подписанный информационный листок пациента с формой письменного информированного согласия.
Критерии исключения:
- Инфекции, передаваемые половым путем (ИППП), по данным лабораторного исследования методом полимеразной цепной реакции (ПЦР) менее чем за месяц или в момент включения в исследование;
- Заболевания шейки матки (дисплазия эпителия или карцинома in situ, интраэпителиальная неоплазия и пр.);
- Отсутствие лабораторного подтверждения кандидоза (результат мазка по Граму на первом визите);
- Нарушения менструального цикла по типу менометроррагии; отказ от контрацепции, беременность, клинически значимые иммунодефицитные состояния;
- Применение других препаратов из группы пре- и/или пробиотиков (препараты, закисляющие влагалищную среду и/или содержащие другие виды лактобацилл);
- Непереносимость исследуемого препарата и/или одного из его компонентов; сертаконазола и/или одного из их компонентов.
Для постановки диагноза и оценки эффективности лечения всем пациенткам был проведен следующий объем обследования:
- Клиническое: жалобы, анамнез, общий и гинекологический осмотр;
- Лабораторное: микроскопия мазка на степень чистоты влагалищного содержимого, окрашенного по Грамму, бактериологическое, молекулярно-генетическое (ПЦР), оценка по критериям Амселя, включая рН-метрию влагалищного секрета.
Комплексное обследование проводилось дважды: до начала лечения и после завершения курса терапии; микроскопия влагалищного мазка, оценка критериев Амселя, включая рН-метрию влагалищного секрета – на каждом приеме.
У всех пациенток на момент включения в исследование клинически и лабораторно было подтверждено обострение вульвовагинального кандидоза. Длительность обострения до момента включения в исследование у всех 154 пациенток составила 23,1±13,06 дня (у пациенток группы лактожиналь составляла 23,9±14,58 дня, у пациенток группы сравнения 22,3±11,50 дня). Данные осмотра свидетельствовали о текущем ВВК по состоянию слизистых, характеру выделений, значениям рН.
Исследование состояло из трех этапов. Первый этап – терапия противогрибковыми препаратами: всем пациенткам с рецидивом вульвовагинального кандидоза проводилась терапия препаратом сертаконазола – залаин, суппозиторий вагинальный 300 мг вагинально однократно на ночь перед сном в сочетании с ежедневным использованием препарата залаин, крем для наружного применения 2% для обработки кожи в области вульвы 2 раза в день в течение 8 дней. Второй этап начинался сразу после окончания курса противогрибковой терапии. Во время второго этапа предполагался прием исследуемого препарата лактожиналь по одной вагинальной капсуле ежедневно в течение 21 дня. Во время этого этапа пациентки группы сравнения не получали какую-либо терапию и находились под наблюдением. Третий этап – наблюдение в течение 5 месяцев с момента окончания терапии препаратом лактожиналь.
Критериями эффективности терапии служили: время до следующего рецидива ВВК (дни), а также частота клинических и лабораторно подтвержденных обострений кандидоза, количество клинических обострений, не подтвержденных лабораторным исследованием; общее количество обострений ВВК в течение всего исследования.
Оценка безопасности включала сбор и последующий анализ частоты и тяжести всех нежелательных явлений со стороны пациентки, в том числе частота и тяжесть нежелательных явлений, связанных с введением препарата.
Количественные данные были суммированы с использованием средней, стандартного отклонения, медианы, минимальных и максимальных величин. Качественные данные суммированы по частоте и процентам. Все статистические тесты являются двусторонними при уровне значимости р<0,05.
Демографические и другие исходные характеристики, собранные на скрининге, были представлены описательной статистикой по популяциям и группам терапии. Для обработки результатов исследования были использованы стандартные методы дескриптивной статистики, представленные как средние величины и стандартное отклонение (для нормально распределенных величин) или медиана и процентили (для распределений, отличающихся от нормального). Для анализа времени до рецидива были построены кривые по методу Каплана–Меира. Тестирование первичной гипотезы проведено путем проведения лог-ранк анализа. При сравнении данных в группах был применен двухвыборочный тест Стьюдента для нормально распределенных величин и тест Манна–Уитни при отклонении от нормального распределения. Сопоставление частоты событий проведено с помощью тестов χ2 и точного теста Фишера. Частота событий описана в виде абсолютного и относительного рисков с приведением 95% доверительных интервалов. Нулевая гипотеза (отсутствие различий во времени до наступления рецидива) отвергнута при уровне значимости менее 0,05. Для сопоставления других величин также был принят уровень значимости 0,05.
Результаты исследования
Всего в анализ эффективности и безопасности были включены данные 154 пациенток (74 пациентки основной группы и 80 пациенток группы сравнения).
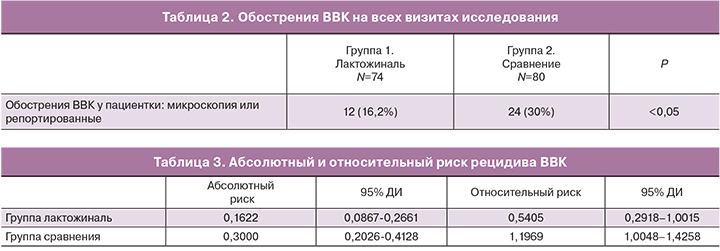
Клинические проявления рецидива ВВК, как подтвержденные лабораторно, так и неподтвержденные, являются важным критерием эффективности терапии и улучшения качества жизни пациенток. При наличии рецидивирующего ВВК именно клинические симптомы кандидоза являются маркером обострения, снижают качество жизни пациенток даже без лабораторного подтверждения, а эффективность лечения оценивается с позиций удлинений времени до рецидива процесса. В результате проведенного исследования рецидив вульвовагинального кандидоза был диагностирован у 12 пациенток (16,2%) группы лактожиналь и 24 (30,0%) пациенток группы сравнения. Проведенный статистический анализ данных показал эффективность препарата лактожиналь в профилактике рецидива вульвовагинального кандидоза после проведенного курса противогрибковой терапии, различия в группах статистически достоверны (p<0,05). Анализ данных зафиксированных обострений ВВК представлен в табл. 2.
В ходе плановых визитов по протоколу исследования у 3 пациенток группы лактожиналь и 4 пациенток группы сравнения имели место клинические проявления рецидива вульвовагинального кандидоза (жалобы на зуд, жжение, выделения), однако на проведенном дополнительно визите ни данные осмотра, ни лабораторные исследования не подтвердили наличие Candida albicans. Эти данные вошли в общую статистику как репортированные обострения. Дополнительная терапия этим пациенткам не проводилась. Данные табл. 2 демонстрируют, что при учете всех случаев рецидива вульвовагинального кандидоза в группах меньшая частота обострений наблюдается в группе исследуемого препарата лактожиналь. Данные различия в группе статистически достоверны (р<0,05).
Расчет абсолютного и относительного риска рецидива ВВК в исследуемых группах представлен в табл. 3.
Отношение шансов рецидива вульвовагинального кандидоза 0,4516 (95% ДИ 0,2067–0,9867). Снижение относительного риска рецидива ВВК в группе лактожиналь составляет -0,1378 (95% ДИ -0,2687 – -0,0069). Таким образом, различия в группах по риску рецидива вульвовагинального кандидоза статистически значимы.
Целью проведенного исследования было выяснить, возможно ли с помощью препарата, содержащего L. casei rhamnosus Doderleini (лактожиналь, капсулы вагинальные), предотвратить рецидив вульвовагинального кандидоза. В качестве критерия эффективности работы препарата лактожиналь после антимикотической терапии оценивалось время до следующего обострения ВВК. По полученным данным, в среднем время до обострения ВВК в группе пациенток, получивших терапию исследуемым препаратом лактожиналь, составило 148,454±2,039 дня, а в группе сравнения (пациентки, получившие только терапию препаратами сертаконазола) – 137,4±4,41 дня. Таким образом, полученные данные демонстрируют тенденцию к пролонгации периода ремиссии при рецидивирующем вульвовагинальном кандидозе в группе пациенток, получавших терапию исследуемым препаратом лактожиналь.
Нежелательных явлений в ходе исследования зарегистрировано не было, как и нежелательных изменений в сопутствующей терапии у пациенток обеих групп.
Обсуждение результатов
Результаты проведенного исследования свидетельствуют об эффективности препарата, содержащего L. casei rhamnosus Doderleini (лактожиналь, капсулы вагинальные), для профилактики обострений в комплексной терапии рецидивирующего вульвовагинального кандидоза. Частота обострения вульвовагинального кандидоза в группе лактожиналь составила 16,2% (12 пациенток), что статистически достоверно ниже, чем в группе сравнения – 30% (24 пациентки) (р<0,05).
Полученные результаты свидетельствуют, что препарат лактожиналь в может эффективно предотвращать рецидив вульвовагинального кандидоза. Статистически значимо и снижение относительного риска рецидива ВВК в группе лактожиналь, которое составляет -0,1378 (95% ДИ -0,2687 – -0,0069). Аналогичные результаты были опубликованы в 2016 г. исследователем R. Davar, где было продемонстрировано достоверное снижение частоты рецидивов кандидоза при использования пробиотиков вместе с азолами (150 мг флуконазола), p=0,01, OR 0,14 (95% ДИ 0,028–0,7) [12].
В исследуемой группе время до рецидива вульвовагинального кандидоза составило 148,454±2,039 дня, а в группе сравнения – 137,4±4,41 дня. Полученные данные демонстрируют тенденцию к пролонгации периода ремиссии при рецидивирующем вульвовагинальном кандидозе в группе пациенток, получавших терапию исследуемым препаратом лактожиналь.
Препарат лактожиналь (лиофилизированная культура лактобактерий L. casei rhamnosus Doderleini (не менее 1×108 КОЕ жизнеспособных лактобактерий), капсулы для вагинального применения) имеет благоприятный профиль безопасности и переносимости.
Заключение
На основании полученных данных можно сделать вывод о снижении риска рецидива вульвовагинального кандидоза при комплексной терапии сертаконазолом (залаин, суппозиторий 300 мг однократно и 2% крем 2 раза в сутки в течение 8 дней) с последующим применением препарата лактожиналь (L. casei rhamnosus Doderleini) в течение 21 дня по сравнению с монотерапией препаратами сертаконазола. При этом исследуемый препарат лактожиналь продемонстрировал достаточную безопасность и хорошую переносимость.
Полученные в результате проведенного клинического исследования данные позволили зарегистрировать новое показание лекарственного препарата лактожиналь – «Профилактика рецидивов вульвовагинального кандидоза (включая обострения рецидивирующего вульвовагинального кандидоза) после местной и/или системной терапии противогрибковыми препаратами». Препарат лактожиналь на настоящий момент – первый и единственный пробиотик, имеющий данное зарегистрированное показание на территории Российской Федерации.



