По данным ВОЗ, пятая часть населения Земли страдает тем или иным грибковым заболеванием. Общая заболеваемость микозами трудно поддается точной оценке, так как до сих пор они не относятся к категории заболеваний, подлежащих строгому учету [1]. До 45% обращений по поводу инфекционной патологии нижнего отдела женской репродуктивной системы приходится на долю вульвовагинального кандидоза (ВВК) [2]. Заболеваемость ВВК занимает ведущее место в структуре инфекционно-воспалительной патологии влагалища и не имеет тенденции к значительному снижению [3]. Более 75% женщин репродуктивного возраста переносят один эпизод неосложненного (острого) ВВК, 40–45% отмечают два и более рецидива заболевания, рецидивирующее течение ВВК встречается у 10–15% [2, 4]. Частота ВВК у беременных женщин достигает 30–35%, бессимптомное носительство – до 40%, что является одной из актуальных проблем современного здравоохранения [5–7].
В связи с выраженной тенденцией к распространению вагинального кандидоза особую важность приобретает проблема его лечения. По причине того, что этиологические возбудители этого заболевания, чаще всего Candida albicans, могут входить в состав нормальной микрофлоры влагалища, конечной целью лечения ВВК является восстановление нормальных показателей микроэкосистемы влагалища, предотвращающих гиперколонизацию грибов [8–10]. Необычайно широкая распространенность заболевания, его устойчивость к терапии и длительное течение заставляют обращать внимание на причины, приводящие к развитию грибковой инфекции и обусловливающие ее существование [1, 3].
Наибольший интерес в патогенезе ВВК представляют факторы, снижающие сопротивляемость макроорганизма. В большинстве случаев вагинального кандидоза, в том числе при его рецидивирующем течении, достаточно сложно выявить какое-либо состояние, однозначно предрасполагающее к инфекции. В связи с этим считается, что в патогенезе принимают участие многие факторы, находящиеся в сложном взаимодействии. К ним традиционно относят дисбаланс нормальной микрофлоры влагалища [11, 12].
Эффективность противогрибковых средств при лечении ВВК может достигать 80–90%. Препаратами выбора по многочисленным публикациям и международным клиническим рекомендациям являются препараты группы имидазолов [3, 6]. Как при наружном (сертаконазол, кетоконазол), так и при пероральном приеме (флуконазол) эффективность имидазолов достаточно высока. Тем не менее, долгосрочное и частое лечение противогрибковыми препаратами является фактором риска формирования резистентных штаммов Candida. Частота развития ВВК, вызванного Candida albicans и non-albicans, существенно возросла в популяции после того, как некоторые антимикотики и их дженерики (в частности флуконазол) были отнесены к безрецептурным препаратам, что связано с развитием устойчивости к ним (до 30% штаммов). При этом наиболее высокий уровень резистентности (45–75%) зафиксирован для non-albicans штаммов – C. krusei и C. glabrata, являющихся наиболее частой этиологической причиной рецидивирующей формы ВВК [13]. Таким образом, возникает проблема поиска и применения альтернативных методов предотвращения рецидивов ВВК [14, 15].
Результаты доклинических и ряда сравнительных клинических исследований свидетельствуют о том, что отдельные штаммы лактобактерий, в том числе L. casei rhamnosus 35 (LCR35) способны подавлять адгезию Candida albicans к вагинальному эпителию и/или пролиферацию Candida albicans [16]. В исследовании in vitro было показано прямое ингибирующее действие, направленное на штаммы грибка Candida albicans, а также non-albicans, при их совместном лабораторном культивировании с лактобактериями LCR35, входящих в состав препарата лактожиналь. При этом полной элиминации грибка удалось достичь в течение первых трех суток ко-инкубации [17]. Обнадеживающие результаты клинических исследований эффективности препарата LCR35 обусловлены особенностями механизма действия этого штамма. Помимо обладания высокими адгезивными свойствами, LCR35 способны выделять бактерицидные факторы, подавляя при этом рост патогенной флоры, в том числе грибковой. Результаты, полученные в доклинических и в ходе интервенционных клинических исследований, свидетельствуют о том, что бактерии LCR35 способны предотвращать возникновения рецидивов и могут применяться в качестве профилактики возникновения рецидивов ВВК [18–20].
Все эти полезные свойства лактобактерии LCR35 обретают в результате уникального технологического процесса, отличного от ряда иных, используемых при производстве других вагинальных и пероральных пробиотиков. Благодаря этому удается достичь уникального трибиотического эффекта препарата, сочетающего в себе 3 компонента: штамм LCR35 (пробиотик), секретируемые метаболиты, обладающие противомикробным действием (постбиотик) и лактозы моногидрат – питательная среда для LCR35 (пребиотик). По данным 2018 года на территории России штамм LCR35 в вагинальной форме представлен только в составе лекарственного препарата лактожиналь.
Цель исследования: изучить эффективность и безопасность препарата, содержащего культуру лактобактерий LCR35 (лактожиналь, капсулы вагинальные), в профилактике рецидивов вульвовагинального кандидоза после системной и/или местной терапии противогрибковыми препаратами.
Материал и методы исследования
В рамках многоцентрового открытого проспективного сравнительного неинтервенционного исследования эффективности и переносимости препарата лактожиналь для профилактики рецидивов вульвовагинального кандидоза после системной и/или местной терапии противогрибковыми препаратами приняло участие 800 пациенток с диагнозом острый вульвовагинальный кандидоз (ВВК) в 78 лечебно-профилактических учреждениях России, обеспечивающих медицинскую помощь женщинам с данной патологией. Расчет объема выборки осуществлялся, исходя из того, что пропорция пациенток без рецидива ВВК в группе сравнения приблизительно составит 30% (в соответствии с данными ранее проведенного исследования Револакт) [16]. Предполагаемое различие между группами – не менее 20%. Расчет объема выборки проводился с учетом необходимой мощности 80% (бета ошибка 20%) и допустимой альфа-ошибки 5%.
Пациентки в зависимости от назначенной им терапии распределялись в две группы в соотношении 1:3. Пациентки 1 группы (200 пациенток) получали курс терапии ВВК системной и/или местной терапии противогрибковыми препаратами. Пациентки 2 группы (600 пациенток) получали курс терапии ВВК системной и/или местной терапии противогрибковыми препаратами, а затем препарат, содержащий культуру лактобактерий LCR35 (лактожиналь) по 1 капсуле вагинально на ночь в течение 21 дня. У всех пациенток на момент включения в исследование был диагностирован острый вульвовагинальный кандидоз.
При проведении исследования соблюдались следующие критерии включения\невключения пациентов.
Критерии включения в исследование:
- Наличие подписанного информированного согласия пациентки на участие в исследовании;
- Наличие острого вульвовагинального кандидоза (не менее двух локальных признаков и симптомов: зуд, жжение, отек слизистой, обильные выделения «творожистого характера»);
- Женщины в возрасте 18–45 лет;
- Назначение пациентке системной и/или местной терапии противогрибковыми препаратами, а также, в зависимости от выбранной тактики лечения, назначение препарата Лактожиналь.
Решение врача о выборе терапии, а также о тактике дальнейшего лечения должно быть принято до включения пациентки в исследование и независимо от него.
Критерии невключения в исследование:
- Инфекции, передаваемые половым путем (ИППП) на момент включения в исследование;
- Беременность;
- Любые клинические состояния, которые, по мнению врача-исследователя, противоречат критериям включения, могут стать причиной досрочного прекращения ее участия в исследовании или затруднят трактовку результатов последнего;
- Противопоказания к терапии препаратом лактожиналь, перечисленные в утвержденной инструкции;
- Клинически значимые иммунодефицитные состояния;
- Применение других препаратов из группы пре- и/или пробиотиков, препаратов, закисляющих влагалищную среду и/или содержащих другие виды лактобацилл.
Для постановки диагноза и оценки эффективности лечения всем пациенткам был проведен следующий объем обследования: клиническое (жалобы, анамнез, общий и гинекологический осмотр), лабораторное (микроскопическое исследование мазка влагалищного секрета для верификации диагноза ВВК, определение pH). У всех пациенток на момент включения в исследование был подтвержден диагноз острый вульвовагинальный кандидоз. Данные осмотра свидетельствовали о текущем ВВК по состоянию слизистой влагалища и характеру выделений, значениям рН.
Исследование состояло из трех этапов. Первый этап – всем пациенткам проводилась терапия системными и/или местными противогрибковыми препаратами. Второй этап – начинался сразу после окончания курса противогрибковой терапии. Во время второго этапа осуществлялся прием исследуемого препарата лактожиналь по одной вагинальной капсуле ежедневно в течение 21 дня. В это время пациентки группы сравнения не получали какую-либо терапию и находились под наблюдением. Третий этап – наблюдение в течение 5 месяцев с момента окончания терапии препаратом лактожиналь.
Критериями эффективности терапии служили:
- время до следующего рецидива ВВК (дни);
- общее количество обострений вульвовагинального кандидоза в течение всего исследования;
- оценка приверженности пациентов к терапии исследуемым препаратом (с помощью валидированного многофакторного опросника на исследование приверженности к фармакотерапии).
Оценка безопасности включала сбор и последующий анализ частоты и тяжести всех нежелательных явлений со стороны пациентки, в том числе, частота и тяжесть нежелательных явлений, связанных с приемом препарата.
При проведении статистического анализа количественные данные были суммированы с использованием средней, стандартного отклонения, медианы, минимальных и максимальных величин. Качественные данные суммированы по частоте и процентам. Все статистические тесты являются двусторонними при уровне значимости р<0,05. Для проверки гипотезы об исходной однородности групп исследования было проведено тестирование нулевых гипотез при помощи t-критерия Стьюдента (для количественных показателей между независимыми выборками с нормальным распределением в исследуемой популяции), критерия Манна-Уитни (для показателей с распределением, отличающимся от нормального) или критерия χ2 (для качественных признаков). Если предпосылки применения критерия χ2 не выполнялись, применялся точный двусторонний критерий Фишера.
Статистические сравнения ДО – ПОСЛЕ терапии были проведены с помощью методов непараметрического теста знаковых рангов Уилкоксона внутри групп, а сравнение полученных изменений между терапевтическими группами – с помощью непараметрического критерия Уилкоксона-Манна-Уитни. Доли пациентов в группах сравнивались на основе критерия χ2 (или точного критерия Фишера). Для оценки и сравнения времени до следующего рецидива ВВК после проведенной терапии между исследуемыми группами был использован анализ выживания Каплана-Майера (статистический критерий Log rank).
Результаты исследования и обсуждение
Клинические проявления рецидива ВВК, как подтвержденные лабораторно, так и неподтвержденные, являются важным критерием эффективности терапии. При наличии рецидива ВВК именно клинические симптомы кандидоза являются маркером обострения, снижают качество жизни пациенток даже без лабораторного подтверждения, а эффективность лечения оценивается с позиций удлинения времени до следующего рецидива. Целью проведенного исследования было выяснить, возможно ли с помощью препарата, содержащего культуру LCR35, профилактировать рецидивы острого вульвовагинального кандидоза. В качестве критерия эффективности препарата после курса антимикотической терапии оценивалось время до следующего обострения (рецидива) ВВК.
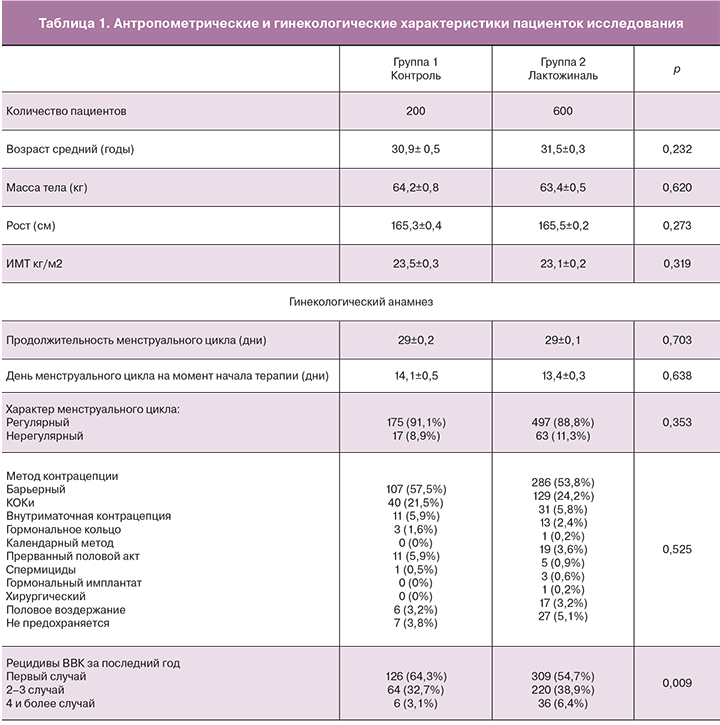
По антропометрическим показателям и гинекологическому анамнезу пациентки достоверно не различалась между исследуемыми группами (табл. 1). Однако, по данным гинекологического анамнеза количество обострений ВВК за прошедший год до включения в исследование, включая текущее обострение, было значимо большим в группе пациентов, включенных в исследуемую группу, получавших терапию препаратом лактожиналь (p=0,009), таблица 1.
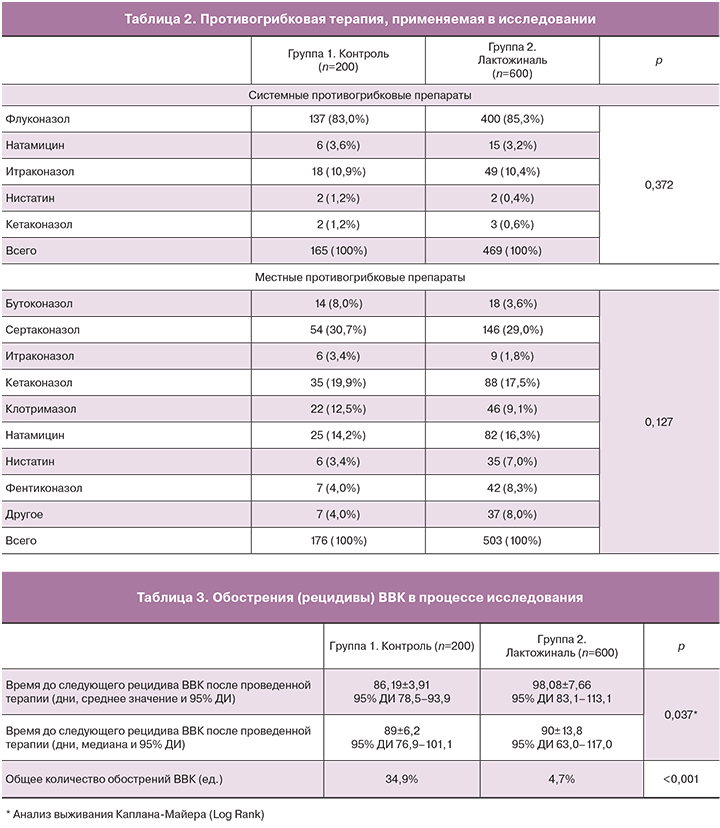
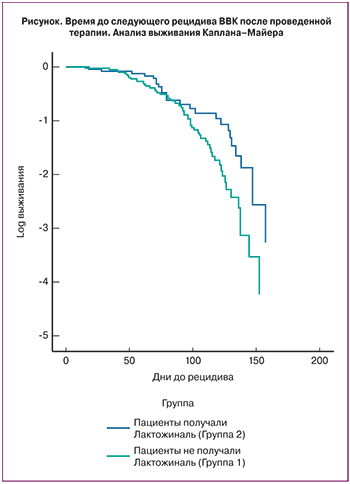
Все пациентки исследования на первом этапе терапии получали местные и/или системные противогрибковые препараты (табл. 2). Полученные в исследовании данные показали, что время до рецидива ВВК было значимо большим в группе 2 (где применялся препарат лактожиналь) 98,08±7,66 дней по сравнению с группой 1 – 86,19±3,91 дней, p=0,037. Таким образом, полученные данные демонстрируют тенденцию к пролонгации безрецидивного периода после терапии острого ВВК в группе пациенток, получавших терапию исследуемым препаратом лактожиналь (табл. 3, рисунок).
Общая частота обострения (рецидивов) ВВК в группе лактожиналь была достоверно ниже (4,7%) по сравнению с группой, где не применялся исследуемый препарат (34,9%), р<0,001, что также подтверждает доказываемую эффективность исследуемого препарата лактожиналь в профилактике рецидивов острого ВВК (табл. 3).
 Оценка приверженности пациентов к терапии исследуемым препаратом лактожиналь показала высокий уровень (178,16±1,16 баллов) по шкале валидированного многофакторного опросника на исследование приверженности к фармакотерапии (171–200 баллов – высокий уровень приверженности).
Оценка приверженности пациентов к терапии исследуемым препаратом лактожиналь показала высокий уровень (178,16±1,16 баллов) по шкале валидированного многофакторного опросника на исследование приверженности к фармакотерапии (171–200 баллов – высокий уровень приверженности).
Таким образом, результаты проведенного наблюдательного исследования свидетельствуют об эффективности препарата, содержащего культуру лактобактерий LCR35 для профилактики обострений в комплексной терапии острого вульвовагинального кандидоза (вторым этапом после курса системной и/или местной противогрибковой терапии).
За время проведения настоящего наблюдательного исследования нежелательные явления были зарегистрированы у 62 пациенток: 44 (7,33%) исследуемой группы и 18 (9,0%) группы контроля. Анализ количества и выраженности нежелательных явлений, выявляемых в процессе исследования, показал, что группы лечения были сопоставимы по параметрам безопасности, без статистически значимых различий, p>0,05. Таким образом, препарат лактожиналь, содержащий культуру лактобактерий LCR35 (капсулы для вагинального применения), имеет благоприятный профиль безопасности и переносимости.
Заключение
На основании полученных данных проведенного наблюдательного исследования можно сделать вывод, что применение препарата лактожиналь, содержащего культуру лактобактерий LCR35, в комплексной терапии ВВК после системных и/или местных противогрибковых препаратов способствует снижению риска рецидива заболевания в 7 раз по сравнению с монотерапией противогрибковыми препаратами.
При этом исследуемый препарат продемонстрировал хорошую переносимость и приверженность к терапии.
Предлагаемый двухэтапный метод терапии с интравагинальным применением лактобактерий LCR35 после завершения базового курса антимикотика направлен на снижение рецидива ВВК и имеет преимущество над используемым одноэтапным методом лечения данного заболевания.



