Заболевания, сопровождающиеся патологическими выделениями из половых путей, – актуальная и социально значимая проблема современной гинекологии. Европейское общество по противодействию инфекциям, передаваемым половым путем (IUSTU), в 2018 г. выделило четыре заболевания, являющихся основными причинами патологических выделений из половых путей, – бактериальный вагиноз (БВ), аэробный вагинит (АВ), кандидозный вульвовагинит (КВВ) и трихомониаз [1]. Наиболее частыми причинами заболеваний, сопровождающихся патологическими выделениями из половых путей, являются БВ, а также вагинит сочетанной этиологии [2]. Заболеваемость вульвовагинитом бактериальной и грибковой природы неуклонно растет. Так, в США и Великобритании их число за первое десятилетие ХXI в. увеличилось почти вдвое, схожая ситуация наблюдается и в других развитых странах [3]. В России вагинит является наиболее частой причиной обращения к гинекологу среди пациенток от 18 до 50 лет [4]. Вульвовагинит существенно ухудшает качество жизни женщин и может способствовать развитию осложнений беременности. Кроме того, БВ и трихомониаз повышают риск приобретения и передачи других опасных инфекционных заболеваний, в частности вирус иммунодефицита человека (ВИЧ) [5].
По современным данным, примерно у 30% пациенток, обращающихся с жалобами на патологические выделения из половых путей, наблюдается клиническая картина вагинита, в основе развития которого лежат несколько патологических состояний, что принято называть вагинитом сочетанной этиологии. При этом такая комбинация состояний может рассматриваться как самостоятельная патогенетическая сущность, нежели просто коинфекция разнообразными микроорганизмами [6]. Наиболее часто встречается сочетание БВ и КВВ, при этом ситуация осложняется тем, что одно из этих состояний может проявляться уже после санации другого, приводя к клиническому рецидиву заболевания [6]. В этой же работе показано, что сочетанные инфекции имеют более тяжелое, длительное и нетипичное течение, частые рецидивы и риск развития восходящей инфекции.
Вместе с тем известно, что методы, широко применяемые для диагностики заболеваний, сопровождающихся патологическими выделениями из половых путей, в первую очередь основанные на микроскопии, оказываются малоинформативными и зачастую не позволяют поставить точный диагноз, число ошибочных диагнозов может превышать 70% [7, 8].
К сожалению, на сегодняшний день четкие схемы лечения сочетанных вульвовагинальных инфекций отсутствуют, а их высокая распространенность зачастую провоцирует полипрагмазию, которая, в свою очередь, способствует развитию общего фона устойчивости возбудителей инфекции к наиболее распространенным лекарственным препаратам [9]. Так, уже с 1962 г. регистрируются случаи резистентности к метронидазолу, доказана перекрестная устойчивость к тинидазолу и орнидазолу, что свидетельствует о формировании устойчивости ко всей группе 5-нитроимидазолов [10].
Таким образом, распространенность вульвовагинита сочетанной этиологии, трудности с постановкой точного диагноза, возрастающая резистентность к широко используемым лекарственным препаратам приводят к необходимости поиска альтернативных схем терапии для лечения заболеваний, сопровождающихся патологическими выделениями из половых путей, которые, с одной стороны, будут способны справиться с широким спектром возбудителей, а с другой – позволят решить проблему резистентности к терапии.
Цель настоящей работы заключалась в изучении этиологии заболеваний, сопровождающихся патологическими выделениями из половых путей, в клинической практике на основе высокоэффективных молекулярно-биологических методов лабораторной диагностики, а также оценке переносимости лечения заболеваний, сопровождающихся патологическими выделениями из половых путей у женщин, препаратом «Макмирор Комплекс», содержащим нифурател и нистатин.
Материалы и методы
Проспективная многоцентровая наблюдательная программа «Проспект» была проведена в период с января по июль 2020 г. в 11 клинических центрах 10 городов Российской Федерации (Москва, Санкт-Петербург, Нижний Новгород, Воронеж, Ставрополь, Казань, Уфа, Новосибирск, Екатеринбург, Владивосток). Критериями включения в программу являлись: женский пол, возраст от 18 до 49 лет на момент включения, наличие жалоб на патологические выделения из половых путей, подтвержденных при клиническом обследовании, установленный диагноз «бактериальный вагиноз», «кандидозный вульвовагинит», «аэробный вагинит», «вагинит сочетанной этиологии» на основании лабораторного молекулярно-биологического исследования, решение врача о назначении терапии комбинированным препаратом, включающим нифурател и нистатин (препаратом «Макмирор Комплекс»), в амбулаторных условиях, а также согласие пациентки участвовать в исследовании. Все пациентки подписывали информированное согласие на участие в наблюдательной программе.
В программу не включались пациентки, у которых присутствовал один или более критериев: 1) беременность; 2) возраст 50 лет и старше; 3) системное или локальное использование антибиотиков в течение 1 месяца перед включением в программу; 4) локальное применение противомикробных, антисептических препаратов в течение 1 месяца перед включением в программу; 5) инфекционно-воспалительные заболевания в стадии обострения, не связанные с заболеваниями, сопровождающимися патологическими выделениями из половых путей, инфекции, передающиеся половым путем (ИППП); 6) сахарный диабет в стадии суб- и декомпенсации; 7) наличие противопоказаний для назначения препарата «Макмирор Комплекс».
На визите для включения в программу проводился сбор данных о возрасте пациенток и гинекологическом анамнезе (число половых партнеров за последний год, число обострений вульвовагинита и цистита в течение последнего года, жалобы на наличие патологических выделений из половых путей/зуд/жжение у полового партнера). Врач оценивал наличие жалоб у пациентки, в частности, наличие зуда, жжения, дискомфорта во влагалище, а также проводил гинекологическое обследование с оценкой клинических признаков вульвовагинита: патологические выделения из влагалища, их цвет (белые, желтоватые и т.п.) и выраженность в заднем своде влагалища (отсутствие, умеренные, выраженные), рН вагинальных выделений, признаки гиперемии и отека слизистой оболочки влагалища и наружных половых органов. Во время гинекологического осмотра получали образцы биологического материала – отделяемого из влагалища и цервикального канала для микроскопического и отделяемого влагалища для молекулярно-биологического исследований с помощью одноразовых зондов-тампонов. Для микроскопического исследования полученный материал наносили на предметное стекло и оценивали на базе локальных лабораторий исследовательских центров. Для молекулярно-биологического исследования полученный образец вагинального отделяемого помещался в пробирку с транспортной средой «ТСМ» (ООО «НекстБио») для дальнейшей транспортировки в клинико-диагностическую лабораторию для исследования.
Для установления этиологии заболеваний, сопровождающихся патологическими выделениями из половых путей, проводилось лабораторное молекулярно-биологическое исследование с использованием наборов реагентов линейки «АмплиПрайм-Флороскрин» (ООО «НекстБио»): «АмплиПрайм-Флороскрин-Бактериальный вагиноз», «АмплиПрайм-Флороскрин-Кандида», «АмплиПрайм-Флороскрин-Аэробы». Дополнительно проводилось исследование на наличие сопутствующих инфекций, вызванных M. hominis, U. urealyticum, U. parvum, с использованием набора реагентов «АмплиПрайм-Флороскрин-Микоплазмы».
Диагноз соответствующего заболевания устанавливали на основании результатов клинического обследования и лабораторного заключения по тестам «АмплиПрайм-Флороскрин».
В ходе программы в скрининге участвовали 206 пациенток, из них всем критериям включения соответствовали 93 женщины. Данным пациенткам был назначен в амбулаторных условиях препарат «Макмирор Комплекс» в соответствии с инструкцией по медицинскому применению. Продолжительность терапии Макмирор Комплексом определялась лечащим врачом в соответствии с инструкцией по медицинскому применению препарата и действующими клиническими рекомендациями при установленном заболевании, составляя в среднем 8 дней.
Все включенные в исследование пациентки в рамках программы осуществляли 4 визита к врачу: 1-й, вышеописанный, визит включения с назначением терапии (визит 1, день 0) и 3 визита наблюдения через 10 (визит 2), 30±7 (визит 3) и 90±7 (визит 4) дней от 1-го визита. На каждом визите наблюдения проводилась оценка субъективных симптомов и объективных клинических проявлений заболевания, а также гинекологическое обследование с получением биологического материала для микроскопического и молекулярно-биологического исследований, как описано выше.
Первичной целью являлась оценка доли пациенток с клинико-лабораторно установленными диагнозами «бактериальный вагиноз», «кандидозный вульвовагинит», «аэробный вагинит» и «вагинит сочетанной этиологии», достигших клинического выздоровления на 2-м визите.
Вторичные цели включали оценку:
- этиологической структуры заболеваний, сопровождающихся патологическими выделениями из половых путей;
- доли пациенток с диагнозами «бактериальный вагиноз», «кандидозный вульвовагинит», «аэробный вагинит» и «смешанный вагинит», достигших состояния нормы по данным молекулярно-биологического исследования (АмплиПрайм-Флороскрин) на 3-м визите;
- доли пациенток с отличной и хорошей переносимостью терапии на 2-м визите;
- доли клинических рецидивов на 3-м и 4-м визите;
- доли пациенток с нежелательными явлениями (НЯ) во время проведения наблюдательной программы.
Клиническую эффективность терапии оценивали на 2-м визите (10-й день наблюдения) по критериям разрешения субъективных симптомов (зуд/жжение, дискомфорт) и объективных признаков – патологических выделений, гиперемии и отека слизистых влагалища, нормализации pH. Анализ наличия клинических рецидивов проводился на 3-м и 4-м визитах, т.е. на 30±7 и 90±7 день наблюдения соответственно. Лабораторные молекулярно-биологические (тест «АмплиПрайм-Флороскрин») показатели эффективности лечения оценивались на 3-м визите, т.е. на 30±7 день наблюдения. На 2-м визите пациентки оценивали переносимость применяемой терапии как отличную, хорошую, удовлетворительную или неудовлетворительную. Также фиксировались возникающие в ходе программы НЯ, их тяжесть и возможная связь с препаратом.
Статистический анализ
В соответствии с дизайном программы для анализа демографических и иных характеристик исследуемой популяции применялись методы описательной статистики в программе Microsoft Exсel.
Результаты
Терапию препаратом «Макмирор Комплекс» получили 93 пациентки. Средний возраст составил 32,2±7,4 года. В числе сопутствующих заболеваний 8/29 (27,6%) ответивших пациенток указали наличие хронического цистита (более 3 обострений цистита за год либо более 1 обострения за полгода). На вопрос о предшествующих рецидивах вагинальной инфекции ответили 78/93 (84%) пациенток. Из них 52/78 (66,7%) отметили рецидивы вагинита менее 3 раз за последний год до включения в программу, 16/78 (20,5%) – от 3 до 6 эпизодов за год, и 10/78 (12,8%) – более 6 эпизодов за предшествующий наблюдению год.
На вопрос о наличии жалоб у половых партнеров смогли ответить 91/93 (98%) пациенток. 5,5% подтвердили наличие жалоб в виде покраснения головки полового члена, а 94,5% сообщили, что какие-либо жалобы у их половых партнеров отсутствовали. В течение года, предшествующего включению в программу, у 77/92 (83,7%) ответивших пациенток было менее 5 половых партнеров, у 15/92 (16,3%) – более 5.
На 1-м визите у всех 93 пациенток отмечались жалобы на патологические выделения из половых путей с изменением цвета и/или запаха, у 43/93 (46,2%) выделения имели выраженный характер, 50/93 (53,8%) оценивали выделения как умеренные. Наличие выраженного и умеренного зуда/жжения/дискомфорта во влагалище отмечали 79/93 (85%) пациенток.
Распределение диагнозов в группе 93 пациенток было представлено следующим образом: как моноэтиологические состояния, в частности БВ, АВ, КВВ, и как вагинит сочетанной этиологии: БВ+КВВ, АВ+КВВ, БВ+АВ и БВ+АВ+КВВ (рис. 1).
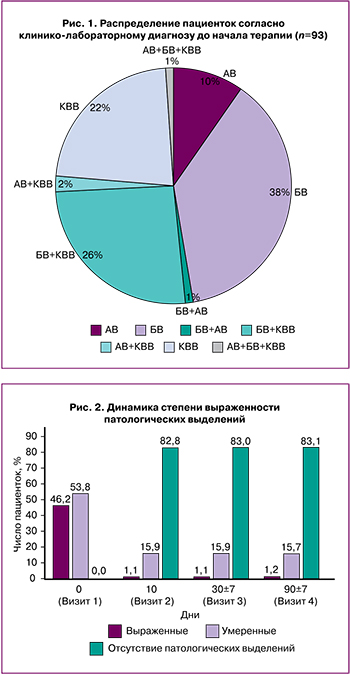
Стоит отметить, что наличие признаков воспаления при гинекологическом осмотре (гиперемия и отек слизистых влагалища) наблюдалось у 52/93 (56%) пациенток, что в целом соответствовало этиологической структуре на основе результатов лабораторного исследования.
Все 93 пациентки завершили назначенный курс терапии препаратом «Макмирор Комплекс». На 2-м визите купирование патологических выделений после терапии, подтвержденное гинекологическим осмотром, наблюдалось в 77/93 (82,8%) случаев. Достигнутый результат сохранялся через 1 и 3 месяца наблюдения. Отдельного внимания также заслуживает положительная динамика степени выраженности патологических выделений (рис. 2).
Выделения имели выраженный характер на 2-м визите только у 1/93 (1,1%) пациенток, на 3-м – у 1/88 (1,1%) и на 4-м – у 1/83 (1,2%) пациенток.
Разрешение субъективных симптомов (зуд/жжение, дискомфорт) на 2-м визите было достигнуто в 88/93 (94,6%) случаев. Важно подчеркнуть, что эта положительная динамика сохранялась при оценке наличия жалоб пациенток на 3-м и 4-м визитах (рис. 3).
Данные клинической эффективности (динамика субъективных симптомов) в подгруппах по нозологиям возбудителей представлены в таблице.

Купирование признаков воспаления – гиперемии и отека – после терапии, по данным гинекологического осмотра, наблюдалось у 89/93 (95,7%) и 93/93 (100%) пациенток соответственно на 2-м визите, с полным разрешением на 3-м месяце наблюдения (4-й визит) (рис. 4).
На фоне лечения Макмирор Комплексом pH влагалищной среды возвращался к нормальным значениям (рис. 5).
Отметим, что только 60% (55/93) пациенток были доступны для проведения молекулярно-биологических исследований (тест «АмплиПрайм-Флороскрин») на 3-м визите. Эффективность нормализации состояния вагинальной микробиоты спустя 1 месяц наблюдения в подгруппе КВВ достигнута у 14/16 (87,5%) женщин, явившихся на 3-й визит, в подгруппе БВ – у 16/23 (70%) и в подгруппе БВ+КВВ – у 9/13 (70%). В группе АВ данный показатель оценить не представлялось возможным в связи с явкой всего 1 из 9 пациенток с подтвержденным диагнозом на 1-м визите. Аналогичная ситуация в группах смешанных инфекций – АВ+КВВ, БВ+АВ и БВ+АВ+КВВ – данные нерепрезентативны в связи с малой выборкой.
На 2-м визите в 85,3% случаев отмечалась отличная и хорошая переносимость Макмирор Комплекса (5,6 и 79,7% соответственно), а отсутствие аллергических реакций – в 100% случаев. Ни одна из пациенток не отказалась от назначенного лечения по причине непереносимости. НЯ в ходе программы зафиксировано не было.
Обсуждение
Данные проспективной наблюдательной многоцентровой программы «Проспект» показали преобладание БВ и заболеваний сочетанной этиологии при анализе частоты встречаемости возбудителей заболеваний, сопровождающихся патологическими выделениями из половых путей, среди обратившихся к врачу-гинекологу российских женщин репродуктивного возраста, что в целом согласуется с современными мировыми данными [6, 7].
Высокая распространенность заболеваний, сопровождающихся патологическими выделениями из половых путей, сочетанной этиологии обуславливает необходимость назначения в рутинной практике множества лекарственных препаратов для достижения комплексного эффекта. К сожалению, неконтролируемое их применение ведет к непредсказуемому лекарственному взаимодействию, снижению приверженности к лечению и, как следствие, ухудшению состояния здоровья и качества жизни пациенток. Так, по результатам наблюдательной программы треть пациенток с заболеваниями, сопровождающимися патологическими выделениями из половых путей, страдали хроническими заболеваниями мочеполовой сферы (25% отмечали хронический цистит и до 30% – хронические вагинальные инфекции), и половине этих женщин назначалось более 1 препарата. Это подтверждает высказанный выше тезис о распространенности полипрагмазии в лечении данной категории пациенток, способствующей развитию лекарственной устойчивости возбудителей.
Согласно метаанализу A. Muñoz-Barreno (2021), включавшему 35 рандомизированных контролируемых исследований по изучению эффективности препаратов 1-й линии терапии БВ – метронидазола или клиндамицина у небеременных женщин (в различных дозировках/способах введения), клиническая эффективность лечения составляла 74,6% (69,1–79,3) [11]. Но, несмотря на приемлемые показатели эффективности, в настоящее время отмечается высокий процент рецидивов вагинальных инфекций на фоне применения стандартной терапии. Так, частота рецидивов БВ на фоне применения метронидазола или клиндамицина достигает 50% случаев в течение 6 месяцев наблюдения [12, 13], что обращает внимание специалистов на поиск альтернативных схем терапии. Большой интерес с этой точки зрения представляет итальянский препарат «Макмирор Комплекс» – нифурател в комбинации с нистатином, антимикробное средство с антибактериальным, противогрибковым и противопротозойным действиями.
Спектр действия нифуратела включает широкий диапазон микроорганизмов, в том числе основных возбудителей БВ и АВ. В 2011 г. были опубликованы данные исследования in vitro, где в сравнении с клиндамицином и метронидазолом нифурател (Макмирор) продемонстрировал высокую эффективность при лечении инфекций, вызванных Gardnerella vaginalis и Atopobium vaginae, и при этом не оказывал влияния на нормальную вагинальную флору и лактобактерии влагалища [14]. Последнее было подтверждено и в ряде клинических исследований [15–17]. Нифурател активен в отношении Trichomonas vaginalis и грибов рода Candida.
Второй компонент препарата «Макмирор Комплекс» – нистатин также активен в отношении всех видов Candida, включая С. non-albicans. При этом немаловажно, что нифурател усиливает противогрибковую активность нистатина. Таким образом, комбинированный препарат не просто представляет собой комбинацию двух известных агентов, но и обладает синергическим эффектом [18].
В настоящий момент продолжается поиск наиболее эффективной стратегии медикаментозного лечения вагинальных инфекций. Целесообразность применения комплексных препаратов для лечения заболеваний, сопровождающихся патологическими выделениями из половых путей, обоснована не только распространенностью инфекций сочетанной этиологии, но и проблемой формирования бактериальных биопленок, включающих целые бактериальные сообщества и являющих причиной клинических рецидивов заболевания. В исследованиях также было показано, что C. albicans в присутствии полимикробной ассоциации приобретает свойство тканевой инвазии, переходя в мицеллярную форму в глубоких слоях эпителия влагалища, что может служить резервуаром для ее персистенции после проведенной антибактериальной терапии [19]. В связи с этим применение комбинированной терапии является объективной необходимостью, так как она имеет потенциальные преимущества благодаря более широкому спектру действия, большему потенциалу по сравнению с препаратами, применяемыми в монотерапии, в снижении количества устойчивых организмов и более низкой толерантности к противогрибковым средствам [20]. Также важным моментом является возможность назначения комбинированной терапии пациенткам эмпирически, без лабораторно подтвержденного диагноза, так как именно наличие у большинства пациенток клинической картины заболеваний, сопровождающихся патологическими выделениями из половых путей, является основным показанием к лечению, исключая инфекции, передающиеся половым путем.
Одним из таких перспективных комбинированных препаратов является «Макмирор Комплекс», в отношении эффективности и безопасности которого проводится ряд масштабных исследований [21]. Действительно, препарат «Макмирор Комплекс» неоднократно изучался в ходе клинических исследований, неизменно показывая высокую эффективность и хорошую переносимость. Мультицентровое исследование в Швейцарии с участием 465 пациенток со смешанной вагинальной инфекцией показало, что полное выздоровление в результате терапии препаратом «Макмирор Комплекс» наблюдалось у 66,2% пациенток, при этом частота рецидивов через 1 месяц после терапии составила всего 28,5% даже у пациенток, прежде страдавших от рецидивирующей формы заболевания в течение 6 месяцев и дольше [15]. В исследовании 2010 г. (Хорватия) на 70 пациентках применение комбинации нифуратела с нистатином привело к полному выздоровлению при БВ в 71%, при кандидозе – в 93% и при трихомониазе – в 100% случаев [16]. В ходе отечественного исследования на 197 пациентках с БВ, включающим Atopobium vaginae, сравнивалась эффективность комбинации нифуратела и нистатина с метронидазолом. По результатам исследования комбинированная терапия оказалась эффективна в 93% случаев, в то время как в группе метронидазола положительный результат был достигнут только в 10% случаев [22]. Учитывая, что Atopobium vaginae является основным ассоциантом с G. vaginalis при формировании биопленки и обнаруживается у более чем 80% пациенток, страдающих БВ, данные результаты, безусловно, говорят о том, что в подобном случае комбинированный препарат является терапией выбора, что подтверждают российские клинические рекомендации по диагностике и лечению заболеваний, сопровождающихся патологическими выделениями из половых путей, 2019 г. [23].
Полученные в рамках настоящей наблюдательной программы данные рутинной клинической практики врачей-гинекологов на территории РФ согласуются с результатами проведенных ранее международных клинических исследований [15, 16, 24, 25]. В данной работе применение препарата «Макмирор Комплекс» в лечении заболеваний, сопровождающихся патологическими выделениями из половых путей, различной этиологии, включая случаи инфекций сочетанной этиологии и рецидивирующего течения заболевания, продемонстрировало высокую эффективность и безопасность. Клиническая эффективность терапии в разрешении беспокоящих пациенток симптомов (зуд, жжение и дискомфорт во влагалище) достигнута в 94,6% случаев, в том числе и при внутригрупповом анализе по микробиологически подтвержденным диагнозам. В течение 3 месяцев наблюдения клинические рецидивы наблюдались не более чем в 8,3% случаев в целом, главным образом в группе инфекции сочетанной этиологии с самой частой комбинацией БВ+КВВ. Объективные симптомы, такие как отек влагалища, гиперемия и выделения из половых путей, также купировались у абсолютного большинства пациенток. Следует отметить, отличную динамику разрешения выраженности сохраняющихся на этапе наблюдения патологических выделений. А результаты лабораторного (молекулярно-биологического) исследования показали эффективность восстановления микробиоты в 87,5% случаев спустя 1 месяц наблюдения, а также нормализацию рН влагалища. Весьма низкое количество рецидивов даже у тех пациенток, кто раньше испытывал их более 6 раз в год, несмотря на получаемую антимикробную и противогрибковую терапию, говорит о том, что препарат показал себя эффективным в долгосрочной перспективе. В подавляющем большинстве пациентки оценили переносимость препарата в среднем как хорошую и были полностью привержены назначенному лечению.
Безусловно, ограничением исследования является отсутствие строгих/узких критериев включения в программу, а также группы сравнения и рандомизации, частичная неявка пациенток на визиты/не полностью проведенные визиты в ходе наблюдательной программы, главным образом вследствие неблагоприятной эпидемиологической обстановки в начале 2020 г. Учитывая преобладание сочетанного характера вагинальных инфекций, этот факт, безусловно, затруднял точную диагностику заболеваний, сопровождающихся патологическими выделениями из половых путей, в условиях реальной клинической практики.
В то же время в данной статье представлены результаты первой многоцентровой проспективной наблюдательной программы, проведенной по всей территории РФ, – в 10 городах. Дизайн данной программы имеет свою особенность – преимущество в виде изучения результатов терапии заболеваний, сопровождающихся патологическими выделениями из половых путей, в клинической практике с независимой молекулярно-биологической диагностикой заболевания. Используемый метод диагностики с использованием наборов реагентов линейки «АмплиПрайм-Флороскрин» (ООО «НекстБио») продемонстрировал информативность и точность у пациенток с вагинальными выделениями в ряде клинических исследований [26–28]. Это позволило минимизировать риск диагностических ошибок и провести объективный анализ результатов лечения в подгруппах пациенток.
Наличие хронических заболеваний мочеполовой сферы с неоднократными курсами антимикробных препаратов в анамнезе у трети пациенток свидетельствует о необходимости тщательного обследования и подбора адекватной терапии с учетом уже, возможно, имеющейся резистентности возбудителей к стандартным препаратам. Нифурател в составе Макмирор Комплекса относится к группе нитрофуранов, к которым крайне редко развивается лекарственная устойчивость [29]. Именно поэтому мы считаем, что выбор препарата из иной группы, чем стандартные средства терапии, в данном исследовании был целесообразным.
Безусловно, в настоящее время возрастает актуальность проведения дальнейших рандомизированных клинических исследований комплексной терапии заболеваний, сопровождающихся патологическими выделениями из половых путей, в Российской Федерации.
Заключение
Высокая распространенность инфекций сочетанной этиологии среди заболеваний, сопровождающиеся патологическими выделениями из половых путей, а также рост лекарственной устойчивости возбудителей представляют собой актуальную проблему при выборе эффективной терапии вагинальной инфекции. Благодаря широкому спектру действия, отсутствию микробиологической резистентности и негативного влияния на лактобактерии влагалища комбинированный препарат «Макмирор Комплекс» показал показал высокую эффективность и хорошую переносимость, в связи с чем может быть рекомендован для активного применения в клинической практике для лечения заболеваний, сопровождающиеся патологическими выделениями из половых путей, в том числе при вагинитах сочетанной этиологии.



