В 1974 г., в классическом издании по оперативному акушерству Михаил Сергеевич Малиновский указывал: «Истинное приращение плаценты - явление очень редкое». Однако с середины XX в. по настоящее время частота врастания плаценты в рубец на матке (ВПРМ) возросла в 50-60 раз: с 1:25 000-50 000 родов до 1:500-1000 в настоящее время, а в специализированных центрах - до 1:343 [1, 2]. По сведениям FIGO (2018), имеются убедительные эпидемиологические доказательства того, что врастание плаценты по существу стало ятрогенным состоянием в результате повышения частоты кесарева сечения (КС) во всем мире. В связи с высоким риском массивной кровопотери и материнской смертности данная патология является актуальной проблемой современного акушерства, а оптимизация кровесберегающих технологий стала ее важнейшим аспектом [3-9]. Учитывая гетерогенный состав пациенток с placenta accreta spectrum (PAS), оптимизация хирургической тактики подразумевает рациональный баланс между характером хирургической травмы, эффективностью и безопасностью вмешательства относительно реально существующей патологии в каждом конкретном случае. Мы постарались подвести предварительные итоги нашей деятельности с февраля 2018 г., когда наше учреждение стало аккумулировать пациенток с PAS.
Цель исследования: усовершенствование тактики родоразрешения беременных с рубцом на матке и аномальной плацентацией.
Материалы и методы
В исследование включены 54 беременных с рубцом на матке и аномальной плацентацией (центральное предлежание плаценты) в сроке более 22 недель, поступившие в Ташкентский городской перинатальный центр (ТГПЦ) в период 20182020 гг. Критерием включения явилось наличие у пациентки 1 и более рубцов на матке после КС, центрального предлежания плаценты (ПП) и признаков врастания плаценты (ВП) по данным УЗИ, МРТ и гистологического исследования.
Возраст пациенток колебался от 21 до 41 года, средний возраст беременных составил 31 (21;41) год. Среднее число беременностей в анамнезе - 3,9±1,3. С одним рубцом на матке (РНМ) было 27,8% (15/54) женщин, с 2 - 51,8% (28/54), с 3 - 12,9% (7/54), с 4 - 7,4% (4/54). Двойня имела место у 3,7% (2/54). Самопроизвольные роды (до КС) в анамнезе были у 11,1% (6/54) женщин. Артифициальных абортов в анамнезе не отмечено, замерших беременностей было 14,8% (8/54) в сроках гестации от 5 до 14 недель. Срок беременности, при котором проведено оперативное родоразрешение, колебался от 24 до 39 недель: 24-30 недель - у 13,9% (7/54), 31-34 недель - у 31,5% (17/54), 35-37 недель - у 44,4% (24/54), 38-39 недель - у 11,1% (6/54). Все беременные поступали без регулярной родовой деятельности.
Осложнения беременности в момент поступления: преэклампсия легкой степени имела место у 16,7% (9/54), тяжелой степени - у 7,4% (4/54); про-грессирующая отслойка - у 16,7% (9/54); наличие старых ретроплацентарных гематом (УЗИ) величиной от 26,0x18,0 мм до 80,0x34,0 мм отмечено у 53,7% (29/54); антенатальная гибель плода в сроке 31 неделя отмечена в 1,9% (1/54) случаев; угроза прерывания на различных сроках беременности с кровяными выделениями до поступления отмечалась у 50,0% (27/54) женщин. Значимый состав экстрагенитальной патологии был представлен: сахарный диабет - у 5,6% (3/54); нарушения сердечного ритма - у 3,7% (2/54); хроническая артериальная гипертензия - у 7,4% (4/54); варикозная болезнь (включая область вульвы) - у 22,2% (12/54); хронический гепатит (В и С) - у 5,6% (3/54); бессимптомная бактериурия - у 5,6% (3/54).
В женской консультации первичный диагноз PAS был установлен у 70,4% (38/54) женщин в сроке беременности от 16 до 27 недель. У остальных 29,6% (16/54) диагноз верифицирован при ургент- ном поступлении в стационар: у 18,5% (10/54) в приемном отделении, а у 11,1% (6/54) - интраоперационно. Диагноз центрального ПП, подозрение на врастание в РНМ устанавливали на основании ультразвукового исследования (УЗИ) (доплеровское исследование). УЗИ проведено всем пациенткам. Критериями постановки диагноза при УЗИ были: плацентарные лакуны, гипертрофированные крупнокалиберные сосуды в области рубца на матке и в подскладочном пространстве, исчезновение гипоэхогенной зоны между плацентой и миометрием нижнего сегмента матки (НСМ), исчезновение очевидной границы между мочевым пузырем и стенкой матки. МРТ-исследование проведено 38,9% (21/54) пациенток.
В плановом порядке оперировано 63,0% (34/54) пациенток, в экстренном - 37,0% (20/54). Основанием для проведения экстренного вмешательства во всех случаях была прогрессирующая отслойка плаценты. В сроке 24-30 недель оперировано 13,0% (7/54) женщин в экстренном порядке. В сроке 31-34 недели - 31,5% (17/54) женщин, из них в плановом порядке - 16,7% (9/54), в экстренном - 14,8% (8/54). В 35-37 недель оперированы 42,6% (23/54) пациенток в плановом и 1,9% (1/54) в экстренном порядке. В 38-39 недель - 3,7% (2/54) беременных в плановом и 7,4% (4/54) в экс-тренном. Таким образом, основной массив плановых операций проведен в сроках 31-37 недель, а экстренных - в 24-30 и 38-39 недель.
Во время операции использовали кровесберегающие хирургические методы: перевязка 3 пар сосудов матки - 7 (13%), перевязка внутренних подвздошных артерий - 5 (9,3%), временное клеммирование общих подвздошных артерий - 11 (20,4%), временное клеммирование абдоминальной аорты - 1 (1,9%), комплексный компрессионный гемостаз - 30 (55.6%)
Комплексный компрессионный гемостаз выполнен у 55,6% (30/54) женщин. Метод Шмакова Р.Г., Чупрынина В.Д. [3, 5] заключается в наложении турникетных жгутов билатерально на основание широких связок и шеечно-перешеечную область матки. В широких связках матки на уровне перешейка формируются «окна» слева и справа, через которые накладываются турникетные жгуты, после чего затягиваются и фиксируются двумя зажимами. Яичники отводятся латеральнее турникетов, таким образом, в петлю попадают маточная труба, мезосальпинкс, собственная связка яичника, за счет чего пережимаются трубные ветви и коммуниканты, связывающие яичниковую и маточную артерии. Через эти же окна вокруг шейки проводится 3-й турникет, фиксируется зажимом на уровне шейки матки.
Интраоперационное прямое временное клемми- рование общих подвздошных артерий (ВКОПА) применили у 20,4% (11/54) женщин совместно с сосудистым хирургом. Доступ к сосудам осуществляли традиционно.
Баллонную окклюзию подвздошных артерий не использовали из-за отсутствия технологического оснащения.
Перевязка внутренних подвздошных артерий проводилась путем вскрытия париетальной брюшины над ее начальным отделом, проведения под ней лигатуры, лигирования викрилом.
Перевязка трех пар магистральных сосудов матки осуществлялась традиционно: прошивание, лигирование викрилом области маточных сосудистых пучков на уровне внутреннего зева шейки матки, прошивание, лигирование викрилом области маточно-трубных углов и собственных связок яичников.
Окончательное решение относительно плана опе-рации и применения того или иного кровесбере-гающего пособия принимали интраоперационно. Критериями выбора были макроскопические маркеры глубины и распространенности ВП, признаки, предвещающие технические трудности проведения операции и большой объем кровопотери: степень и площадь гипертрофии сосудов в области передней стенки НСМ, степень истончения передней стенки НСМ и выраженность маточной грыжи, характер спаечного процесса между мочевым пузырем и НСМ.
Удаляемый материал: резецированные участки НСМ, плацента, матка после гистерэктомии, направлялись на гистологическое исследование. Во всех 54 случаях проводилось фото- и видеодокумен-тирование основных этапов операции.
Результаты
Статистические данные родовспоможения по г. Ташкенту за 2018-2020 гг. показывают: на фоне увеличения числа родившихся живыми (44 838 в 2018 г., 49 906 - в 2019 г. и 47 028 - в 2020 г.) отмечается рост частоты КС - 27,0% в 2018 г., 28,1% - в 2019 г. и 30,6% - в 2020 г. Частота гистерэктомии в эти годы оставалась стабильной, на уровне 0,2% (283 из 141 772 родов в сроке более 22 недель).
В ТГПЦ в вышеуказанные годы оперировано 0,7% (110/16881) женщин с ПП (все формы) из 16 881 поступивших при беременности более 22 недель. При этом без РНМ оперировано 0,1% (17/16 881) женщин, с РНМ - 0,6% (93/16 881), а с центральным ПП и РНМ - 0,3% (54/16 881). Как видно, частота ПП в популяции женщин с РНМ существенно превышала показатель среди пациенток без РНМ, в среднем в 6 раз. Надо обратить внимание, что в структуре гистерэктомии показатель PAS, начавший фигурировать в статистических отчетах ТГПЦ с 2018 г., резко возрастал на фоне пятикратного снижения показателя гипотонии матки (табл. 1). В настоящее время он является ведущим показанием к акушерской гистерэктомии в ТГПЦ, занимая более половины от числа всех гистерэктомий.
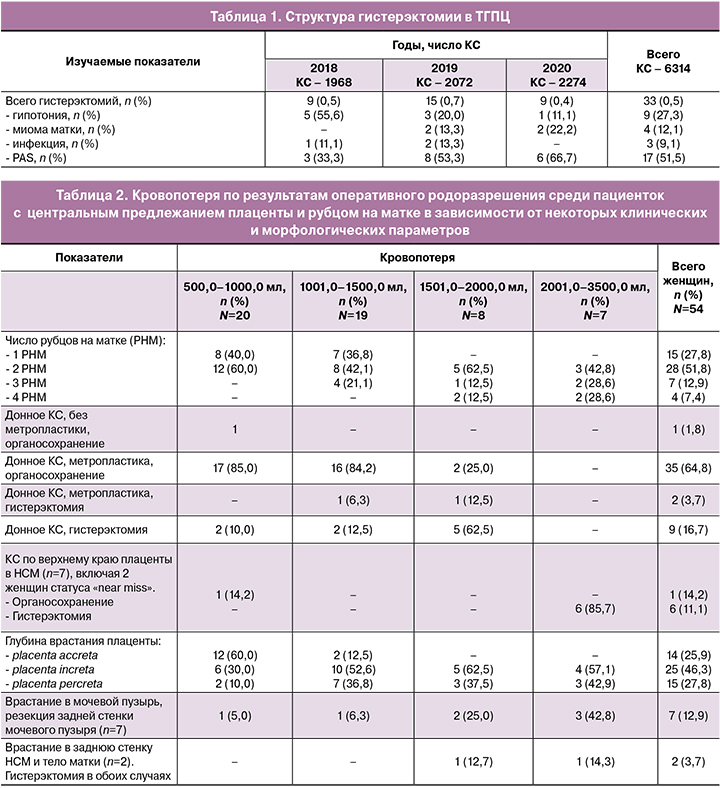
Кровопотеря является краеугольным камнем в оценке результатов оперативного родоразрешения беременных с PAS. В таблице 2 приводятся уровни кровопотери в зависимости от некоторых клинических и морфологических параметров. Как видно, из 39 женщин с уровнем кровопотери до 1500,0 мл 61,5% (24/39) имели 2 и более РНМ, а с кровопотерей от 1500,0 до 3500,0 мл все 15 женщин были с таким статусом. Второй важной особенностью, вытекающей из данной таблицы, является влияние способа проведения КС на уровень кровопотери. Как видно, донное КС ни в одном случае не сопровождалось кровопотерей более 2000,0 мл, в то время как из 7 женщин, которым проведено КС поперечным разрезом по верхнему краю предлежащей плаценты, у 6 кровопотеря была в диапазоне 2000,0-3500,0 мл. В число этих пациенток вошли 2 женщины статуса «near miss». У обеих во время операции в результате большой кровопотери в течение нескольких минут отмечалась остановка сердца. Быстрая успешная реанимация позволила сохранить жизнь женщинам и выписать их из ТГПЦ вместе с младенцами. Также необходимо обратить внимание на то, что из 7 женщин данной группы у 6 (включая 2 с «near miss») пришлось провести гистерэктомию (табл. 2). Только в 1 случае из 7 отмечалась кровопотеря не более 1000,0 мл. У данной пациентки не было глубокоинвазивного поражения миометрия, не было несостоятельности РНМ, и не потребовалась метропластика, несмотря на наличие центрального предлежания плаценты. Пренатальные результаты УЗИ, указывавшие на placenta increta, оказались ошибочны. Поэтому небольшой уровень кровопотери в данном случае мы связываем с относительно спокойным морфо-логическим субстратом патологии.
Отчетливое влияние на объем кровопотери оказывал фактор глубины врастания плаценты. При placenta accreta отмечали кровопотерю не более 1500,0 мл. Кровопотеря более 1500,0 мл наблюдалась только у пациенток с placenta increta и placenta percreta. Важным фактором, обуславливающим большую кровопотерю, перекликающимся с глубиной плацентарной деструкции, является поражение мочевого пузыря (табл. 2). Вынужденное вскрытие, резекция мочевого пузыря последовали в 13,0% (7/54) случаях; вскрытие мочевого пузыря без резекции его стенки - в 3,7% (2/54). Данные осложнения течения операции были связаны с очевидным врастанием плаценты в дно и заднюю стенку мочевого пузыря и тяжелым спаечным процессом. При этом сквозного повреждения слизистой оболочки мочевого пузыря в результате плацентарной инвазии не отмечалось.
У 3,7% (2/54) женщин с центральным ПП и РНМ интраоперационно (подтверждено гистологическим исследованием) отмечена placenta percreta с инвазией задней стенки НСМ и тела матки. Кровопотеря составила 2000,0 мл и 2400,0 мл. Оба случая завершились гистерэктомией (табл. 2).
Распределение уровней кровопотери в зависимости от хирургических способов редукции кровопотери показало следующие результаты (табл. 3). Как видно, перевязка трех пар магистральных сосудов матки, только в 1 случае из 7 сопровождалась кровопотерей не более 1000,0 мл. Это те самые 7 пациенток, у которых КС проводилось поперечным разрезом по верхнему краю предлежащей плаценты (табл. 2). Как отмечалось выше, у 1 из них не отмечалось глубокоинвазивного поражения, не было несостоятельности РНМ, и не потребовалась метропластика. Остальные 6 женщин дали кровопотерю в диапазоне 2000,0-3500,0 мл: минимальная кровопотеря среди них - 2000,0 мл была у 1 женщины, 2500,0-3000,0 мл - у 3, до 3500,0 мл - у 2.
Перевязка внутренних подвздошных артерий перед метропластикой и экстракцией плаценты также мало удовлетворяла нас (табл. 3). Из 5 женщин, среди которых проводился данный метод, кровопотеря составила: 1800,0 мл - у 2, 1900,0 мл - у 2 и 2400,0 мл - у 1.
ВКОПА использовалось у 12/54 женщин с наиболее сложным, макроскопически определяемым составом патологии, где отмечались крайние формы несостоятельности РНМ с формированием обширной маточной грыжи, выраженные формы гипертрофии сосудов в зоне РНМ, очевидные признаки врастания плаценты в заднюю стенку и дно мочевого пузыря. У 8 из 12 женщин кровопотеря не превышала 1,5 л, у 4 - 2,0 л. Длительность пережатия артериальных магистралей не превышало 35 минут.
Наиболее эффективным способом снижения кровопотери в нашем исследовании явился комплексный компрессионный гемостаз по Р.Г. Шмакову [5]. Он использовался у 55,6% (30/54) женщин. Как видно, кровопотеря во всех 30 случаях не превышала 1500,0 мл: медиана - 1200,0 мл, минимальная кровопотеря 700,0 мл, максимальная 1500,0 мл в единичном случае.
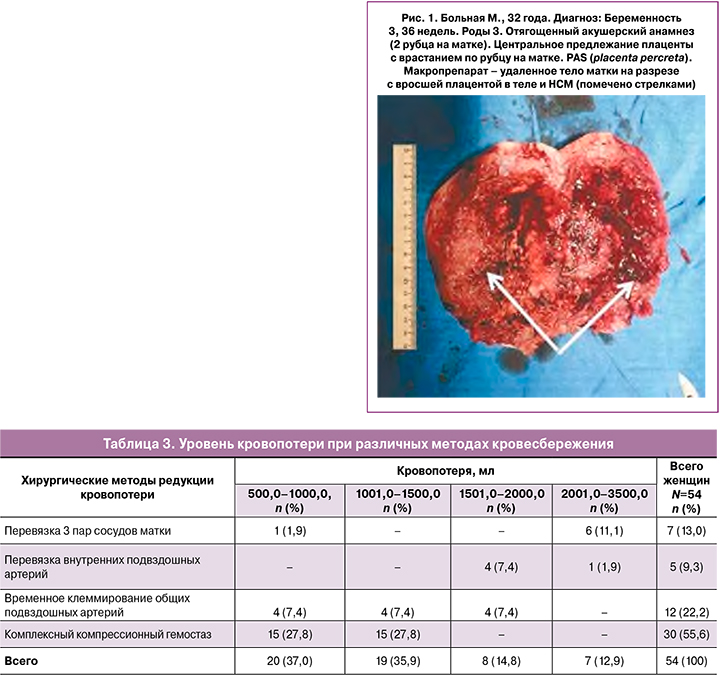
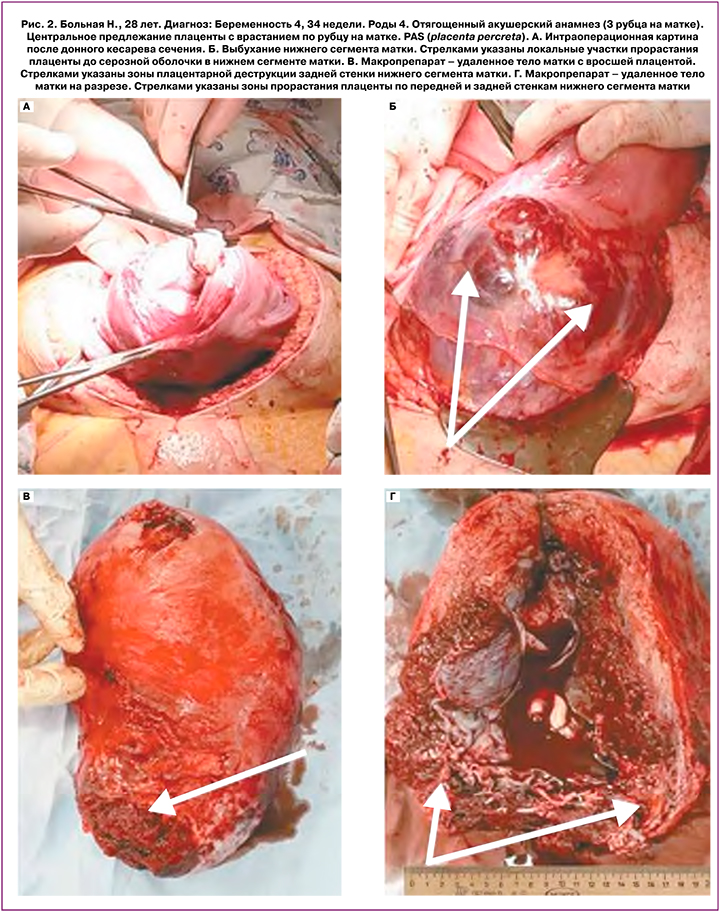
Гистерэктомия проведена у 31,5% (17/54) женщин. Из этого числа у 11,8% (2/17), помимо ВПРНМ (как было сказано выше), отмечалось глубокоинвазивное (placenta increta, placenta percreta) поражение задней стенки нижнего сегмента и тела матки (рис. 1, 2). У одной из них КС проводилось по верхнему краю предлежащей плаценты, и данная форма врастания была установлена при попытке проведения метропластики. У другой — обширное поражение задней стенки НСМ и тела матки (по передней и задней стенке) установлено при донном КС. Пренатальное экспертное УЗИ не выявило данных форм инвазии плаценты. Интраоперационно уровень и площадь плацентарной инвазии были настолько очевидны, что гистерэктомия последовала без попыток проведения метропластики. Наибольшее влияние на необходимость проведения гистерэктомии оказывал фактор интенсивного кровотечения в результате КС по верхнему краю предлежащей плаценты: у 6 из 7 женщин (табл. 2). В общей сложности после донного КС, без попыток проведения метропластики, гистерэктомия проведена у 9 из 17 женщин, а после таких попыток — у 2 (табл. 2). Показанием к гистерэктомии была значительная кровопотеря, наступившая до начала проведения операции у пациенток, поступавших в экстренном порядке (20 женщин из 54). Кровопотеря до момента проведения операции среди указанных 20 пациенток колебалась от 300,0 до 800,0 мл, в среднем - 532,0±210,0 мл, медиана - 450,0 мл.
У части больных в послеоперационном периоде диагностированы осложнения: эндометрит - у 3,7% (2/54), инфекция мочевых путей - у 7,4% (4/54), формирование гематом под пузырно-маточной складкой - у 5,6% (3/54). Отсутствовали: релапа-ротомия, тромбоэмболические осложнения, случаи материнской смертности.
Перинатальные потери составили 7,4% (4/54), включая антенатальную гибель плода в сроке 31 неделя беременности - 1,9% (1/54), постнатальную - вследствие глубокой недоношенности - 5,6% (3/54).
Обсуждение
Вероятно, в том, что РНМ после КС провоцирует увеличение частоты ПП, уже мало кто сомневается. Как показано в нашем исследовании, это происходит примерно в 6 раз чаще, чем в общей популяции. Увеличение частоты ВП в область РНМ объяснимо, и генез понятен. Однако возникновение глубокой пла-центарной инвазии в области, свободные от рубцовых изменений, возникающие параллельно с ВПРМ, — в одном и том же клиническом случае, не укладывается в классическую модель патофизиологии PAS. С тех пор, как Beard J. [10] еще в начале прошлого века высказал предположение о сходстве поведения злокачественных опухолей и трофобласта, в научной литературе периодически появлялись работы на данную тему. Новый импульс она получила в связи с современным состоянием проблемы ВПРМ. В последнее время большое значение предается балансу между генами, регулирующими активность и супрессию хориона [11, 12]. В данных работах существенную роль отводят так называемому KiSS-гену, открытому в 1996 г. в клетках некоторых злокачественных опухолей. Однако относительно недавно установлена его роль в супрессии рака различной локализации. Вместе с тем показано активное участие KiSS-гена в инвазии трофобласта в эндометрий [13], а самая высокая его концентрация в человеческом организме выявлена в плаценте. Последние сообщения показывают: повышенная экспрессия EGFR (epidermal growth factor receptor) синцитиотрофобластом при врастании плаценты позволяет предположить, что аномальная ворсинчатая адгезия развивается в результате ненор-мальной экспрессии факторов роста, ангиогенеза и инвазии в популяциях трофобластов. Авторы приходят к выводу о том, что сосудисто-эндотелиальный фактор роста (VEGF) и sFLT-1 играют ключевую роль в процессе патологического программирования вневорсинчатого трофобласта в направлении повы-шения инвазивности при PAS [14]. Однако остается открытым вопрос: это результат определенной гене-тической мутации в популяции или данный процесс может быть индуцирован особенностями РНМ. По данным настоящего исследования, глубокая инвазия врастания плаценты в участки матки, свободные от рубцовых изменений, встречается примерно у 1:27 пациенток с центральным предлежанием на фоне РНМ.
В одной из последних работ [15] относительно наиболее сложного контингента PAS — «near miss» показано, что инвазия плаценты выявлялась (на УЗИ или МРТ) до родов только в 54,4% (95% ДИ 41,0-67,5) случаев «near miss». Авторы отмечают, что в 22,1% (95% ДИ 9,7-37,9) случаев PAS, диагностированных пренатально, степень тяжести врастания, выявленная интраоперационно, была выше, чем сообщалось до операции. Таким образом, тезис о том, что до сих пор нет убедительных данных, может ли пренатальная визуализация идентифицировать случаи с самым высоким риском PAS, при которых ожидаем неблагоприятный материнский исход, находит подтверждение и в наших исследованиях. Если случаи «near miss» в исследованиях Palacios-Jaraquemada J.M. [6] в основном были связаны с поражением задней стенки мочевого пузыря, то в наших наблюдениях - это, вероятно, следует связывать с неоправданными попытками проведения КС по верхнему краю предлежащей плаценты. В свете вышеуказанных работ, а также принимая во внимание наш собственный опыт, следует признать, что такой подход (проведение КС по верхнему краю предлежащей плаценты) может быть оправдан, когда параллельно осуществляется эндоваскулярный блок на уровне общих подвздошных артерий [16] (так называемая методика «Triple-P»). На наш взгляд, при отсутствии баллонной окклюзии (в нарушение вышеназванной методики), попытки проведения КС по верхнему краю плаценты (наблюдаемые в отдельных учреждениях) при наличии признаков врастания плаценты является ошибкой, что лишний раз показывают результаты нашего исследования.
Мы стали отмечать участившиеся случаи врастания плаценты не только в область рубца на передней стенке НСМ, но и в область задней стенки НСМ и тело матки — свободные от рубцовых изменений. Почему так происходит? Пока это открытый вопрос. Мы лишь предполагаем, что это происходит в результате активации инвазивных свойств плаценты при ее центральном предлежании. В представленных нами 2 случаях врастания плаценты в заднюю стенку нижнего сегмента матки и тело матки пренатальная диагностика была ошибочной. В протоколах УЗИ не описаны признаки врастания плаценты вне зоны рубца. Вероятно, это следует связывать с недостатком опыта таких наблюдений у специалистов ультразвуковой диагностики. У обеих пациенток операция протекала по одной и той же схеме: донное КС, клеммирование общих подвздошных артерий. Несмотря на своевременно констатированные макроскопические признаки глубокоинвазивного врастания плаценты в области задней стенки НСМ и тела матки (по передней и задней стенке), хирурги предпринимали попытки провести органосохраняющую операцию. Однако малоуправляемое кровотечение в конце концов заставило прибегнуть к гистерэктомии. Ничем другим, кроме попыток органосохранения, при очевидной обширной плацентарной деструкции, потерянные объемы крови в изученных 2 клинических эпизодах нам объяснить не удалось. Многие специалисты, задаваясь вопросом возникновения массивной кровопотери, несмотря на устанавливаемый блок на уровне общих подвздошных артерий тем или иным методом (как и в наших случаях), указывают на то, что даже в этих условиях действуют обходные артериальные коллатерали. Важнейшими из них, как было установлено в исследованиях Palacios-Jaraquemada J.M. et al. (2019) [6], является бассейн нижнебрыжеечной артерии, которая во время беременности по диаметру основного сосуда увеличивается в 2-3 раза.
В данном обсуждении, вероятно, необходимо кос-нуться выжидательной тактики - оставление плаценты in situ. Надо отметить - в настоящее время выжидательная тактика не имеет прямых рекомен-даций международных организаций, контролирующих данную проблему (ACOG, FIGO). Главной причиной этого является тревожный и хорошо известный спектр послеоперационных осложнений [2, 18, 19].
Гистерэктомия в большинстве исследований, включая международные экспертные группы, пози-ционируется как вполне оправданный этап завершения операции при PAS. Вместе с тем к вопросу сохранения матки некоторые акушерские школы, вероятно, небезосновательно подходят весьма трепетно, пытаясь достичь высоких показателей. Используя ангиографические пособия, ряд российских исследователей добиваются хороших результатов органосохраняющих операций [5, 8], несмотря на крайне тяжелые по глубине и площади формы PAS. На наш взгляд, современная акушерская наука находится в эпицентре данной дискуссии, а на результатах исследований сказывается не только технологическая оснащенность, но и региональные особенности.
Заключение
Таким образом, как показали наши исследования, причинами случаев «near miss» при PAS могут быть недостаточная пренатальная диагностика тяжести патологии и применение на этом фоне неоправданных хирургических методик. При выявлении признаков глубокого инвазивного повреждения задней стенки НСМ или тела матки (пренатально или интраоперационно) высока вероятность гистер-эктомии. При развитии неконтролируемого кро-вотечения гистерэктомия является оправданным объемом завершения операции.
Базируясь на собственном опыте работы, мы можем предположить, что метод комплексного компрессионного гемостаза, предложенный Шмаковым Р.Г. и Чупрыниным В.Д., в ближайшем будущем станет базовым при оперативном родоразрешении пациенток с PAS. Такая точка зрения сформировалась в результате достаточно продолжительной практической работы с данным контингентом беременных. В методике есть лишь одно уязвимое место, т.е. ограничение ее использования - это случаи серьезных осложнений, связанных с врастанием плаценты в мочевой пузырь, когда его диссекция (для обеспечения наложения «удавки» на начальные отделы шейки матки) может быть связана с дебютом неуправляемого кровотечения. Подробное рассмотрение данного вопроса - это отдельная тема. Следует отметить, что случаи тяжелого врастания плаценты в мочевой пузырь редки, поэтому данный метод может занять основную нишу кровесберегающих технологий при PAS.



