За последние 10–15 лет во многих странах мира, в том числе и в России, отмечен рост инфекций влагалища, занимающих ведущее место в структуре акушерско-гинекологических заболеваний [1]. Особенностью урогенитальной инфекции в современных условиях является увеличение заболеваний, протекающих с участием микроорганизмов, входящих в состав нормальной микрофлоры влагалища [2]. Между вагинальной средой и микрофлорой влагалища существуют сложные взаимоотношения. Эпителий стенок влагалища и влагалищной части шейки матки не содержит желез. Клетки базального слоя эпителия делятся, созревают, обогащаются гликогеном и слущиваются в просвет влагалища. Вагинальный секрет имеет определенную кислотность, которую обеспечивают лактобактерии влагалища [2, 3]. Это создает условия, препятствующие росту и размножению анаэробных микроорганизмов. Наличие обильных выделений из влагалища – одна из наиболее частых жалоб пациенток. В 22–50% наблюдений патологические бели из влагалища являются симптомами бактериального вагиноза (БВ).
БВ – нарушение микроэкологии влагалища, которое характеризуется ростом облигатных или факультативных анаэробных бактерий: Gardnerella vaginalis, Prevotella spp., Mabiluncus spp., Veilonella spp., Bacteroides spp., Peptococcus spp. при возможном участии Mycoplasma spp. и Ureaplasma spp. Это приводит к угнетению роста и жизнедеятельности влагалищных лактобактерий [4, 5]. Анаэробные бактерии синтезируют ферменты – аминопептидазы, которые расщепляют пептиды до аминокислот, а затем до аминов. С этим связан характерный для БВ «рыбный» запах. Кроме того, амины способствуют еще большему сдвигу pH в сторону щелочной среды. Таким образом, создаются условия для прикрепления присутствующих во влагалище в большом количестве бактерий, в основном G. Vaginalis, к эпителиальным клеткам влагалища, которые слущиваются с поверхности слизистой оболочки. Зрелые эпителиальные клетки с адгезированными на них микроорганизмами, ассоциированными с БВ (Gardnerella vaginalis, Prevotella spp., Mabiluncus spp., грам-положительные кокки), носят название «ключевые» клетки [6].
Нарушение микробиоценоза влагалища – БВ имеет широкое распространение у женщин репродуктивного возраста (до 84%), среди беременных его наблюдают в 10–27% [4]. Клинические проявления и осложнения заболевания связаны с бактериальной обсемененностью влагалища. При этом клинические и лабораторные признаки воспаления отсутствуют.
Диагноз БВ может быть установлен на основании наличия критериев Амселя [7]. К этим критериям относятся: патологические выделения (бели) из влагалища – белые или сероватые гомогенные выделения, покрывающие всю слизистую влагалища; pH>4,5 – с помощью полосок для pH-метрии; положительный аминотест – появление «рыбного» запаха при смешивании влагалищного отделяемого с 10% KOH; обнаружение «ключевых» клеток, полимикробная картина мазка. В диагностике БВ необходимым является определение видового состава микрофлоры влагалища. Gardnerella vaginalis – самый известный участник из числа микроорганизмов, ассоциированных с БВ [2, 8].
 Клиническое значение проблемы обусловлено повышением риска (до 7,1%) преждевременных родов (ПР) у этих больных, а также возможностью развития хориоамнионита (ХА), послеродового эндометрита (ПЭ), воспалительных процессов половых органов, гнойно-септических осложнений у матери и ребенка в послеродовом периоде, рождения детей с низким весом, что влияет на частоту акушерской патологии и неонатальной заболеваемости [9].
Клиническое значение проблемы обусловлено повышением риска (до 7,1%) преждевременных родов (ПР) у этих больных, а также возможностью развития хориоамнионита (ХА), послеродового эндометрита (ПЭ), воспалительных процессов половых органов, гнойно-септических осложнений у матери и ребенка в послеродовом периоде, рождения детей с низким весом, что влияет на частоту акушерской патологии и неонатальной заболеваемости [9].
Терапия БВ во время беременности является сложной проблемой из-за возможного неблагоприятного воздействия лекарственных препаратов на плод, особенно в ранние гестационные сроки, когда решаются вопросы наиболее эффективной профилактики осложнений беременности и родов [4, 9].
Лечение БВ состоит из двух этапов [10–14]. На первом этапе назначается антибактериальная терапия. Средства 1-й линии при этом – метронидазол и клиндамицин. Однако в 75–85% наблюдений эффект этих препаратов носит краткосрочный характер. Эффективность лечения в отношении устранения симптомов заболевания и восстановления нормальной вагинальной флоры составляет 85%. У 75–80% пролеченных в течение 8 месяцев возможны рецидивы. Большинство лекарственных средств с противомикробным действием имеют свои достоинства и недостатки, такие как узкая терапевтическая активность и угнетение лактобактерий. После проведения антибактериальной терапии возникает резистентность к антибиотикам. Кроме того, наблюдается рост лактобактерий, не продуцирующих перекиси. На втором этапе лечения идет восстановление микроценоза влагалища путем применения биологических препаратов (ацилакт, лактобактерии, бифидобактерии и др.). Нельзя не отметить, что большинство препаратов содержит лактобактерии кишечного происхождения, которые не способны хорошо приживаться из-за низких адгезивных свойств к вагинальным эпителиоцитам. Кроме того, бактерии находятся в биологически неактивном состоянии и не сразу проявляют свою активность.
Высокая частота рецидивов БВ, возможные осложнения во время беременности и в послеродовом периоде диктуют необходимость разработки новых подходов к терапии этого заболевания. Трудности диагностики смешанных инфекций и адекватности выбора препарата определяют необходимость патогенетических подходов к лечению.
Цель исследования: оценка эффективности и безопасности применения препарата мульти-гин актигель для профилактики и в составе терапии бактериального вагиноза у беременных перед родами.
Материал и методы исследования
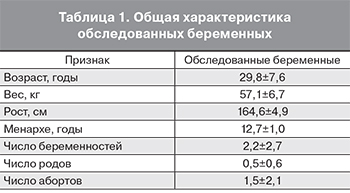
Под наблюдением находились 80 беременных, госпитализированных в акушерское обсервационное отделение МОНИИАГ. Их общая характеристика представлена в табл. 1.
Все беременные были разделены на 2 группы. В 1-ю группу вошли 50 беременных с симптомами угрозы преждевременных родов в гестационные сроки 35–36 недель. При обследовании у них был выявлен бактериальный вагиноз. Возраст обследованных составил от 18 до 39 лет. Для лечения бактериального вагиноза все беременные 1-й группы получали мульти-гин актигель. При проведении исследования строго соблюдались критерии включения/исключения.
Критерии включения в исследование:
- Срок беременности 35–36 недель;
- Диагноз: Угроза преждевременных родов;
- Возраст от 18 до 39 лет;
- Диагноз: Бактериальный вагиноз;
- Информированное согласие на участие в исследовании после полного разъяснения протокола;
- Соблюдение указаний врача.
Критерии исключения:
- Кольпиты установленной специфической этиологии (грибковой, хламидийной, уреаплазменной, трихомонадной, гонорейной);
- Кольпиты, вызванные неспецифической флорой (стафилококк, кишечная палочка, стрептококк и др., в титрах 10 х 6 КОЕ и более);
- Прием антибактериальных препаратов менее чем за 3 месяца до начала настоящего лечения;
- Индивидуальная непереносимость препарата.
Беременные 1-й группы были разделены на 2 подгруппы. 1а подгруппа – 35 беременных, у которых присутствовали все симптомы, характеризующие бактериальный вагиноз: выделения из влагалища с «рыбным» запахом, зуд, боль, жжение, гиперемия, лабораторные и микроскопические характеристики, результаты посевов. 1б подгруппа – 15 беременных, у которых диагноз БВ был установлен на основании данных лабораторного обследования.
В группу сравнения вошли 30 беременных, у которых также был обнаружен БВ, но они не соответствовали критериям включения/исключения: во время беременности у них неоднократно диагностировали кольпиты специфической этиологии (кандидозные, уреаплазменные), им проводилась антибактериальная и противогрибковая терапия. Срок гестации в этой группе также соответствовал 35–36 неделям беременности. Для лечения бактериального вагиноза им назначались пробиотики. Ранее все беременные этой группы получали метронидазол или клиндамицин. По возрасту и паритету беременные обеих групп не имели существенных различий.
Для постановки диагноза и оценки эффективности лечения всем пациенткам были проведены следующие обследования:
- клиническое: жалобы, анамнез, общий осмотр, влагалищное исследование;
- лабораторное: микроскопия мазка на степень чистоты влагалищного содержимого, окрашенного по Граму, бактериологическое, вирусологическое, исследование влагалищных выделений с определением качественных и количественных характеристик микробных колоний, Оценивали критерии Амселя, включая pH-метрию влагалищного секрета и амино-тест. Обследование проводилось дважды: до начала лечения и после завершения курса терапии.
Пациентки 1-й группы получали препарат мульти-гин актигель на основе 2QR-комплекса. 2QR – это комплекс биоактивных полисахаридов, полученных из мякоти алоэ способом молекулярной фильтрации. 2QR-комплекс позволяет нейтрализовать вредные микробы путем физического воздействия. Он блокирует адгезины на клеточной поверхности патогенных микробов. 2QR-комплекс – это сетчатый полимер галактоарабинана и полиглюкуроновой кислоты. Вспомогательными компонентами являются глюкоза, галактоза, ксилоза и глюкуроновая кислота. Функция 2QR-комплекса заключается во взаимодействии полисахаридов и адгезинов в профилактике бактериальных инфекций. Заряженные 2QR-молекулы обладают высокой способностью связываться с патогенными компанентами – адгезинами – на поверхности клетки. Тем самым блокируется связывание микроорганизмов с клеточными рецепторами организма, которые обладают сильной антимикробной активностью, контролируют натуральную микрофлору и предотвращают бактериальные проблемы, то есть развитие инфекции на ранней стадии. В ходе терапии БВ все пациентки получали препарат мульти-гин актигель. Препарат назначался для обработки влагалища и вульвы 2 раза в сутки через 12 часов в течение 5 дней. После нанесения геля у пациенток возникало легкое пощипывание, которое исчезало через 5–10 минут. По показаниям (данные клинико-лабораторного обследования) через 2 недели терапию повторяли.
Пробиотики, назначенные пациенткам 2-й группы, были препаратами для перорального приема, содержащими пробиотические лактобациллы и/или бифидобациллы, что способствует увеличению числа бактерий во влагалище и нормализует микрофлору.
Результаты исследования
Первую группу составили 33 первородящих и 17 повторнородящих женщин. У 17 беременных этой группы БВ был диагностирован еще на этапе наблюдения в женской консультации. Им проводилось лечение вагинормом в начале II триместра беременности. У 5 беременных БВ имел рецидивирующее течение, в связи с чем, терапию повторяли трижды. В условиях стационара все беременные получали терапию, направленную на пролонгирование беременности. Кроме того, у 12 беременных была диагностирована фетоплацентарная недостаточность (ФПН), задержка внутриутробного роста 1–2-й степени, а у 43 беременных по данным клинического анализа крови зафиксировано снижение уровня гемоглобина до 100–105 г/л, что соответствовало железодефицитной анемии 1-й степени.
Во 2-й группе 19 пациенток были первородящими, 11 – повторнородящими. У 13 беременных было неосложненное течение беременности, у 7 беременность осложнилась угрозой прерывания, у 8 диагностирована ФПН, у двоих выявлен гестационный сахарный диабет. У 14 беременных 2-й группы для лечения БВ применялись метронидазол, клиндамицин. На II этапе назначались пробиотики (лактобактерин, ацилакт, гинофорт и др.). Во всех наблюдениях имели место рецидивы БВ.
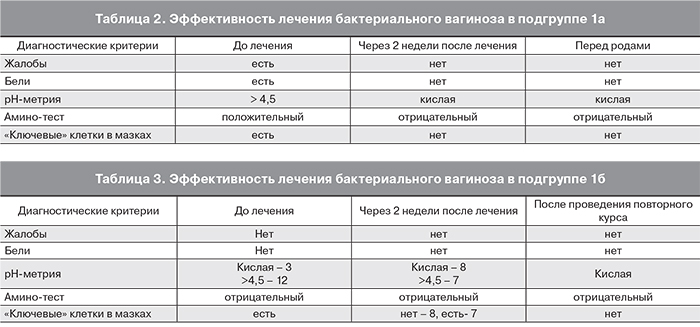
У всех пациенток 1-й группы диагноз БВ был подтвержден на основании низкой концентрации лактобактерий (менее 50%), повышенного содержания анаэробов (более 10×4 КОЕ/мл). Кроме того, отмечены положительные критерии Амселя в обеих подгруппах 1-й группы (табл. 2, 3). Через 2 недели после лечения проведено повторное обследование. Лишь у 7 из 50 беременных сохранялись симптомы БВ, в связи с чем проведен повторный курс терапии. После повторного курса лечения признаки БВ были купированы во всех наблюдениях (табл. 2, 3).
Все беременные 1-й группы были родоразрешены при доношенной беременности: 47 через естественные родовые пути, троим предпринято абдоминальное родоразрешение в связи с аномалиями сократительной деятельности матки. Дети родились в удовлетворительном состоянии и в проведении этапного лечения не нуждались. У родильниц послеродовых инфекционно-воспалительных осложнений не было.
Во 2-й группе повторное обследование проводилось через 7 и 14 дней после лечения. Через 7 дней обследование проведено у 30 беременных. Через 14 дней – у 21 пациентки, так как 9 беременных к сроку повторного обследования были родоразрешены: пятерым произведено повторное кесарево сечение по поводу несостоятельного рубца на матке, у 4 пациенток произошли преждевременные роды.
При первом контрольном обследовании ни у одной пациентки не произошло полной нормализации микробиоценоза влагалища. Однако у всех обследованных женщин количество лактобактерий увеличилось на 70–80%, снизилось количество «ключевых» клеток. У 21 беременной количество аэробов/анаэробов снизилось до 10×3–4 КОЕ/мл, у 9 – осталось выше нормы.
Через 14 дней от начала лечения у 16 беременных из 21 было констатировано состояние нормобиоценоза влагалища. У одной при высоком титре лактобактерий (более 80%) обнаружены Mycoplasma spp. и Candida albicans, у 1 – Ureaplasma spp., однако количество этих микроорганизмов не превышало 10×4 КОЕ/мл.
10 пациенток 2-й группы были родоразрешены путем операции кесарева сечения: 8 произведено повторное кесарево сечение в связи с наличием несостоятельного рубца на матке, двум – первое кесарево сечение в связи с декомпенсированной ФПН. Произошло 4 преждевременных родов в 36 недель беременности. У 20 пациенток роды самопроизвольные, 11 роженицам в связи с угрозой разрыва промежности произведена эпизиотомия. При осмотре родовых путей у 5 родильниц обнаружены разрывы шейки матки I степени. Глубоких разрывов влагалища не было. Ранний послеродовой и послеоперационный периоды у 28 родильниц протекали без осложнений. У 2 родильниц после кесарева сечения была диагностирована субинволюция матки.
У 28 новорожденных из 30 не было проявлений внутриутробной инфекции (ВУИ). У 2 детей, родившихся от матерей с неоднократно рецидивирующим БВ, диагностирована ВУИ: внутриутробная пневмония – 1, везикулез – 1. Дети переведены на этапное лечение. После проведенного лечения выписаны в удовлетворительном состоянии.
Обсуждение результатов
Результаты проведенного исследования свидетельствуют о высокой эффективности мульти-гин актигель в терапии БВ и профилактики акушерских осложнений. На фоне назначения препарата снижалась степень выраженности жалоб беременных (сухость, болезненность во влагалище, зуд, жжение, патологические выделения). При нанесении геля во влагалище он сразу создает оптимальный уровень pH, что подтверждено проведенным исследованием. В группе беременных с угрозой преждевременных родов и БВ, которым назначался мульти-гин актигель, все беременные были родоразрешены в срок. В группе сравнения, беременные которой получали пробиотики, а ранее были пролечены метронидазолом и клиндамицином, в 4 наблюдениях произошли преждевременные роды.
Основным компонентом препарата мульти-гин актигель является 2QR-комплекс, который состоит из отрицательно заряженного высокомолекулярного полисахаридного комплекса, полученного из алоэ лекарственного. Данные полисахариды оказывают мощное антиадгезивное действие. Предотвращение адгезии G. vaginalis сможет препятствовать возникновению инфекционного процесса и образованию биопленки. Образование биопленки, которая была обнаружена при проведении микроскопии биоптатов влагалища женщин с БВ, является важным фактором вирулентности, поскольку ее наличие связано с повышенной устойчивостью к антибиотикам [12].
Таким образом, действие препарата мульти-гин актигель заключается в блокировании адгезии патогенных бактерий, нормализации pH влагалища, оптимизации нормальной микрофлоры влагалища, а также в поддержании естественной системы восстановления тканей. С другими лекарственными средствами препарат не взаимодействует.
Поскольку мульти-гин актигель основан не на агрессивных химических или токсических веществах, не влияет на полезные бактерии, не оказывает негативного влияния на клетки организма, не имеет побочных эффектов, безвреден и безопасен, он соответствует всем требованиям, предъявляемым к лекарственным средствам, назначаемым беременным.
Важным следует считать и то, что врач может рекомендовать беременной нетоксичный гель, отпускаемый без рецепта, для самостоятельного применения пациенткой с целью профилактики рецидива заболевания, не опасаясь передозировки.
Заключение
Таким образом, препарат мульти-гин актигель – эффективное средство лечения БВ и профилактики его рецидивов. При этом он является безопасным для плода, что позволяет назначать его беременным в ранние гестационные сроки, когда решаются вопросы наиболее эффективной профилактики осложнений беременности и родов.



