Исторически сложилось, что в начале развития вспомогательных репродуктивных технологий (ВРТ) в большинстве программ ВРТ проводили перенос в полость матки нескольких эмбрионов, в основном с целью повышения частоты наступления беременности (ЧНБ), а также в связи с отсутствием возможности криоконсервации эмбрионов. Однако за последние десятилетия технологии репродуктивной медицины в развитых странах стремительно развивались, и сегодня криоконсервация эмбрионов является рутинной практикой, а ЧНБ в расчете на перенос эмбриона выше, чем когда-либо ранее.
На современном этапе развития ВРТ значительное внимание уделяется развитию селективного переноса одного эмбриона (elective Single Embryo Transfer, eSET) для профилактики многоплодной беременности и связанных с многоплодием осложнений для матери и плода. В Российской Федерации первые данные о технологии eSET были опубликованы в 2001 г. По данным регистра ООО «Российская ассоциация репродукции человека» (РАРЧ), частота eSET составила 0,8% для циклов экстракорпорального оплодотворения (ЭКО) и 0,4% – для циклов интрацитоплазматической инъекции сперматозоида в ооцит (ИКСИ), селективного переноса 2 эмбрионов – 8,6% для ЭКО и 2,7% для ИКСИ соответственно (регистр ВРТ РАРЧ, 2001).
Основным препятствием для широкого внедрения технологии eSET служила гипотеза о значительном снижении эффективности программ ВРТ; однако на сегодняшний день имеется большое число исследований, опровергающих данную гипотезу. Стоит также учитывать, что многоплодная беременность ассоциирована с повышенным риском различных перинатальных и постнатальных осложнений [1] и все еще остается осложнением циклов ВРТ [2]. Многоплодная беременность повышает риск невынашивания беременности, преждевременных родов, эктопической беременности, больших акушерских синдромов, осложнений послеродового периода [3]. В свою очередь, все перечисленные акушерские состояния негативно влияют на здоровье детей не только в неонатальном периоде, но и в долгосрочной перспективе. Поэтому широкое использование технологии eSET выходит за рамки профилактики многоплодной беременности. При этом, согласно данным РАРЧ, частота многоплодных родов в результате программ ЭКО и ИКСИ и программ переноса размороженных эмбрионов остается достаточно высокой, составив в 2021 г. 10,1 и 8,6% соответственно (регистр ВРТ РАРЧ, 2021).
Учитывая сказанное выше, целью настоящего исследования явилось изучение подходов к тактике eSET в полость матки в программах ВРТ и законодательной базы различных стран мира в отношении данного вопроса.
История внедрения технологии селективного переноса одного эмбриона
Одно из первых исследований, результаты которого поставили под сомнение необходимость переноса большого числа эмбрионов, опубликовано в 1998 г. в журнале New England Journal of Medicine группой авторов из Великобритании. В данной статье авторы проанализировали результаты 44 236 циклов ВРТ у 25 240 женщин в Великобритании за период с 1991 по 1994 гг. [4]. Результаты данного исследования актуальны и сегодня: основными предикторами неудачных циклов ВРТ были: поздний репродуктивный возраст пациенток, длительное бесплодие и отсутствие родов в анамнезе, неудачи ВРТ в анамнезе и воспалительные заболевания органов малого таза. Шансы клинической беременности увеличивались вместе с увеличением числа ооцитов и зигот. Авторы установили, что при наличии достаточного числа эмбрионов перенос 4 эмбрионов не увеличивает ЧНБ по сравнению с переносом 2 эмбрионов, однако частота многоплодной беременности увеличивается в 1,6 раза. Был сделан вывод о том, что независимо от возраста пациентки и числа эмбрионов целесообразно переносить не более 2 эмбрионов в полость матки и осуществлять криоконсервацию оставшихся эмбрионов.
Сравнение эффективности программ вспомогательных репродуктивных технологий при переносе одного или двух эмбрионов
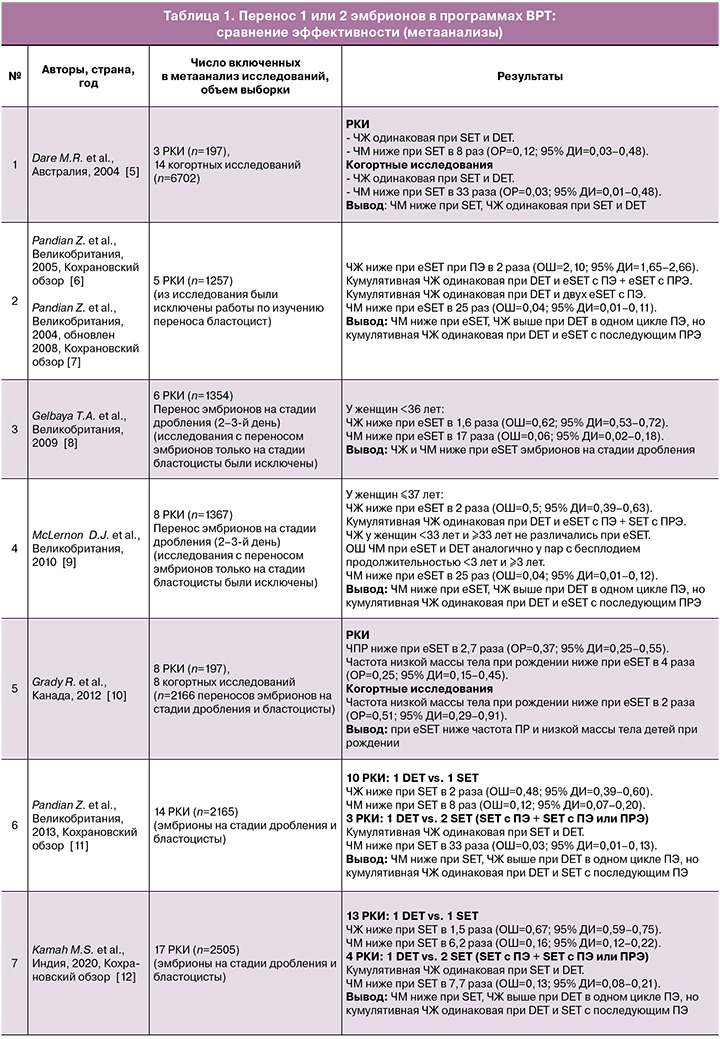
В таблице 1 приведены результаты исследований, сравнивающих эффективность программ ВРТ при переносе 1 эмбриона и 2 эмбрионов
Можно сделать следующий вывод по проведенным метаанализам. В более ранних исследованиях с включением небольшого числа исследований в метаанализы было показано, что перенос одного эмбриона связан с более низкой частотой живорождения (ЧЖ), чем перенос 2 эмбрионов. При этом не было выявлено значимой разницы в кумулятивной частоте живорождения при сравнении однократного переноса 2 эмбрионов и последовательного переноса одного эмбриона (нативного или размороженного) в разных циклах ВРТ. Также перенос 1 эмбриона был связан с гораздо более низкой частотой многоплодной беременности. В более поздних метаанализах с включением большего числа исследований было показано, что в целом при последовательном переносе одного эмбриона в разных циклах ВРТ частота живорождения выше, частота многоплодия и акушерских осложнений ниже, особенно у женщин раннего репродуктивного возраста и при переносе эмбриона на стадии бластоцисты. Одновременный перенос эмбриона хорошего и эмбриона плохого качества также не улучшал исходы программ ВРТ по сравнению с переносом одного эмбриона хорошего качества. Таким образом, практика повторного переноса одного эмбриона может свести к минимуму риск многоплодной беременности у пациенток программ ВРТ без существенного снижения вероятности рождения живого ребенка. При этом следует отметить, что большинство имеющихся в настоящее время данных касается молодых женщин с хорошим прогнозом.


Далее был проведен анализ с более детальным рассмотрением отдельных наиболее крупных рандомизированных контролируемых исследований (РКИ) и исследований с проведением клинико-экономического анализа (КЭА), в которых проводилось сравнение результатов программ ВРТ при переносе 1 или 2 эмбрионов (табл. 2).
Проанализировав данные исследования, можно сделать следующие выводы.
Отмечено снижение ЧНБ/ЧЖ на 1 цикл переноса эмбриона при еSET, однако кумулятивная ЧЖ была сравнима в группах (или даже выше при еSET).
Во всех исследованиях наблюдалась крайне высокая частота многоплодия (21,4–47,7%), что значительно превышает общепопуляционные показатели.
Ни в одном из исследований стратегия DET не оказалась экономически более эффективной. Даже в тех исследованиях, где для достижения 1 случая родов требовалось проведение нескольких циклов ВРТ, затраты были ниже при еSET, даже без учета долгосрочных экономических последствий.
Число переносимых эмбрионов: механизмы влияния на наступление беременности
Дискуссия о том, что первостепенно в отношении наступления беременности – рецептивность эндометрия или качество и количество переносимых эмбрионов, по-прежнему продолжается. В клинических ситуациях, когда перенос морфологически нормального эмбриона в «нормальный» по всем критериям эндометрий не приводит к наступлению беременности («привычное отсутствие имплантации»), применяются различные стратегии, в том числе изменение схем подготовки эндометрия, использование преимплантационного генетического тестирования на анеуплоидии (ПГТ-А), а также увеличение числа переносимых эмбрионов.
Безусловно, имеется достаточное количество данных о том, что нарушение рецептивности эндометрия у женщин с гинекологическими заболеваниями с высокой вероятностью приводит к развитию у них бесплодия и невынашивания беременности [25]. На протяжении всего периода развития ВРТ существовали попытки определения окна имплантации, в течение которого шансы на наступление беременности могли быть максимально высоки, с целью выбора оптимального дня для переноса эмбриона. Однако, согласно данным крупного метаанализа, проведенного Arian S.E. et al. (2023), тактика переноса эмбриона с предварительным определением индивидуального окна имплантации не приводит к значимому повышению частоты живорождения у пациенток, проходящих лечение с использованием методов ВРТ [26]. Более того, по результатам некоторых исследований, она даже может снизить ЧНБ [27].
ПГТ-А рекомендовано супружеским парам с неудачами программ ВРТ в анамнезе (согласно рекомендациям Европейского общества репродукции человека (ESHRE), 2020) [28]. Также, по мнению многих авторитетных исследователей, термин «привычное отсутствие имплантации» справедлив только для тех ситуаций, когда осуществлялся перенос эуплоидного эмбриона, и частота данного явления в популяции на самом деле не так велика (не более 5%) [29]. При этом доказательная база у метода ПГТ-А для пациентов с неудачами ВРТ в анамнезе остается недостаточной: ни в одном из крупных исследований использование ПГТ-А не приводило к повышению ЧНБ и ЧЖ [30, 31].
Увеличение числа переносимых в полость матки эмбрионов также является весьма спорной стратегий. Считается, что перенос нескольких эмбрионов может быть эффективнее, так как повышается вероятность, что хотя бы один из них имеет способность к имплантации, нормальный генетический набор, а также метаболическую и энергетическую компетентность клеток трофэктодермы. Следовательно, при «нормальном» эндометрии и наличии нескольких эмбрионов с различным потенциалом к имплантации неселективный перенос может быть более эффективной стратегией. Однако очень сложно оценить, насколько часто встречается такая комбинация событий. Данные исследований, демонстрирующих отсутствие повышения ЧНБ при неселективном переносе у молодых пациенток, подтверждают предположение, что если рецептивность эндометрия нарушена, число переносимых эмбрионов не имеет значения. С другой стороны, рецептивность эндометрия вряд ли можно охарактеризовать как бинарную величину, так как аномальная имплантация может приводить к большому спектру состояний – от полного отсутствия имплантации (бесплодие, неудачи ВРТ) до прерывания беременности на ранних сроках гестации и формирования акушерских осложнений. Перенос нескольких эмбрионов в полость матки при неудачах программ ВРТ в анамнезе также не оказался эффективной стратегией [30].
Роль осведомленности пациенток
Одним из факторов, препятствующих широкому внедрению стратегии eSET, является низкая информированность пациенток об эффективности данной стратегии (миф – «перенос 2 эмбрионов увеличивает шансы на беременность в 2 раза»), а также о рисках и осложнениях для матери и ребенка, связанных с многоплодием (миф – «современные медицинские технологии могут выходить ребенка с любыми состояниями»). Исследования в данной области демонстрируют, что стратегия eSET приемлема для пациенток в том случае, если не снижает шансы на наступление беременности [32]. Очевидно, что любое вмешательство, которое, как считается, снижает шансы на наступление беременности, будет встречено враждебно пациентами, имеющими анамнез бесплодия или репродуктивных потерь. Возможные меры преодоления подобных негативных установок:
- широкое использование технологии eSET;
- информирование пациенток об эффективности eSET, рисках многоплодной беременности; включение партнера, родственников пациентки в разговор;
- повышение результативности программ ВРТ при eSET;
- законодательное ограничение числа переносимых в полость матки эмбрионов.
В исследовании van den Akker O.B.A. et al. (2011) проанализирована эффективность различных методик информирования пациенток о преимуществах eSET: использование коммуникационных методик (эффект фрейминга – когнитивное искажение, когда форма подачи информации влияет на ее восприятие) показало себя более эффективным по сравнению со стандартным образовательным контентом [33].
Если нет четких законодательных ограничений по числу эмбрионов для переноса, врачи могут отказываться от стратегии eSET по просьбам пациентов [32]. По данным социологических опросов, для пациентов с бесплодием наступление многоплодной беременности является более предпочтительным по сравнению с одноплодной беременностью; однако следует учитывать, что пациенты не в полной мере осознают все риски для здоровья матери и детей, связанные с многоплодной беременностью, а средства массовой информации могут предоставлять искаженную информацию по данной теме. Другой мотивацией для отказа пациентов от eSET могут быть финансовые причины (особенно если циклы ВРТ не оплачиваются государством), а также нежелание повторно вступать в программу ВРТ. Так, по данным анкетирования пациентов в Дании, 58,6% пациентов предпочли наступление многоплодной беременности по сравнению с одноплодной. Несмотря на то что все пациенты получали информацию о рисках и осложнениях многоплодной беременности, 58% опрошенных заявили, что не получали такую информацию, а 32% из них отметили, что нуждаются в дополнительной информации. Авторы исследования сделали вывод, что пациенты, настроенные на многоплодную беременность, не до конца понимают и оценивают связанные с ней риски; кроме того, полученные данные свидетельствуют о нарушенной коммуникации между пациентами и персоналом клиники (видимо, пациенты находятся в стрессе и не воспринимают информацию правильно, а медицинский персонал не уделяет этому должного внимания) [34].
В 2016 г. психиатр Klitzman R. провел анкетирование сотрудников и пациенток клиник ВРТ (среди испытуемых также были сотрудники, которые сами проходили лечение с использованием ВРТ) с целью определения факторов, влияющих на выбор тактики лечения, в первую очередь число эмбрионов для переноса [35]. Наибольшее внимание уделяли психологическим факторам: пациенты часто могут игнорировать, минимизировать или отрицать риски и возможный вред для себя и детей, рожденных от многоплодной беременности, и пытаться рационализировать свои решения («со мной это никогда не случится» – цитата пациента). Кроме того, пациенты могут испытывать смешанные эмоции, связанные с их потребностями, желаниями, тревогой («пациенты очень непостоянны, поскольку находятся в отчаянии, ожидают волшебства и гарантии беременности» – цитата врача). Следовательно, пациенты могут не воспринимать сообщения об опасности и зацикливаться только на одном результате – рождении ребенка.
Кроме того, в данном исследовании отмечена низкая информированность пациентов о реальной статистике программ ВРТ. Например, некоторые пациенты не видели отличий между ЧНБ и частотой успешных родов. Возможно, в основе данного явления лежит недостаточное информирование широкой общественности об особенностях репродуктивной системы: «40% процентов женщин говорят, что скорее хотели бы получить четверню в результате ВРТ, чем неудачный перенос» [цитата врача]. В статье также обсуждалась роль средств массовой информации, которые, по мнению автора, искажают подаваемую информацию: например, распространяют фото «семерняшек» и «восьмерняшек» в раннем возрасте, но ничего не говорят об их здоровье в долгосрочной перспективе.
Когда речь идет о формировании семьи, теория часто расходится с практикой. Хотя многие пациенты считают наличие близнецов «идеальным» исходом ВРТ – результаты исследований противоположны. Многоплодная беременность ассоциирована с увеличением риска послеродовой депрессии, чувства неудовлетворенности браком, снижением качества жизни [36]. Пациенты с отсутствием родительского опыта могут не учитывать увеличение финансовых затрат, а также сложности ухода за двумя новорожденными детьми одновременно, особенно если дети родились преждевременно и требуют специального ухода. Поэтому выделение времени для обсуждения реальных исходов многоплодной беременности может быть одним из методов повышения приемлемости селективного переноса эмбриона.
Селективный перенос одного эмбриона в различных странах мира
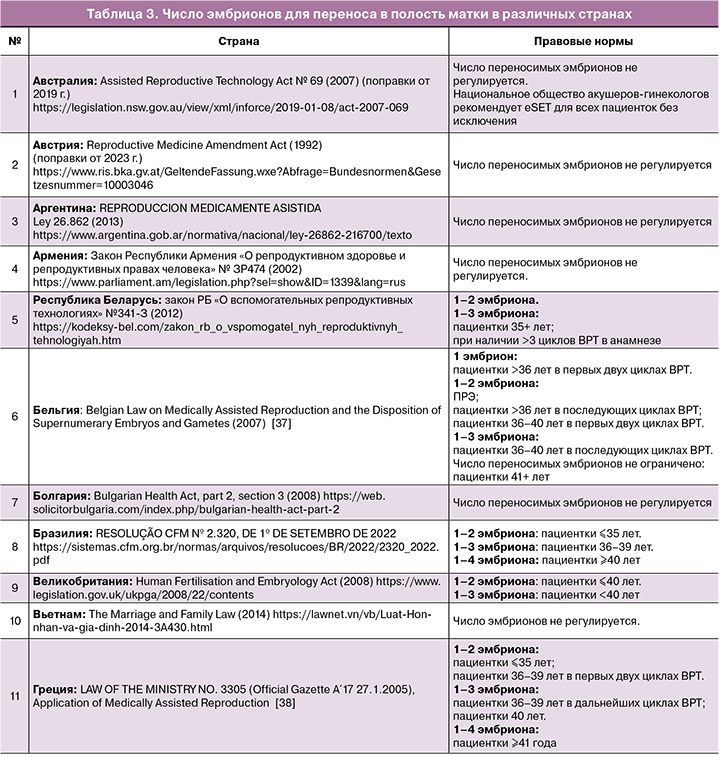
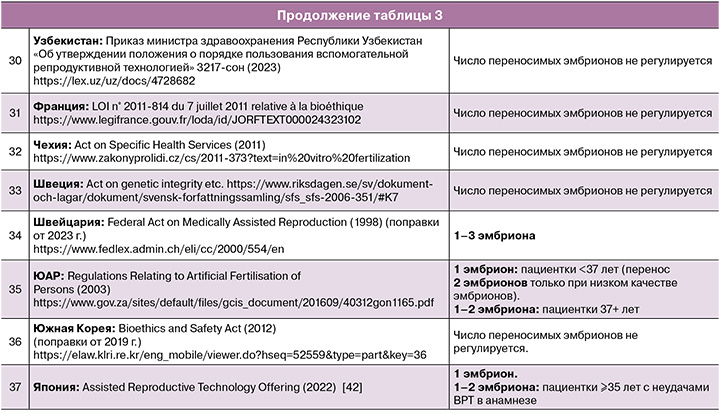
Во всем мире наблюдается тенденция к снижению числа переносимых эмбрионов в программах ВРТ. Однако наблюдается значительный разброс в законодательном регулировании ВРТ в зависимости от социально-географических, демографических, религиозных и других факторов. В ряде стран основные правила при проведении ВРТ регулируются законом, в других странах – национальными клиническими рекомендациями, в некоторых странах (в основном страны Латинской Америки) существуют только локальные нормативные акты (табл. 3).

Заключение
Несмотря на все достижения репродуктивной медицины за последние десятилетия, частота многоплодной беременности все еще остается проблемой, особенно учитывая тот факт, что часть подобных беременностей являются ятрогенными, и их появление можно предотвратить.На поверхность выходит еще одна проблема – недостаточное информирование пациентов о репродуктивной системе человека, о программах и методах ВРТ, их рисках и эффективности, а также коммуникативные проблемы между медицинскими работниками и пациентами.
Нет сомнений, что техника селективного переноса эмбрионов для всех пациентов без исключений приведет к снижению доли многоплодных беременностей после ВРТ. Но вызывает дискуссию вопрос о возможном снижении ЧНБ и родов у ряда пациенток при eSET. Селективный перенос эмбриона следует рекомендовать всем пациенткам с «хорошим» прогнозом наступления беременности, так как в данной группе частота родов сопоставима с таковой при переносе 2 эмбрионов. У пациенток с «неблагоприятным» прогнозом наступления беременности возможность внедрения eSET требует дальнейшего обсуждения.



