Ботулинотерапия – перспективное и быстро развивающееся направление в медицине, которое основано на инъекционном введении в мышечную ткань препаратов, содержащих ботулинический токсин (БТ), чаще типа А. Первые исследования БТ как лекарственного средства начались в конце 1960-х гг. в офтальмологии. В дальнейшем в 1984 г. было получено разрешение FDA на применение БТ типа А для коррекции косоглазия и блефароспазма. Впоследствии области медицины и список показаний стремительно расширялись. Так, в настоящее время ботулинотерапия активно применяется в косметологии, неврологии и урологии. Изучается применение БТ в лечении заболеваний желудочно-кишечного тракта [1].
В 2004 г. группой ученых из Австралии опубликовано первое пилотное исследование об эффективном применении БТ типа А при лечении хронической тазовой боли, связанной со спазмом мышцы, поднимающей задний проход. В результате исследования статистически значимо снижалась выраженность диспареунии (p=0,01), дисменореи (p=0,03) и дисхезии [2].
Ботулинический токсин: классификация, механизм действия
БТ – экзотоксин, нейротоксический белок, продуцируемый штаммами грамположительных, облигатно-анаэробных и спорообразующих бактерий рода Clostridium. Pirazzini M. et al. [3, 4] описали 4 группы клостридий, которые продуцируют семь серотипов БТ (от БТ-A до БТ-G) [5]. Первые серотипы нейротоксина (БТ-A, БТ-B) были выделены в 1919 г., а последний – БТ-G – в 1969 г. [6–8]. Разные типы БТ отличаются по эффективности. БТ-А и БТ-B являются единственными типами БТ, используемыми в лечебных целях; из них наиболее изученный БТ-А считается самым сильным и длительно действующим. Помимо денервации он оказывает обезболивающее действие, что особенно ценно при мышечных спазмах, сопровождающихся болевым синдромом. Особенности других БТ менее изучены, но представляют клинический интерес. Так, действие токсинов типа Е и F менее продолжительное; при этом их рассматривают в качестве альтернативы, когда у пациентки выработался иммунитет к БТ-А. Показана хорошая эффективность БТ-С, близкая с БТ-А, однако эти исследования еще продолжаются [9].
БТ состоит из тяжелой (м.м.~100 кДа) и легкой (м.м.~50 кДа) полипептидных цепей, связанных дисульфидной связью [10]. Тяжелая цепь одинакова для токсинов всех типов; она связывается с мембраной периферических нервных окончаний и с помощью аминогруппы, расположенной на ее конце, осуществляет перенос легкой цепи через эндосомальную мембрану. Легкая цепь различается у серотипов и представляет собой фермент – цинк-зависимую эндопептидазу, которая препятствует высвобождению ацетилхолина нервным окончанием [11]. Легкая цепь участвует в расщеплении белков
БТ – SNAP-25, VAMP1, VAMP2, VAMP3 и синтаксина-1. Расщепление одного из белков предотвращает высвобождение нейротрансмиттера из нейронов, блокируя слияние синаптических везикул с пресинаптической мембраной [3, 12, 13]. Именно благодаря этому механизму БТ используется в медицине. Был выявлен другой механизм, с помощью которого нейротоксин уменьшает боль. Из всех серотипов БТ-А специфически расщепляет SNAP-25, предотвращая высвобождение ацетилхолина в синаптическое пространство нейропептидов, таких как субстанция Р, кальцитонин-ген-родственный пептид и ионный канал TRPV1 [14]. Кроме того, БТ-A инактивирует натриевые каналы и может использоваться для нормализации повышенной возбудимости в периферических сенсорных нейронах [15]. Нейротоксиновый комплекс дополнительно стабилизирован белками, которые защищают его от разрушения в желудочно-кишечном тракте и, возможно, отвечают за формирование антител [9].
Безопасность введения БТ-А оценивалась в метаанализе Naumann M. et al. (2006), в котором были проанализированы данные 2361 пациента, из которых 1447 получили БТ-А по таким показаниям, как дистония и двигательные расстройства, церебральный паралич, желудочно-кишечные и урологические расстройства, болевые синдромы, гипергидроз, и в косметических целях. Частота побочных эффектов составила примерно 25% (365 из 1447) при введении БТ-А. Чаще всего упоминались очаговая слабость в месте введения, боль, эритема и отек. Случаев с очаговой слабостью было больше при лечении блефароспазма, но частота возникновения была одинаковой как в контрольной группе, так и при введении БТ-А [16].
Благодаря антиноцицептивным, противовоспалительным и миорелаксирующим свойствам БТ-А нашел свое применение в лечении многих хронических болевых синдромов [14, 15]. Список потенциальных новых показаний для БТ быстро расширяется, особенно активно в области терапии болевых синдромов, связанных с дисфункцией мышц тазового дна, и вульвовагинальной боли.
В России официально зарегистрированы следующие ботулотоксиновые препараты (БТ-А):
1. Ботокс (Allergan, США) – в России с 1994 г.;
2. Диспорт (Ipsen Pharma, Франция) – с 1999 г.;
3. Ксеомин (Merz, Германия) – с 2008 г.;
4. Лантокс (Lanzhou Institute of Biological Products, Китай) – с 2008 г.;
5. Релатокс («Микроген», Россия) – с 2012 г.;
6. Ботулакс (Hugel, Корея) – с 2017 г.
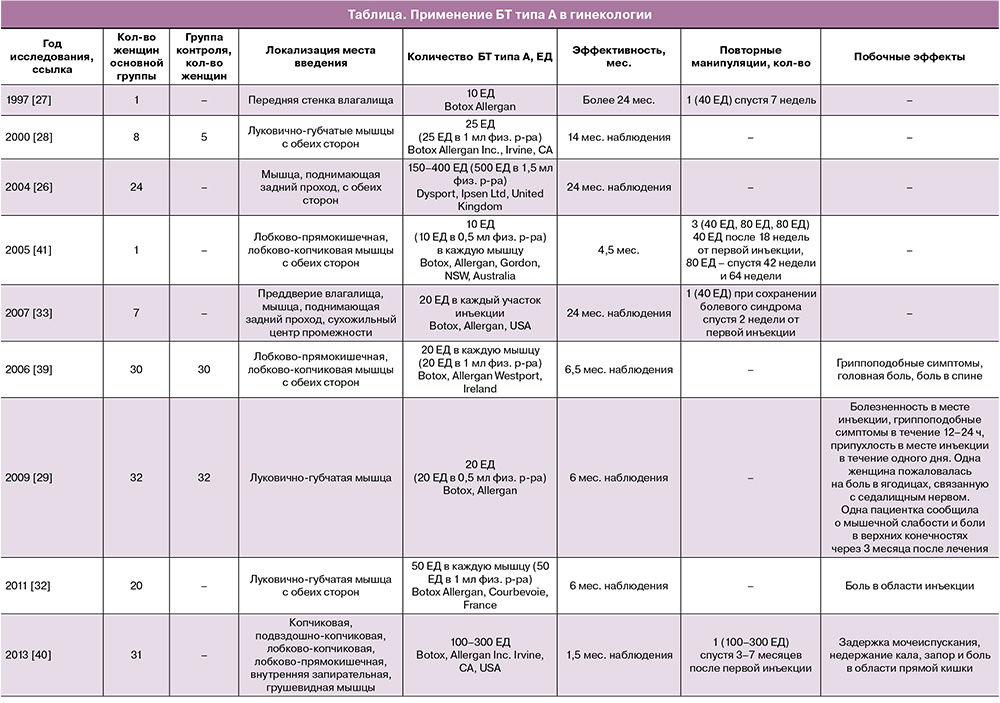
На данный момент применение БТ типа А в гинекологической практике возможно только в рамках клинических исследований (таблица).
Вагинизм
Вагинизм характеризуется непроизвольным, периодическим или постоянным сокращением мышц нижней трети влагалища, препятствующим половой близости. Вагинизм встречается у 5–17% женщин и может наблюдаться в любом возрасте [17]. Выделяют первичный вагинизм, при котором у пациентки половой акт болезненный с коитархе, и вторичный, при котором до появления симптомов половой акт не сопровождался болью [18]. Впервые вагинизм был описан в 1978 г. Ламонтом, который выделил 4 его степени тяжести [19].
1-я.
- Спазм мышц тазового дна поддается лечению.
- Пациентка способна переносить вагинальный осмотр.
2-я.
- Спазм присутствует, но сохраняется по всему тазу даже при попытке расслабления мышц.
- Невозможно расслабиться перед гинекологическим осмотром.
3-я.
- Спазм мышцы, поднимающей задний проход.
- Пациентка приподнимает ягодицы, чтобы избежать осмотра.
4-я.
- Спазм мышц промежности и мышцы, поднимающей задний проход.
- Пациентка приподнимает ягодицы, сводит бедра, гинекологический осмотр провести невозможно.
С помощью электромиографии у женщин с вагинизмом было зарегистрировано значительное повышение мышечной активности в мышце, поднимающей задний проход, лобково-прямокишечной и луково-губчатой мышцах даже при малейшем прикосновении или осмотре в отличие от здоровых женщин [20]. Этиология вагинизма неизвестна, значение имеют физические, психологические, социальные и культурные факторы [21]. Наиболее очевидна его связь с психологическими расстройствами. Так, некоторые женщины с вагинизмом ранее пережили сексуальное насилие, имели строгое религиозное воспитание, страх перед первым половым актом и избегали гинекологических осмотров [22–24]. Тревожные расстройства также могут быть причиной возникновения заболевания; при этом вагинизму сопутствуют болезненные и негативные переживания, за которыми следуют страх, уклонение от сексуальной близости, повышенная мышечная готовность [17]. Непсихологические причины могут включать заболевания, передающиеся половым путем, эндометриоз, пороки развития, выраженную атрофию влагалища и рубцовые изменения, воспалительные и онкологические заболевания органов малого таза [17, 25].
Лечение вагинизма должно быть комплексным и включать физиотерапию, тренировки мышц тазового дна, психотерапию, применение антидепрессантов, местное лечение (смазки, анестезирующие кремы, расширители) и, конечно, введение миорелаксантов. Как правило, в первую очередь лечение начинается с применения градуированных вагинальных расширителей. Другие способы облегчают или дополняют их использование и доступны только в клиниках, специализирующихся по проблемам дисфункции тазового дна [25].
Примерно у 10% женщин симптомы вагинизма не улучшаются при приеме анксиолитических препаратов и местном лечении [26]. Ботулинотерапия может рассматриваться в качестве перспективного альтернативного метода лечения данной группы пациенток. Первый случай лечения вагинизма БТ-А описали Brin M., Vapnek J. в 1997 г. [27]. Они сообщили об успешном лечении 29-летней женщины с диспареунией с помощью введения БТ-А в переднюю стенку влагалища. После терапии пациентка возобновила половую активность, которая была невозможной в течение 8 лет [27].
В исследованиях «случай–контроль» изучалась эффективность применения БТ в лечении вагинизма [28]. В одном исследовании женщинам с диагнозом вагинизма в луковично-губчатые мышцы вводили 25 ЕД БТ-А, разведенного в 1 мл физиологического раствора (n=8), и только физиологический раствор (n=5, группа контроля). Период наблюдения составил в среднем 10,2±3,3 месяца. У всех женщин после введения миорелаксанта наблюдались улучшения в сексуальной сфере: половая жизнь стала возможной или удовлетворительной; при этом в контрольной группе улучшений не было. Ghazizadeh I., Nikzad M. (2004) провели аналогичное исследование: 24 женщинам с отсутствием эффекта от предыдущего лечения вводили 150–400 ЕД БТ-А в лобково-прямокишечную мышцу. Согласно результатам исследования, 96% пациенток были осмотрены на гинекологическом кресле через 1 неделю после лечения, 75% женщин возобновили половую активность после первой инъекции. При среднем сроке наблюдения 12,3 месяца рецидивов не было [26].
При неэффективности терапии первой линии (физиотерапия, вагинальные расширители и др.) ботулинотерапия может быть альтернативным способом лечения боли и спазма и облегчать последующее использование расширителей.
Вульводиния
Вульводиния – это вид сексуальной дисфункции, проявляющейся болью в области половых органов без четкой идентифицируемой причины, которая длится не менее 3 месяцев. Вульводиния встречается примерно у 15% женщин [29]. Клинически наиболее распространенной формой вульводинии является спровоцированная вестибулодиния (боль локализуется в области преддверия влагалища). Заболевание характеризуется сложной патофизиологией, его этиология до конца не известна. Такие факторы, как инфекционно-воспалительные процессы, генетические, гормональные или механические, играют значимую роль в патогенезе заболевания [29, 30]. Одной из причин возникновения вульводинии является аберрантное увеличение числа ноцицепторов. Интраэпителиальная гиперплазия, связанная с повышенной чувствительностью периферических ноцицепторов, вызывает сильную боль в преддверии влагалища. Тучные клетки могут индуцировать гиперплазию нейронов через фактор роста нервов и гепараназу, возможно, в ответ на аллергены, такие как местный противогрибковый крем или семенная жидкость. Есть данные о гиперактивности афферентных С-волокон и нейротрансмиттеров (субстанция Р, глутамат), которые способствуют развитию боли. Лечение вульводинии включает местные анестетики, психотерапию, прием антидепрессантов, вплоть до вестибулэктомии [31]. В современной медицине БТ применяется, когда другие методы терапии не помогают.
Pelletier F. et al. (2011) проводили билатеральные инъекции 100 ЕД БТ типа А в луковично-губчатые мышцы женщинам с вульводинией (n=20). В результате было продемонстрированно значительное улучшение среднего показателя боли по ВАШ (визуальной аналоговой шкале от 0 до 10, где 10 – максимально сильная боль): от исходного уровня 8,37±1,22 до 2,57±2,67 (p<0,0001) через 3 месяца после лечения и 3,9±2,92 (p<0,0001) через 6 месяцев [32]. До введения БТ 90% женщин (n=18) имели апареунию. После проведенного лечения 72% женщин (n=13) смогли перенести осмотр гинекологическим зеркалом (p<0,001) [25]. Похожие результаты были описаны в исследовании Yoon H. et al. [33]. После введения 20–40 ЕД БТ-А женщинам с вульводинией (n=7) у всех исследуемых наблюдалось уменьшение боли, а ее субъективная оценка улучшилась с 8,3 до 1,4 балла; также следует отметить отсутствие рецидивов в периоде наблюдения от 4 до 24 месяцев. Пациентки сообщили, что после лечения значительно улучшилось качество половой жизни в аспекте диспареунии. Несмотря на многообещающие результаты данных исследований, недостатком является отсутствие контрольной группы.
В 2009 г. Petersen C. et al. в рандомизированном двойном слепом плацебо-контролируемом исследовании оценили эффективность инъекций БТ-А у 32 женщин с вульводинией по сравнению с контрольной группой (n=32) [29]. В луковично-губчатые мышцы женщинам основной группы вводили 20 ЕД БТ, разведенных в 0,5 мл физиологического раствора, в то время как в контрольной группе – 0,5 мл физиологического раствора. Результаты исследования были абсолютно противоположными: в обеих группах достигнуто значительное уменьшение боли, и авторы усомнились в успешном лечении вульводинии БТ.
Хроническая тазовая боль
Постоянная тазовая боль в течение более полугода считается хронической [34, 35]. Распространенность хронической тазовой боли (ХТБ) у женщин увеличивается и составляет примерно 15–20% во всем мире [36]. Однако фактическая распространенность ХТБ, вероятно, выше, так как многие женщины обследованы недостаточно. Jarrel J. et al. [37] определили сложную этиологию ХТБ, не связанную с желудочно-кишечными расстройствами, менструацией или сексуальной активностью. ХТБ наблюдается у лиц обоих полов, чаще у женщин. В основе развития болевого синдрома лежат общие механизмы, затрагивающие центральную нервную систему: сначала возникает регионарный болевой синдром, который в последующем охватывает всю область таза. Триггеры могут быть относительно безобидными, но у людей, предрасположенных к этому заболеванию, развивается ряд сенсорных нарушений, и они могут воспринимать нормальные ощущения как усиленные, вплоть до невыносимой боли. Это связано, в том числе, с психологическими, сексуальными, социальными и поведенческими расстройствами [37, 38]. К другим проявлениям данной патологии относятся: снижение физической активности, нарушение социальных и семейных отношений, депрессия и сопутствующие вегетативные дисфункции, такие как нарушения сна и аппетита.
В 2006 г. проведено двойное слепое рандомизированное исследование эффективности БТ-А по сравнению с плацебо у женщин с тазовой болью спастического характера и ХТБ длительностью более двух лет [39]. БТ вводили в количестве 80 ЕД в разведении 20 ЕД на 1 мл физиологического раствора в мышцы тазового дна (n=30), контрольной группе – физиологический раствор (n=30). Симптомы оценивались по ВАШ. Период наблюдения составил 6 месяцев, по окончании которого было отмечено уменьшение болевого синдрома в обеих группах, однако эффект у женщин, получивших инъекции БТ, был выше: тазовые боли, не связанные с менструациями, уменьшились с 51 балла по ВАШ до 22 баллов, диспареуния – с 66 до 12 баллов. После применения физиологического раствора улучшения отмечены только у женщин с диспареунией – 64 балла по ВАШ против 27 баллов. В ретроспективном исследовании Adelowo A. et al. (2013) оценили эффективность введения БТ-А в мышцу, поднимающую задний проход, у женщин с тазовой миофасциальной болью (n=31) [40]. Через 6 недель после манипуляции у 79,3% женщин наблюдалось уменьшение боли, у 20,7% отмечалось улучшение состояния. Двум женщинам с отсутствием эффекта проведено повторное введение БТ двукратно – через 3 и 7 месяцев. У трех пациенток процедура осложнилась недержанием мочи, требующим катетеризации мочевого пузыря, побочный эффект прошел самостоятельно спустя 12 недель после инъекций. В результате авторы сделали вывод об эффективности инъекций БТ-А в мышцу, поднимающую задний проход, женщинам с миофасциальной тазовой болью.
Thomson A. еt al. описали случай лечения пациентки с ХТБ, возникшей после субтотальной гистерэктомии по поводу перфорации матки. При перинеометрии был выявлен спазм лобково-прямокишечной мышцы. Женщине было введено по 10 ЕД БТ-А в разведении 10 ЕД на 0,5 мл физиологического раствора в правую и левую лобково-прямокишечные мышцы и правую и левую лобково-копчиковые мышцы с положительным эффектом в течение 18 недель [41]. После повторной манипуляции эффект сохранялся в течение 5 и 10 месяцев в виде улучшения качества жизни и сексуальной активности, снижения силы сокращения мышц тазового дна по данным манометрии и улучшения баллов по ВАШ. Побочных эффектов в ходе манипуляции и в периоде наблюдения не отмечалось.
Заключение
За последние два десятилетия наблюдается стремительный рост публикаций, посвященных изучению эффективности и безопасности ботулинотерапии в лечении различных гинекологических заболеваний, прежде всего связанных с гипертонусом мышц тазового дна. Для выбора правильного алгоритма лечения таких сложных пациентов необходим мультидисциплинарный подход, включающий участие не только гинеколога, но и невролога/альголога, специализирующихся на лечении тазовой боли, физиотерапевта, психиатра, по показаниям – мануального терапевта, уролога, проктолога и даже нейрохирурга. Данный обзор объединяет исследования, свидетельствующие о том, что ботулинотерапию можно рассматривать в качестве альтернативного метода лечения в случае неэффективности традиционной терапии. Однако необходимо проведение крупномасштабных исследований для определения оптимальной дозы БТ, стандартизации алгоритма его введения у пациенток с гипертонусом мышц тазового дня и тазовой болью.



