В настоящее время в мире нет единой концепции в лечении преждевременных родов (ПР) — в разных странах существующие рекомендации для проведения токолиза отличаются. Основной целью токолитической терапии является пролонгирование беременности на 48 ч для того, чтобы провести профилактику респираторного дистресс-синдрома плода глюкокортикоидами и успеть доставить пациентку в перинатальный центр с возможностью оказания помощи недоношенному новорожденному.
В то же время, не всегда целесообразно пролонгировать беременность при таких ее осложнениях, как тяжелая плацентарная недостаточность, преэклампсия. Именно поэтому американская коллегия акушеров-гинекологов так сформулировала подход к токолитической терапии: проводить токолиз в течение 48 ч только тем беременным, чьи плоды выиграют в результате проведения токолиза. Но, принимая во внимание неблагоприятные перинатальные исходы при ПР, высокую перинатальную смертность, особенно на сроках до 28-й недели [1], задачи токолитической терапии, на наш взгляд, должны быть еще более серьезными — пролонгирование беременности до максимально возможного срока, в идеале — до 37 недель.
Показанием к проведению токолиза являются ПР, клиническими критериями которых являются схватки не менее 4 за 20 мин и динамика шейки матки. Следует помнить, что токолиз при открытии шейки матки 3 и более см, неэффективен.
Токолиз проводится на сроках 24—34 недели гестации. Однако в последнее время американская коллегия акушеров-гинекологов допускает использование токолитиков до 24 недель при индивидуальном подходе [2]. В качестве токолитической терапии используются следующие группы препаратов:
- β-адреномиметики;
- блокаторы кальциевых каналов;
- блокаторы окситоциновых рецепторов;
- ингибиторы циклооксигеназы;
- донаторы оксида азота (NO).
Рекомендации Всемирной Организации Здравоохранения (ВОЗ)
ВОЗ при ПР рекомендует применять глюкокортикоиды (дексаметазон или бетаметазон в суммарной дозе 24 мг) для профилактики респираторного дистресса плода новорожденных. При этом токолитическая терапия не рекомендована ВОЗ в случае угрожающих ПР, потому что ни одна группа препаратов не показала доказанного эффекта в сравнении с плацебо. В то же время, ВОЗ приводит данные ряда исследований, которые говорят о том, что β-адреномиметики и блокаторы кальциевых каналов позволяют пролонгировать беременность на 48 ч и даже на 7 и более дней у женщин с угрожающими ПР, а блокаторы окситоциновых рецепторов показывают высокую эффективность на сроке до 28 недель. Данные по ингибиторам циклооксигеназы противоречивы, а донаторы NO и прогестерон не показали эффективности при развитии ПР. Согласно рекомендациям ВОЗ, если врач считает нужным провести токолиз, то препаратом выбора является нифедипин, а использование магния сульфата рекомендовано в случае начавшихся ПР на сроке до 32 недель для снижения частоты детского церебрального паралича у детей. Кроме того, ВОЗ не рекомендует назначение антибиотиков при ПР и целом плодном пузыре и отсутствии признаков воспаления; в то же время, при преждевременном разрыве плодных оболочек рекомендовано назначение эритромицина [3].
Европейская ассоциация перинатальной медицины в качестве препаратов первой линии для токолиза рассматривает β-адреномиметики (гексопреналин), а также рекомендует использование блокатора окситоциновых рецепторов (атозибан), блокатора кальциевых каналов (нифедипин). Ингибиторы циклооксигеназы (индометацин, аспирин) отнесены к группе с ограниченной эффективностью, а сульфат магния — с недоказанной эффективностью.
Согласно данным ведущего клинического ресурса UpToDate, основанного на принципах доказательной медицины, препаратом выбора для проведения токолиза является индометацин. Чтобы избежать преждевременного закрытия артериального протока у плода и маловодия использовать данный препарат следует не более 72 ч. Если есть противопоказания для использования индометацина (снижение уровня тромбоцитов, нарушения системы гемостаза, язвенная болезнь, нарушение функции почек и/или печени, астма, срок беременности более 32 недель) или при его неэффективности, назначают нифедипин. К препаратам с меньшей эффективностью относится блокатор окситоциновых рецепторов атозибан, который широко используется в Европе. В США управление по контролю за продуктами и лекарствами (FDA) отказалось одобрить использование атозибана для токолиза из-за опасений о безопасности препарата при использовании во время беременности менее 28 недель беременности, поскольку проведенный мета-анализ в 2014 г. показал неэффективность атозибана в сравнении с плацебо — не было снижения частоты ПР на всех сроках гестации [2, 4].
В то же время американская коллегия акушеров-гинекологов и общество медицины матери и плода рассматривают сульфат магния в качестве возможного препарата для токолиза [5]. В настоящее время нет данных, объясняющих действие сульфата магния на сократительную активность матки, несмотря на более чем 40-летнюю историю использования его в акушерской практике. Большое количество исследований эффективности использования сульфата магния для лечения ПР не выявило преимуществ этого препарата в сравнении с другими, но и не показало его неэффективность [6].
Еще одной группой препаратов, рекомендованных для токолиза, являются донаторы NO. Нитраты взаимодействуют с SН-группами гладкомышечных клеток сосудистой стенки, что ведет к высвобождению NО — мощного эндотелиального релаксирующего фактора. NО вызывает активацию гуанилатциклазы, что приводит к увеличению циклического гуанозинмонофосфата (цГМФ). Увеличение содержания цГМФ в гладкомышечных клетках активирует киназы легкой цепи миозина, приводящие к расслаблению гладких мышц [7]. Поэтому нитроглицерин также возможно использовать в качестве токолитика. Однако, нет убедительных данных, подтверждающих или опровергающих его эффективность. Нитроглицерин можно использовать трансдермально в виде пластыря (10 мг на кожу живота и при сохраняющейся клинике ПР через час добавить еще 10 мг) [8] или внутривенно со скоростью 20 мкг/мин [9].
Все исследователи единогласны, что нецелесообразно использование сразу нескольких токолитиков в связи с потенцированием побочных эффектов и невозможностью оценить эффективность каждого из препаратов. Тем не менее, при очень ранних ПР используют комбинацию токолитиков по индивидуальной схеме. В случае повторного эпизода развития ПР рекомендуется использовать те же препараты, что и для лечения в первом случае.
В нашей стране наиболее популярными препаратами для проведения токолиза являются атозибан и гексопреналин. Нифедипин не зарегистрирован в качестве токолитика. Сульфат магния рекомендован в качестве нейропротектора центральной нервной системы плода. Проведенные исследования показали, что атозибан, и в сравнении с гексопреналином, и в сравнении нифедипином, показывает более высокую эффективность и позволяет пролонгировать беременность более чем на 7 дней. Кроме того, после терапии атозибаном каждой третьей пациентке удалось доносить беременность (33,3% и 22,6%) [10, 11].
Цель исследования — выработать патогенетический подход к токолитической терапии при ПР.
Материалы и методы
Нами проведено исследование эффективности атозибана, в которое вошло 146 беременных женщин с угрожающими ПР в сроке беременности от 24-й до 34-й недели. Критериями включения в исследование были: сократительная активность матки (4 и более схватки за 20 мин), динамика шейки матки (укорочение, раскрытие шейки до 3 см), интактный плодный пузырь, удовлетворительное состояние женщины и плода, информированное согласие пациентки. Критериями исключениями из исследования были: тяжелое состояние матери, дистресс плода, врожденные пороки развития плода, хориоамнионит. Сразу после установления диагноза ПР начинали токолиз атозибаном по стандартной схеме:
- 1 этап: в течение 1 мин вводится 1 флакон по 0,9 мл препарата без разведения (начальная доза — 6,75 мг);
- 2 этап – насыщение: в течение 3 ч проводится инфузия препарата в дозе 300 мкг/мин (скорость введения — 24 мл/ч, доза атозибана — 18 мг/ч);
- 3 этап – продолжительная инфузия: проводится продолжительная (до 45 ч) инфузия препарата атозибана в дозе 100 мкг/мин (скорость введения — 8 мл/ч, доза атозибана — 6 мг/ч).
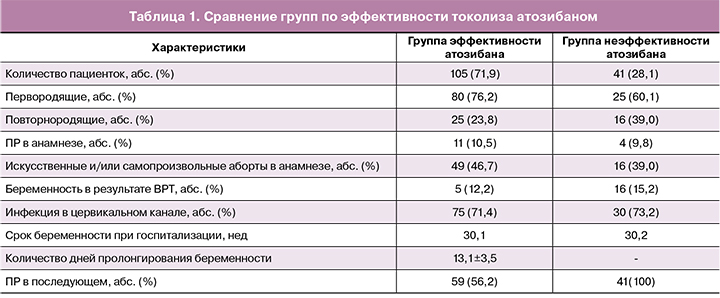
Максимальная общая продолжительность лечения составляла 48 ч. Эффективность токолиза определяли по длительности пролонгирования беременности: эффективен, если удавалось пролонгировать беременность на 48 ч и более; неэффективен, если роды происходили на фоне введения атозибана. Сравнение групп в зависимости от эффективности токолиза приведено в таблице 1.
Всем пациенткам проводилось бактериологическое исследование содержимого цервикального канала и влагалища с определением чувствительности к антибиотикам.
С целью выяснения возможных механизмов патогенеза ПР и проведения не только симптоматического, но и патогенетически обоснованного токолиза, нами дополнительно было проведено исследование экспрессии toll-подобных рецепторов (TLR) клетками цервикального канала у 42 женщин с клинической картиной угрожающих ПР: жалобы пациенток на тянущие боли в нижних отделах живота, повышенный тонус матки и укорочение шейки матки менее 25 мм, по данным цервикометрии. Поскольку роль TLR в генезе ПР, вызванных инфекционными факторами, уже изучена и доказана, то у всех этих пациенток был исключен инфекционный генез ПР на основании данных анамнеза и бактериологического исследования содержимого влагалища и цервикального канала. После удаления слизи из цервикального канала для исследования экспрессии TLR клетками эпителия цервикального канала соскобы слизистой шейки матки собирались цитощеткой тип D модель 1 в отдельные стерильные эппендорфы. На первом этапе из эпителиальных клеток выделяли РНК методом аффинной сорбции на частицах силикагеля с помощью набора «АмплиПрайм РИБО-сорб» компании ИнтерЛабСервис (РФ) строго в соответствии с протоколом. После этого проводилась реакция обратной транскрипции с помощью «Набора реагентов для проведения обратной транскрипции» (Синтол, РФ) строго в соответствии с протоколом. Праймеры для последовательностей исследуемых мРНК были подобраны с помощью программы Vector NTI 8,0 и синтезированы фирмой Синтол. Праймеры и зонды для ПЦР-РВ были смоделированы в компьютерной программе Vector NTI 8,0 в соответствии с последовательностями мРНК исследуемых генов (последовательности мРНК были взяты в базе GenBank) и синтезированы в фирме «Синтол» (РФ). Для проведения ПЦР был использован «Набор реагентов для проведения ПЦР-РВ в присутствии SYBR Green I» (Синтол, РФ) строго в соответствии с протоколом. После приготовления реакционных смесей пробирки помещали в амплификатор для ПЦР-РВ ДТ-96 (ДНК - технология, РФ). Режим реакции - 40 циклов (95 °C 20 мин, 60 °C 40 мин).
Группу сравнения составили 32 женщины с неосложненным течением беременности.
Результаты исследования
Среди факторов риска ПР у 10,3% женщин в анамнезе были ПР, у 44,5% — прерывания беременности (самопроизвольные выкидыши, искусственные аборты), у 14,4% беременность наступила в результате использования вспомогательных репродуктивных технологий (ВРТ). При дообследовании у 71,2% женщин выявлена инфекция в цервикальном канале (E.faecalis, E.coli, St.coagulase negative, K.pneumoniae). У 71,9% (n=105) беременных с ПР токолиз атозибаном позволил пролонгировать беременность на 48 и более часов, и эти пациентки составили группу эффективности атозибана. В среднем удалось пролонгировать беременность на 13,1±3,5 дней (табл. 1). Не было выявлено различий в эффективности атозибана в зависимости от срока гестации: на 24—27-й неделе положительный результат был получен у 75% женщин, в 28—30 недель — у 72,7%, в 31—34 недели – у 67,9% беременных. Среди пациенток со зрелой и созревающей шейкой матки эффективность была в 63,6% и 66,7% наблюдений соответственно; тогда как у женщин с незрелой шейкой матки эффективность достигала 83,7%. Лишь у 31,5% пациенток удалось пролонгировать беременность до доношенного срока.
Изучение экспрессии toll-подобных рецепторов (TLR) эпителием цервикального канала показало, что у женщин с угрозой ПР экспрессия TLR2 была в 3,65 раз выше, чем у женщин с неосложненным течением беременности (48,0 и 174,99; р<0,05). Экспрессия TLR4 также была в 1,33 раза выше в группе с угрозой ПР по сравнению с контрольной группой (53,2 и 70,92; p>0,05) (табл. 2).

Обсуждение
С целью снижения частоты ПР и улучшения перинатальных исходов в современном акушерстве одним из актуальных вопросов остается вопрос токолиза. Подход к токолизу в разных странах отличается. Большие надежды были связаны с блокатором окситоциновых рецепторов атозибаном, поскольку блок этих рецепторов должен был привести к остановке сократительной деятельности матки. Согласно результатам О.Р. Баева и соавт. [11], эффективность атозибана в течение 48 ч была у 96,5% пациенток, однако доносить беременность удалось лишь 33,3% женщин. По результатам нашего исследования, эффективность токолиза была у 71,9% женщин, но только у 31,5% женщин роды произошли после 37-й недели. На наш взгляд, при ПР задачей токолиза должно быть не кратковременное пролонгирование беременности, а рождение доношенного ребенка.
 Все это позволяет говорить о том, что токолиз по-прежнему остается важной и не до конца решенной проблемой. Почему токолиз неэффективен? Возможно, ответ в том, что мы пытаемся воздействовать на уже начавшуюся родовую деятельность и справиться с симптомом, забывая о патогенезе данного осложнения беременности. А в патогенезе ПР лежит воспалительный процесс в маточно-плацентарном комплексе. Причиной его, как показывают многочисленные авторы, может быть как инфекция, которая в нашем исследовании была выявлена у 71,2% женщин, так и так называемое стерильное воспаление, патогенез которого до конца не ясен [12]. Одним из звеньев, участвующих в реализации стерильного воспаления, являются toll-подобные рецепторы (TLR) [13].
Все это позволяет говорить о том, что токолиз по-прежнему остается важной и не до конца решенной проблемой. Почему токолиз неэффективен? Возможно, ответ в том, что мы пытаемся воздействовать на уже начавшуюся родовую деятельность и справиться с симптомом, забывая о патогенезе данного осложнения беременности. А в патогенезе ПР лежит воспалительный процесс в маточно-плацентарном комплексе. Причиной его, как показывают многочисленные авторы, может быть как инфекция, которая в нашем исследовании была выявлена у 71,2% женщин, так и так называемое стерильное воспаление, патогенез которого до конца не ясен [12]. Одним из звеньев, участвующих в реализации стерильного воспаления, являются toll-подобные рецепторы (TLR) [13].
Проведенное нами исследование экспрессии TLR эпителием цервикального канала при спонтанных ПР неясной этиологии показало, что даже при исключении инфекции в цервикальном канале экспрессия TLR была повышена в сравнении с нормально протекающей беременностью. Повышенная экспрессия TLR приводит к запуску процесса воспаления: повышенной выработке провоспалительных цитокинов, простагландинов и в конечном итоге — к преждевременному сокращению матки. Полученные данные позволили еще раз подтвердить, что ПР являются процессом воспалительного генеза. Понимая, что в основе патогенеза ПР лежит воспалительный процесс, на наш взгляд, целесообразно рассматривать именно ингибиторы циклооксигеназы в качестве первой линии терапии ПР. В 70—80-е годы прошлого столетия в нашей стране индометацин использовался в качестве токолитика, однако впоследствии от него отказались в виду побочных эффектов. При соблюдении выработанной в мире схемы введения данного препарата (до срока 32-й недели, не более 5—7 дней), можно избежать нежелательных побочных эффектов.
У 71,2% женщин при дообследовании была выявлена инфекция в цервикальном канале. Поэтому в схему лечения ПР обязательно надо включать антибактериальные препараты. Это должны быть антибиотики широкого спектра, использовать следует внутривенный путь их введения для лучшей биодоступности, с последующей коррекцией терапии по результатам антибиотикограммы.
Заключение
Таким образом, патогенез спонтанных ПР может быть представлен следующей схемой (рисунок). Исходя из этого, ведущим токолитиком должен быть блокатор циклооксигеназы, а для повышения эффективности токолиза обязательно использовать антибактериальную терапию.



