Преэклампсия (ПЭ) остается серьезной медико-социальной проблемой во всем мире, являясь одной из основных причин материнской и перинатальной заболеваемости и смертности [1, 2].
В развитии ПЭ ведущую роль играют нарушение инвазии трофобласта, недостаточность маточно-плацентарного кровотока и ишемия плаценты [1–3]. Согласно современным представлениям о формировании и функционировании плаценты апоптоз и клеточная пролиферация имеют большое значение в поддержании морфофункционального состояния плаценты в норме и при ее патологии [4–9]. В настоящее время указанные феномены активно исследуются с целью выявления патоморфологических предпосылок к развитию ПЭ. Предполагается, что при ПЭ изменяется баланс между программами пролиферации и апоптоза в эндотелиальных клетках, цито- и синцитиотрофобласте, что приводит в итоге к развитию плацентарной ишемии и формированию ПЭ.
Процессы клеточного обновления в плаценте при ПЭ изучены недостаточно, сведения часто противоречивы. Часть авторов указывает на повышенную экспрессию маркеров клеточной пролиферации [10, 11] и антиапоптоза в плаценте при ПЭ на фоне снижения проапоптических показателей [12–14]. Другие исследователи зарегистрировали активацию программ апоптоза в трофобласте в сочетании с неизмененной или сниженной экспрессией показателей антиапоптоза [15–18] и клеточной пролиферации [17].
Целью настоящего исследования является оценка активности процессов плацентарного апоптоза и клеточной пролиферации при ПЭ.
Материал и методы исследования
Проведено исследование «случай-контроль» 39 беременных женщин, которые получали стационарное лечение в родильном доме клиники ГБОУ ВПО ЮУГМУ Минздрава России. Критерием включения явилось информированное согласие женщины на участие в исследовании. Критерии исключения: онкологические заболевания, ВИЧ-инфекция, туберкулез, тяжелая соматическая патология, психические заболевания, алкоголизм, наркомания. План исследования соответствует законодательству России, международным этическим нормам, нормативным документам исследовательских организаций, одобрен этическим комитетом ГБОУ ВПО ЮУГМУ. Изучены особенности течения беременности и исходы родов, проведено морфологическое исследование плацент.
В зависимости от наличия/отсутствия ПЭ и степени ее тяжести [1] выделены: 1-я группа (контрольная) – 11 женщин, течение беременности которых не осложнилось развитием ПЭ; 2-я группа – 14 беременных с умеренной ПЭ; 3-я группа – 14 пациенток с тяжелой ПЭ. Средний возраст женщин 1-й группы составил 27,00±1,67 года, 2-й – 27,63±1,05, 3-й – 30,36±1,64.
Ультразвуковое исследование и оценка допплерометрических параметров кровотока фетоплацентарного комплекса проводились на диагностических ультразвуковых системах М5 (Mindrai, КНР), Sonoace Pico и Sonoace 8800 (Medison, Южная Корея).
В зависимости от степени гемодинамических нарушений в системе мать–плацента–плод (НМПК) и синдрома задержки развития плода (СЗРП) выделены компенсированная (НМПК 1-й степени и/или СЗРП 1-й степени), субкомпенсированная (НМПК 2-й степени и/или СЗРП 2-й степени), декомпенсированная (НМПК 3-й степени и/или СЗРП 3-й степени) формы хронической плацентарной недостаточности (ХПН).
Оценка физического развития новорожденных проводилась с помощью оценочных таблиц Г.М. Дементьевой
Морфологические методы исследования. Исследовано 11 плацент женщин 1-й группы, 15 – 2-й группы (в том числе 2 плаценты из бихориальной биамниотической двойни), 17 – 3-й группы (в том числе 2 плаценты из бихориальной биамниотической двойни, 3 плаценты из трихориальной триамниотической тройни). Проводили гистологическое, иммуногистохимическое и морфометрическое исследование плацент.
Гистологическое исследование проводили на парафиновых срезах, окрашенных гематоксилином и эозином. Количественное исследование гистологических структур (незрелые ворсины, некротизированные ворсины, капилляры стромы терминальных ворсин, синцитиальные почки ворсин) проводили с помощью окулярной измерительной сетки и метода точкосчетной объемометрии [19] в 10 случайно отобранных полях зрения при увеличении 400.
Иммуногистохимическое исследование использовали для оценки в структурах ткани плаценты (симпластотрофобласт, эндотелий капилляров, макрофаги стромы ворсин) активности процессов клеточной пролиферации (ki-67), антиапоптоза (bcl-2) и проапоптоза (р53). В качестве первичных специфических антител использовали моноклональные антитела к p53 («Dako Denmark A/S», RTU-p53, Clon DO-7, Denmark), bcl-2 («Dako Denmark A/S», RTU-bcl-2, Clon 124, Denmark), ki-67 («Dako Denmark A/S», RTU-Ki-67, Clon MIB-1, Denmark). В качестве вторичных антител и визуализирующей системы применяли набор детекции («Dako Denmark A/S», EnVision+ System, HRP, Denmark). Количественное исследование для маркеров ki-67, bcl-2, Р53 проводили в 10 случайно выбранных полях зрения при увеличении 400, подсчитывая количество клеток, дающих интенсивное связывание пероксидазы в 1 мм2. С целью выяснения направленности изменений процессов клеточного обновления рассчитаны индексы: р53/bcl-2 (соотношение процессов про- и антиапоптоза) и ki-67/p53 (соотношение процессов клеточной пролиферации и проапоптоза). Просмотр и фотосъемку микропрепаратов осуществляли на микроскопе «Leica» (Germany) с использованием цифровой фотокамеры «Carl Zeiss Jena» (Germany).
Статистические расчеты были выполнены с помощью пакетов программ: SPSS 12.1, Statistica for Windows 6.0, STADIA 6.3 prof. Применен аппарат проверки статистических гипотез с использованием критериев Манна–Уитни, χ2 Пирсона; отношение правдоподобия, линейно-линейная связь; Тау Гудмена и Краскала; коэффициент неопределенности при уровне значимости критерия 0,05. Кроме того, использовался непараметрический корреляционный анализ с расчетом коэффициента Спирмена.
Результаты исследования и обсуждение
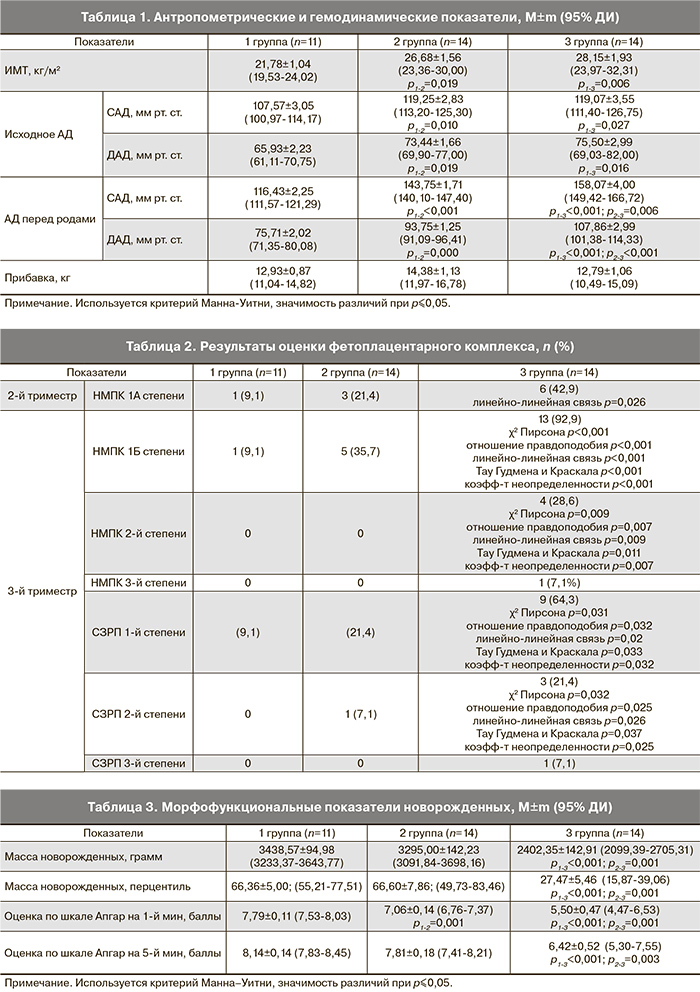
У женщин, течение беременности которых в дальнейшем осложнилось ПЭ, антропометрические параметры (индекс массы тела – ИМТ) и показатели систолического и диастолического артериального давления (САД и ДАД соответственно) до наступления настоящей беременности оказались выше, чем в контрольной группе (табл. 1), статистически значимых отличий между 2-й и 3-й группами не установлено. Перед родоразрешением повышение АД зарегистрировано у всех пациенток с ПЭ (больше при тяжелой ПЭ), прибавка массы тела во время беременности в группах оказалась одинаковой.
В настоящее время плацентарные нарушения считаются приоритетными в патогенезе развития ПЭ, поэтому было оценено состояние фетоплацентарного комплекса у беременных, участвовавших в нашем исследовании. Уже во втором триместре гестации (табл. 2) у пациенток 3-й группы зарегистрирована высокая частота ХПН, которая проявлялась НМПК 1А степени.
В третьем триместре гестации (табл. 2) при допплерометрической оценке маточно-плацентарно-плодового кровотока его нарушение чаще регистрировалось у пациенток с ПЭ, причем случаи НМПК 2-й и 3-й степеней были выявлены только при тяжелой ПЭ. СЗРП в третьем триместре (табл. 2) также диагностировался чаще у беременных 3-й группы, частота регистрации данной патологии 2-й и 3-й степеней оказалась наибольшей. Таким образом, частота ХПН при тяжелой ПЭ (100%) была выше в сравнении с 1-й (18,2%) и 2-ой(50,0%) группами (χ2 Пирсона р=0,002; отношение правдоподобия р=0,001; линейно-линейная связь р=0,000; Тау Гудмена и Краскала р=0,003; коэффициент неопределенности р=0,002). В 3-й группе было выявлено 5 (35,7%) случаев субкомпенсированной и 2 (14,3%) случая декомпенсированной ХПН (χ2 Пирсона р=0,001; отношение правдоподобия р=0,001; линейно-линейная связь р=0,002; Тау Гудмена и Краскала р=0,002; коэффициент неопределенности р=0,001).
Масса новорожденных от матерей с тяжелой ПЭ (табл. 3) оказалась достоверно меньше в сравнении с 1-й и 2-й группами.
Установлены достоверные отличия по частоте асфиксии новорожденных, матери которых имели ПЭ, тяжесть асфиксии увеличивалась при тяжелой ПЭ (χ2 Пирсона р<0,001; отношение правдоподобия р<0,001; линейно-линейная связь р<0,001; коэффициент сопряженности р<0,001; Тау Гудмена и Краскала р<0,001; коэффициент неопределенности р<0,001). В 3-й группе зарегистрирован 1 случай антенатальной гибели плода. Дети, рожденные от женщин с тяжелой ПЭ, достоверно чаще в сравнении с остальными новорожденными имели такие серьезные осложнения течения неонатального периода, как респираторный дистресс-синдром, ателектазы легких, внутриутробная инфекция новорожденного, что потребовало реанимационных мероприятий с использованием искусственной вентиляции легких. Полученные результаты, несомненно, связаны не только с тяжестью ПЭ матерей, но и с недоношенностью новорожденных. Действительно, срок родоразрешения при тяжелой ПЭ (36,35±0,55 недель) оказался достоверно меньше в сравнении с аналогичным показателем в 1-й (39,18±0,23) и 2-й группах (38,60±0,23), частота преждевременных родов (57,2%) была наибольшей в группе пациенток с тяжелой ПЭ (χ2 Пирсона р<0,001; отношение правдоподобия р<0,001; линейно-линейная связь р<0,001; коэффициент сопряженности р=0,000; Тау Гудмена и Краскала р<0,001; коэффициент неопределенности р<0,001).
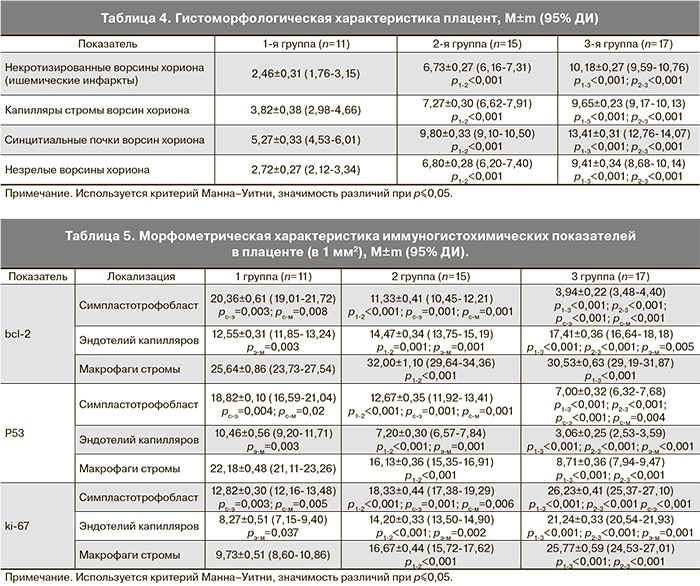
При гистологическом исследовании плацент у женщин 1-й группы (табл. 4) отмечены инволютивные (возрастные) изменения, компенсаторно-приспособительные процессы и в меньшей степени патологические изменения, проявляющиеся иногда незрелостью ворсин хориона. Объемная доля синцитиальных почек и капилляров стромы оказались наибольшими по сравнению с объемными долями некротизированных и незрелых ворсин. При умеренной ПЭ установлено (табл. 4),
что объемные доли незрелых ворсин, ишемических инфарктов, капилляров стромы ворсин, синцитиальных почек были достоверно больше по отношению к контрольной группе. В плацентах пациенток с тяжелой ПЭ (табл. 4) указанные показатели статистически значимо превышали аналогичные в двух других группах. Таким образом, при развитии ПЭ в плаценте наряду с компенсаторно-приспособительными реакциями, которые проявляются выраженной очаговой гиперплазией капилляров стромы и пролиферацией синцитиальных почек ворсин, регистрируются различные по выраженности дистрофические изменения синцитиального покрова ворсин, существенно увеличивается объем незрелых ворсин без синцитиальных почек и ишемических инфарктов. При нарастании тяжести ПЭ степень патологических изменений в сочетании с мелкоочаговым характером компенсаторно-приспособительных реакций значительно увеличиваются.
Результаты нашего исследования согласуются с данными современной литературы. L. Devisme и соавт. (2013), L. Nahar и соавт. (2013), D.U. Stevens и соавт. (2013), Г.Т. Сухих и соавт. (2010) у пациенток с ПЭ выявили аналогичные повреждения: незрелые ворсины, часто отсутствие промежуточных ворсин, аваскулярные терминальные ворсины, увеличение количества синцитиальных почек, децидуальная васкулопатия, фиброз ворсин, эритробластоз, инфаркты, указанные изменения коррелировали с тяжестью ПЭ [2, 20–22]. В.А. Цинзерлинг и соавт. (2002) отмечают, что при ПЭ альтеративные клеточные изменения и нарушения микроциркуляции всегда сочетаются с развитием компенсаторно-приспособительных реакций с гиперваскуляризацией ворсин [23].
Признаки инфицирования плаценты выявлены у 1 (9,1%) женщины 1-й группы, 3 (21,4%) пациенток 2-й и 9 (64,3%) – 3-й группы (χ2 Пирсона р=0,025; отношение правдоподобия р=0,021, линейно-линейная связь р=0,008; Тау Гудмена и Краскала р=0,033; коэффициент неопределенности р=0,021). Аналогичные изменения в плаценте при ПЭ описаны В.А. Цинзерлингом и соавт. (2002) [23].
Особый интерес представляет оценка активности процессов апоптоза и клеточной пролиферации на уровне плаценты, которые в настоящее время считаются патоморфологической основой плацентарной патологии, в том числе при ПЭ. При физиологической беременности в ворсинчатом трофобласте апоптоз регулируется параллельно с дифференцировкой трофобластических клеток и слиянием их в синцитиотрофобласт [8]. Включение гена опухолевого супрессора Р53 может привести к аресту клеточного цикла, следствием которого является репарация ДНК или апоптоз [24]. В плаценте высокая экспрессия Р53 верифицирована во внутренних слоях цитотрофобласта и в колоннах клеток цитотрофобласта, в синцитии экспрессия несколько ниже [24, 25]. Ингибитор апоптоза bcl-2 в плаценте экспрессируется в ворсинчатом и вневорсинчатом трофобласте, мезенхиме ворсин, в плацентарных макрофагах [4]. Степень экспрессии bcl-2 значительно снижается в синцитиотрофобласте после 32-й недели гестации, что происходит одновременно с замедлением роста плаценты. Возможно, это один из механизмов так называемого «старения» плаценты [7, 9]. Экспрессия маркера ki-67 представлена в синцитиотрофобласте, синцитиокапиллярных мембранах, клетках стромы, эндотелии сосудов, что свидетельствует о высокой пролиферативной активности этих элементов [6]. Однако по данным Т.Д. Задорожной и соавт. (2012) реакция на kі-67 в клетках синцитиотрофобласта в третьем триместре была отрицательная [5].
При беременности, не осложненной ПЭ (табл. 5), маркеры про- и антиапоптоза (bс1-2, Р53), клеточной пролиферации (ki-67) были выявлены во всех исследованных нами структурах плаценты (симпластотрофобласт, эндотелий капилляров, макрофаги стромы ворсин). Экспрессия bcl-2 и Р53 в макрофагах стромы ворсин была значительно выше по отношению к симпластотрофобласту и эндотелию капилляров стромы ворсин. В то же время экспрессия ki-67 в симпластотрофобласте значительно превышала таковую в эндотелии капилляров и макрофагах стромы ворсин.
Данные литературы о состоянии про- и антиапоптозных процессов, клеточной пролиферации в плаценте при ПЭ неоднозначны и часто противоречивы. U. Jeschke и соавт. (2006), D. Staribratova и соавт. (2005) при ПЭ зарегистрировали повышенную экспрессию маркера клеточной пролиферации ki-67 в трофобласте и строме ворсин [10, 11], однако в исследовании I.K. Prusac и соавт. (2011) экспрессия ki-67 в ворсинах трофобласта оказалась неизмененной [17]. U. Cali и соавт. (2013), L. Zhang и соавт. (2012), I. Mendilcioglu и соавт. (2011), I.K. Prusac и соавт. (2011) выявили активацию апоптоза в плаценте при ПЭ: увеличение процента апоптоза ядер в трофобластов, повышенная экспрессия маркера апоптоза каспазы-3 в трофобласте на фоне неизмененной или сниженной экспрессии bcl-2 [15–18]. По данным C.L. Whitehead и соавт. (2013), E. Padmini и соавт. (2012), A. Rolfo и соавт. (2012) при ПЭ плацентарная экспрессия показателей антиапоптоза bcl-2 и Mcl-1 была повышена на фоне снижения Р53 [12–14]. L. Mao и соавт. (2013), S.Z. Tomas и соавт. (2011) установили, что при ПЭ одновременно происходит активация анти- и проапоптических программ (маркеры каспаза-3 и bcl-2) [26, 27]. B. Huppertz и соавт. (2004) выдвинули интересную гипотезу о роли нарушения апоптоза в формировании ПЭ, согласно которой при нарушении баланса в системе апоптоз-пролиферация, ремоделирование синцитиотрофобласта происходит не физиологичным апоптозом, а апонекрозом, сопровождающимся высвобождением в материнский кровоток G_актина и ДНК с последующим повреждением эндотелия и развитием эндотелиальной дисфункции [28].
Согласно результатам нашего исследования, при умеренной ПЭ экспрессия bcl-2 в симпластотрофобласте (табл. 5) была существенно ниже, а в эндотелии капилляров и макрофагах стромы – выше 1-й группы. Показатели Р53 в симпластотрофобласте, эндотелии капилляров и макрофагах стромы оказались значительно ниже, а ki-67 в этих же структурах – выше группы контроля.
При тяжелой ПЭ (табл. 5, рис. 1, 2, 3 см. на вклейке) показатели bcl-2 в симпластотрофобласте были меньше, а в эндотелии капилляров – больше по сравнению с 1-й и 2-й группами. Экспрессия bcl-2 в макрофагах стромы была значительно выше, чем в симпластотрофобласте и эндотелии капилляров ворсин. Данный показатель в макрофагах стромы превышал аналогичный в группе контроля. Экспрессия Р53 в симпластотрофобласте, эндотелии капилляров и макрофагах стромы была значительно ниже, а ki-67 выше, чем в 1-й и 2-й группах. При этом в 3-й группе показатели Р53 и ki-67 в симпластотрофобласте и макрофагах стромы превышали таковые в эндотелии капилляров ворсин.
При изучении индексов р53/bcl-2 и ki67/P53 в контрольной группе нами зарегистрированы однонаправленные процессы во всех структурах плаценты: в симпластотрофобласте (0,94±0,06; 95% ДИ 0,80-1,08 и 0,70±0,04; 95% ДИ 0,61-0,79 соответственно), эндотелии капилляров (0,84±0,06; 95% ДИ 0,72-0,97 и 0,81±0,07; 95% ДИ 0,66-0,97), макрофагах (0,88±0,04; 95% ДИ 0,78-0,97 и 0,44±0,06; 0,38-0,50) преобладали процессы антиапоптоза, уровень клеточной пролиферации оказался меньше уровня апоптоза.
При умеренной ПЭ в отличие от группы контроля во всех структурах плаценты преобладали процессы клеточной пролиферации над процессами апоптоза (симпластотрофобласт ki-67/P53 1,46±0,06; 95% ДИ 1,34-1,59; эндотелий капилляров 2,04±0,13; 95% ДИ 1,76-2,32; макрофаги 1,04±,04; 95% ДИ 0,96-1,12; р1-2<0,001). В эндотелии капилляров (P53/bcl-2 0,50±0,02; 95% ДИ 0,45-0,56; р1-2<0,001) и макрофагах (P53/bcl-2 0,51±0,02; 95% ДИ 0,47-0,56; р1-2<0,001) были реализованы антиапоптические программы в сравнении с программами апоптоза, обратная ситуация зарегистрирована в симпластотрофобласте (P53/bcl-2 1,14±0,05; 95% ДИ 1,03-1,24; р1-2=0,032). Аналогичные изменения выявлены нами при тяжелой ПЭ (P53/bcl-2 и ki67/P53: симпластотрофобласт 1,88±0,16; 95% ДИ 1,53-2,22 и 3,88±0,19; 95% ДИ 3,48-4,27; эндотелий капилляров 0,19±0,01; 95% ДИ 0,14-0,21 и 7,93±0,85; 95% ДИ 6,13-9,73; макрофаги стромы 0,29±0,01; 95% ДИ 0,26-0,32 и 3,04±,14; 95% ДИ 2,74-3,35 соответственно), все показатели статистически (р1-3<0,001; р2-3<0,001) отличались от таковых 1-й и 2-й групп.
С целью изучения значения процессов про- и антиапоптоза, клеточной пролиферации на уровне плаценты при таких акушерских осложнений, как тяжелая ПЭ, суб- и декомпенсированная ХПН, гипотрофия и асфиксия новорожденного, использован корреляционный анализ Спирмена.
В симпластотрофобласте показатели P53/bcl-2 и ki67/P53 связаны положительными корреляционными связями с частотой тяжелой ПЭ (r=0,766 и r=0,848; p<0,001 соответственно), суб- и декомпенсированной ХПН (r=0,432 и r=0,506; p=0,004 и p=0,001), асфиксии новорожденного (r=0,324 и r=0,496; p=0,036 и p=0,001), искусственной вентиляции легких (r=0,346 и r=0,395; p=0,025 и p=0,01) и респираторного дистресс – синдрома новорожденного (r=0,552 и r=0,577; p<0,001); отрицательными – с массой новорожденного (r=-0,509 и r=-0,631; p<0,001).
В эндотелии капилляров показатель P53/bcl-2 связан отрицательными корреляционными связями с частотой тяжелой ПЭ (r=-0,733; p<0,001), суб- и декомпенсированной ХПН (r=-0,494; p=0,001), асфиксии новорожденного (r=-0,422; p=0,005), искусственной вентиляции легких(r=-0,364; p=0,018) и респираторного дистресс – синдрома новорожденного (r=-0,565; p<0,001); положительными – с массой новорожденного (r=0,524; p<0,001). Показатель ki67/P53 связан положительными корреляционными связями с частотой тяжелой ПЭ (r=0,848; p<0,001), суб- и декомпенсированной ХПН (r=0,561; p<0,001), асфиксии новорожденного (r=0,454; p=0,003), искусственной вентиляции легких (r=0,385; p=0,012) и респираторного дистресс – синдрома новорожденного (r=0,598; p<0,001); отрицательными – с массой новорожденного (r=-0,616; p<0,001).
В макрофагах стромы показатель P53/bcl-2 связан отрицательными корреляционными связями с частотой тяжелой ПЭ (r=-0,733; p<0,001), суб- и декомпенсированной ХПН (r=-0,521; p<0,001), асфиксии новорожденного (r=-0,427; p=0,005), искусственной вентиляции легких (r=-0,398; p=0,009) и респираторного дистресс – синдрома новорожденного (r=-0,634; p<0,001); положительными – с массой новорожденного (r=0,595; p<0,001). Показатель ki67/P53 связан положительными корреляционными связями с частотой тяжелой ПЭ (r=0,848; p<0,001), суб- и декомпенсированной ХПН (r=0,467; p=0,002), асфиксии новорожденного (r=0,446; p=0,003), искусственной вентиляции легких (r=0,394; p=0,010) и респираторного дистресс – синдрома новорожденного (r=0,623; p<0,001); отрицательными – с массой новорожденного (r=-0,572; p<0,001).
В результате корреляционного анализа установлено, что для указанной гестационной патологии характерны абсолютно однотипные плацентарные изменения: на уровне симпластотрофобласта происходит активация процессов клеточной пролиферации и апоптоза, а на уровне эндотелия капилляров и макрофагов стромы – процессов клеточной пролиферации и антиапоптоза, что, вероятно, свидетельствует об одинаковых механизмах развития данных акушерских осложнений.
Таким образом, согласно результатам нашего исследования процессы плацентарного апоптоза и клеточной пролиферации, несомненно, играют определенную роль в патогенезе формирования ПЭ, однако значение программ клеточного обновления в развитии этого синдрома требует, безусловно, дальнейшего изучения.
Выводы
При беременности, не осложнившейся ПЭ, в плаценте отмечены инволютивные (возрастные) изменения, компенсаторно-приспособительные процессы и в меньшей степени патологические изменения, проявляющиеся незрелостью ворсин хориона. Во всех структурах плаценты были активированы процессы антиапоптоза, уровень клеточной пролиферации был наименьшим.
При ПЭ, особенно тяжелой, значительно увеличивается степень дистрофических изменений стромы хориальной пластинки и синцитиального покрова ворсин, объем незрелых ворсин без синцитиальных почек и ишемических инфарктов в сочетании с мелкоочаговым характером компенсаторно-приспособительных реакций в виде гиперплазии капилляров стромы и пролиферации синцитиальных почек. В эндотелии капилляров и макрофагах стромы отмечена активация процессов клеточной пролиферации и антиапоптоза, но в симпластотрофобласте наряду с клеточной пролиферацией реализуются проапоптические программы, степень активности антиапоптоза резко снижена.
Выявленные корреляционные связи иммуногистохимических показателей клеточной пролиферации, про- и антиапоптоза плаценты с акушерскими осложнениями (суб- и декомпенсированная плацентарная недостаточность, тяжелая ПЭ, гипотрофия и асфиксия новорожденного) свидетельствуют об однотипных механизмах их развития.



