Аномальное прикрепление (врастание) плаценты (placenta accreta spectrum, PAS) – жизнеугрожающее осложнение беременности, одна из актуальных современных причин массивных кровопотерь и высокой материнской смертности [1].
Мировую известность данная проблема получила в 1927 г. благодаря канадскому специалисту Forester D.S., впервые опубликовавшему случай диагностики аномальной плацентации и описавшему гистологические нюансы инвазии ворсин плаценты в миометрий [2]. Спустя 10 лет Irving C., Hertig A.T. предложили термин «врастание плаценты», определив его как «аномальное частичное или полное прикрепление последа к стенке матки» [3]. Примечательно, что из 106 проанализированных ими случаев только у одной пациентки предыдущие роды были проведены путем кесарева сечения (КС). На сегодняшний день ситуация в корне изменилась. Большинство специалистов рассматривают PAS в качестве ятрогенного осложнения в связи с несоизмеримым скачком частоты КС в мире. По данным Росстата, количество абдоминальных родоразрешений в настоящее время продолжает неуклонно расти. Если в 2005 г. КС было проведено в 250,8 тыс. случаев, то к 2018 г. частота увеличилась почти вдвое (470,7 тыс.) [4]. Результатом данной динамики оказался прогрессивный рост массивной кровопотери и материнской смертности, что и определило PAS в качестве актуальной проблемы современного акушерства, а оптимизацию алгоритмов ведения – ее важнейшим аспектом.
Долгие годы единственным способом решения проблемы массивной кровопотери при PAS являлась гистерэктомия. Последние десятилетия отмечены активной разработкой альтернативы инвалидизирующему, органоуносящему алгоритму лечения PAS. Разработан ряд органосохраняющих технологий, целью которых явилось не только спасение жизни матери, но и сохранение ее анатомо-функционального здоровья и репродуктивного потенциала.
В 2004 г. Palacios Jaraquemada J.M. et al. предложили способ, основанный на иссечении участка миометрия с прикрепленной плацентой и последующей метропластике [5]. Это был по-настоящему инновационный прорыв, несмотря на то, что объем кровопотери продолжал оставаться высоким. Далее для усовершенствования подхода к лечению в процесс включались: использование адекватного гемостаза, отсепаровка мочевого пузыря, определение оптимальной локации разреза для извлечения плода и др.
В 2012 г. была предложена баллонная окклюзия внутренних подвздошных артерий (ВПА) с целью снижения кровопотери, однако это не решало задачу полноценного гемостаза. Метод был сложен в исполнении в связи с обязательным наличием дополнительного специального оборудования и специалиста с навыками рентген-эндоваскулярного хирурга [6].
В 2013 г. нашими соотечественниками было предложено использование временной баллонной окклюзии общих подвздошных артерий (ОПА) [7]. В 2015 г. авторы усовершенствовали метод путем смещения разреза для извлечения плода из дна в тело матки, модификации гемостатическими швами на плацентарном ложе, а также улучшения техники отсепаровки мочевого пузыря [8].
В 2016 г. вместо баллонной тампонады началась эпоха «турникетов». После средне-нижнесрединной лапаротомии, выполнения донного КС и ушивания полости матки без извлечения плаценты в широких связках на уровне перешейка формировали «окна» с двух сторон, через которые вдоль ребер матки накладывали турникетные жгуты из эластичных резиновых трубок, которые потом затягивали и фиксировали. Далее через эти же окна вокруг шейки проводили третий турникет, затягивали и фиксировали зажимом. После на ОПА накладывали прямые сосудистые зажимы и производили иссечение стенки матки в зоне врастания плаценты. Стенку матки ушивали, снимали зажимы с ОПА и удаляли турникеты, производили гемостаз [9].
Этими же авторами позднее был описан еще один метод, который характеризовался прошиванием на уровне сохраненной шейки матки П-образного шва на всю ширину в переднезаднем направлении. После этого накладывались турникеты на широкие связки, а ОПА временно пережимались (не более 40 минут) прямыми сосудистыми зажимами Сатинского. Далее уже по стандартной методике проводились резекция стенки матки с вросшей плацентой и метропластика [10].
В 2019 г. метод «турникетов» был несколько видоизменен: на извлеченной из брюшной полости матке выполняли ультразвуковое исследование для определения верхнего края плаценты, затем на уровне перешейка формировали «окна» и накладывали три турникетных жгута уже без натягивания. Далее над верхним краем плаценты проводили поперечный разрез и извлекали плод, затягивали турникеты. Потом из разреза производили иссечение стенки матки в зоне врастания с последующим кюретажем и установкой внутриматочного баллона. Дефект ушивали П-образными швами, снимали турникеты, проводили гемостаз [11].
В 2018 г. другой командой авторов была предложена альтернатива гемостазу: наложение компрессионных пневматических противошоковых штанов с целью компрессии артериального и венозного русла нижних конечностей, далее – временное лигирование ОПА турникетами и наружных подвздошных артерий для предотвращения обратного сброса крови в систему маточной артерии (МА) и сохранения депо артериальной крови в нижних конечностях. После вышеперечисленных манипуляций выполняли иссечение плаценты, метропластику и снятие турникетов [12].
В 2019 г. был предложен еще более упрощенный вариант наложения турникетов: после донного КС плод извлекали через разрез на матке. Далее его ушивали без извлечения плаценты. Иссекали несостоятельную стенку матки с маточной аневризмой и участком врастания и ушивали с использованием турникетного гемостаза. После этого во влагалище устанавливали баллон и раздували, пережимая влагалищные ветви МА и срамные артерии. Далее использовались два турникета: первый накладывался на уровне верхнего края маточной аневризмы (пережимались МА и яичниковые артерии (ЯА)), второй – на уровне нижнего края маточной аневризмы (пережимались МА) [13].
Значимое место в арсенале средств хирургического гемостаза занимают компрессионные швы на матку в различных модификациях [14–18], а также лигирование магистральных сосудов малого таза (МА, ЯА, ВПА).
Несмотря на существование всех вышеперечисленных гемостатических технологий, массивные кровотечения в настоящее время занимают уверенное 2-е место в структуре материнской смертности, лидируя среди причин высокого числа пациенток группы «near-miss» [18]. Женщины с PAS значимо пополняют эти группы. Таким образом, алгоритм ведения пациенток нуждается в дальнейшем совершенствовании.
Цель: cчитаем целесообразным представить собственный опыт ведения пациенток с беременностью, осложненной PAS.
Материалы и методы
За период с 2012 г. по 2023 г. в акушерских стационарах города (клинических базах кафедры акушерства и гинекологии №1 РостГМУ) нами были родоразрешены 54 пациентки с пренатально диагностированной PAS. Все пациентки были родоразрешены оперативно абдоминальным путем. Диагноз PAS во всех случаях был поставлен во время беременности при ультразвуковом исследовании; в 14/54 (25,93%) случаях подтвержден при магнитно-резонансной томографии; в 100% случаев диагноз был верифицирован интра- и постоперационно; степень инвазии определялась при гистологическом исследовании.
Репродуктивный анамнез всех пациенток был отягощен предыдущими оперативными родами (рубец на матке после КС, от 1 до 4) и артифициальными абортами (от 2 до 4).
Во всех анализируемых случаях оперативное родоразрешение было начато под региональным обезболиванием (эпидуральной анальгезией). В 7/54 случаях (12,96%) вследствие развития массивного кровотечения был применен эндотрахеальный наркоз (искусственная вентиляция легких).
Результаты
Наш 10-летний опыт ведения пациенток с PAS был условно разделен на 2 этапа, когда мы работали в рамках разных алгоритмов.
Первый этап – начальные годы практики, опыт курации первых 6/54 (11,11%) случаев PAS [19]. Первые 2 лапаротомии были выполнены по Пфанненштилю с последующим КС в нижнем маточном сегменте и метропластикой. На этапе работы в 2012–2016 гг. предпринималась попытка удаления плаценты рукой (в последующие годы данная тактика была полностью исключена из практики!). В 2 случаях степень врастания плаценты была верифицирована как PAS 2 по версии FIGO [20]. В 4 последующих случаях выполнялась нижнесрединная лапаротомия с последующим корпоральным КС. Перед попыткой отделения плаценты проводилось лигирование ВПА. В 2 из 4 случаев степень врастания плаценты гистологически была определена как PAS 1, в 1 – как PAS 2, в 1 – как PAS 3a. В 1 случае была произведена надвлагалищная ампутация матки, в 3 случаях – экстирпация матки. Средний объем кровопотери составил 1900 мл (от 1200 до 4000 мл). В 2 случаях интраоперационно проводилась реинфузия крови (система Sell Saver). Гемотрансфузия в послеоперационном периоде проводилась в 3/4 (75%) наблюдениях.
Учитывая большое количество органоуносящих операций при PAS, сопровождаемых значительной кровопотерей, за период 2012–2016 гг., в последующем нами была проведена коррекция применяемого алгоритма родоразрешения пациенток с PAS.
Так, в 48 случаях лапаротомия выполнялась из нижнесрединного доступа. В 3/48 (6,25%) операциях выполнялось корпоральное КС, в 45/48 (93,75%) случаях – донное КС с последующей метропластикой (рисунок).
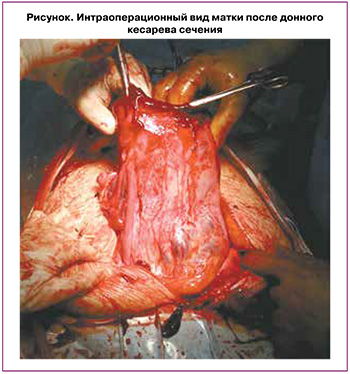
После рождения ребенка в 100% наблюдений проводилась обязательная перевязка ВПА и ЯА с обеих сторон. Попытки отделения плаценты и удаления последа не предпринимались. Проводилась поэтапная максимальная диссекция мочевого пузыря, после чего «неотделенная» плацента удалялась вместе с фрагментом миометрия при выполнении метропластики.
В 12/48 (25%) случаях послеоперационно степень врастания плаценты определена как PAS 1, в 10/48 (20,8%) – как PAS 2, в 8/48 (16,6%) – как PAS 3a. Средняя кровопотеря у этих женщин составила 1500 мл (от 1300 до 1900 мл).
В 5/48 (10,4%) случаях после перевязки ВПА и ЯА, проведения метропластики и полного ушивания матки из-за развившейся вторичной гипотонии матки были наложены компрессионные швы по ранее разработанной нами методике [18].
В 6/48 (12,5%) случаях была выполнена экстирпация матки, в 3/48 (6,25%) – в сочетании с везикопластикой при «врастании» плаценты в заднюю стенку мочевого пузыря. Глубина аномальной инвазии плаценты в 3 наблюдениях гистологически была определена как PAS 3b, еще в 3 – как PAS 3c. Средняя кровопотеря у этих женщин составила 3100 мл (от 2500 до 4000 мл).
Во всех анализируемых 48 случаях хирургического лечения PAS интраоперационно проводилась реинфузия крови (система Sell Saver).
По данным Bergmann R.L. et al., в послеоперационном периоде анемия сопровождается снижением физической работоспособности (усталостью, одышкой, сердцебиением), повышенным риском развития инфекции, нарушением лактации, снижением когнитивных способностей, эмоциональной нестабильностью и депрессией, требующими медикаментозной коррекции [21]. В послеоперационном периоде гемотрансфузия проводилась у 5 пациенток (5/48, 10,4%). В комплексной антианемической терапии нами использован недекстрановый высокодозный препарат карбоксимальтозат железа. Препарат вводился внутривенно капельно (инфузионно) в максимальной однократной дозе до 1000 мг железа (максимально 20 мг железа/кг массы тела) однократно, как правило, на 2-е сутки послеоперационного периода. Нами отмечен положительный эффект представленного подхода комплексной терапии постгеморрагической анемии.
Выводы
Оптимальный способ лапаротомии при PAS – нижнесрединный доступ.
Оптимальный способ КС при PAS – донная модификация.
При наличии признаков PAS попытки отделения плаценты должны быть исключены.
После рождения ребенка показано лигирование ЯА и ВПА.
В случае развития вторичной гипотонии матки после ее ушивания возможно наложение компрессионных швов.
Интраоперационно целесообразно проведение реинфузии крови.
В послеоперационном периоде необходимо проведение антианемической терапии с использованием современных препаратов железа для парентерального введения.



