В отличие от регистрируемого в последнее десятилетие снижения смертности от сердечно-сосудистых заболеваний (ССЗ) у мужчин, сердечно-сосудистая смертность у женщин остается стабильной или устойчиво повышается; прогнозируется дальнейший рост смертности среди женщин в связи с постарением населения [1, 2]. Известно, что женщины репродуктивного возраста достоверно реже и менее тяжело страдают основными ССЗ, что обусловлено защитным влиянием на сердечно-сосудистую систему женских половых гормонов. Снижение их уровня в постменопаузе приводит к широкому спектру метаболических и гемодинамических нарушений, способных оказывать неблагоприятное влияние на степень сердечно-сосудистого риска [3].
Накопление целого ряда факторов риска ССЗ у женщин после наступления менопаузы служит одним из обоснований концепции менопаузального метаболического синдрома (МС) [4, 5]. МС у женщин ответственен за возникновение половины всех сердечно-сосудистых событий и является более значимым фактором риска, чем у мужчин. Вместе с тем, МС является обратимым состоянием и при соответствующем лечении можно добиться исчезновения или, по крайней мере, уменьшения выраженности его проявлений [6].
Широкая распространенность и междисциплинарность проблемы МС в постменопаузе диктует необходимость выработки врачами любой специальности общей совместной стратегии, направленной на сохранение здоровья женщины. И в этой связи период менопаузального перехода и ранняя постменопауза являются наиболее оптимальными периодами для начала превентивных мер – формирования здорового образа жизни и назначения менопаузальной гормональной терапии (МГТ). Однако до сегодняшнего дня использование МГТ для коррекции климактерического синдрома у женщин с сопутствующими метаболическими нарушениями остается неоправданно низким, как и долговременная приверженность такой терапии из-за возможных ее осложнений.
Доза и длительность МГТ должны соответствовать целям лечения, обеспечивать безопасность и подбираться индивидуально. Побочные эффекты и переносимость комбинированных препаратов для МГТ во многом определяются свойствами прогестагенного компонента, что представляется особенно важным при использовании у женщин с сопутствующими метаболическими нарушениями [7, 8]. Однако до сегодняшнего дня в силу определенных обстоятельств МГТ остается предметом научных споров, касающихся не только проблем сердечно-сосудистой безопасности такой терапии, но и фобий пациенток, что послужило поводом для выполнения данного исследования.
Целью данного исследования стала оценка сердечно-сосудистой безопасности длительного применения низкодозовой комбинации 1 мг 17β-эстрадиола (E2) и прогестина – 2 мг дроспиренона (ДРСП) у женщин в ранней постменопаузе.
Материал и методы исследования
В исследование были включены 162 женщины периода ранней постменопаузы с различными проявлениями климактерического синдром в возрасте 52,5 (48,0;56,0) года. После получения письменного согласия на участие в исследование все обследуемые в дальнейшем были разделены на 2 группы: 1-ю группу (основная группа) составили 84 пациентки, которым совместно с гинекологом-эндокринологом по клиническим показаниям была назначена для непрерывного комбинированного режима МГТ 1 мг E2/2 мг ДРСП 1 раз в сутки ежедневно; во 2-ю группу (группу контроля) вошли 78 женщин, не получавших МГТ.
Решение о продолжении МГТ или отказе от нее принималось индивидуально и было отдано на усмотрение хорошо информированной пациентки и врача с учетом объективной оценки индивидуального баланса пользы и риска, согласно существующим рекомендациям [7, 8].
Протокол исследования был одобрен комитетом по этике ФГБОУ ВО Саратовский ГМУ им. В.И. Разумовского Минздрава России. Длительность терапии составила 5,2 (крайние значения от 4,8 до 5,7) года. Динамическое наблюдение за женщинами, принимающими МГТ, осуществлялось в сроки, установленные существующими рекомендациями [7, 8].
Критериями исключения являлись клинические проявления атеросклероза, ранее диагностированный сахарный диабет 1-го и 2-го типа, развитие артериальной гипертонии в репродуктивном периоде и симптоматическая артериальная гипертония, онкологические заболевания, преждевременная и ранняя менопауза, гистеровариэктомия, тяжелые соматические заболевания, курение на момент исследования и в анамнезе, противопоказания к приему МГТ.
Для оценки степени избыточной массы тела или ожирения вычисляли индекс массы тела (ИМТ) – масса тела (кг)/рост (м²). Выраженность абдоминального ожирения определяли косвенно по величине окружности талии (ОТ) и коэффициенту – окружность талии/окружность бедер (ОТ/ОБ).
Состояние углеводного обмена оценивали по уровню глюкозы венозной плазмы натощак и по результатам перорального глюкозотолерантного теста.
Степень тяжести климактерического синдрома (нейровегетативных, психоэмоциональных и обменно-эндокринных нарушений) оценивали в баллах модифицированного менопаузального индекса (ММИ) Куппермана–Уваровой.
Для оценки безопасности проводимой МГТ исследовали показатели гемостаза с оценкой функционального состояния его сосудистого звена. Для определения антитромбогенной (антиагрегационной, антикоагулянтной и фибринолитической) активности сосудистой стенки использовали манжеточную пробу, основанную на создании кратковременной локальной ишемии при окклюзии сосудов плеча манжеткой сфигмоманометра по методике В.П. Балуда и соавт. [9].
Агрегацию тромбоцитов определяли при помощи лазерного анализатора агрегации «Биола», г. Москва. В качестве индуктора агрегации использовался аденозиндифосфат (АДФ) в конечной концентрации 2,5 мкМ. Прогрессивную активность антитромбина III (АТIII) и фибринолитическую активность (стимулированный XII-а зависимый эуглобулиновый лизис) плазмы определяли с помощью набора реактивов фирмы «Технология-Стандарт». Суммарную антиагрегационную и фибринолититческую активность сосудистой стенки выражали в виде индексов – отношение показателей степени агрегации тромбоцитов и времени фибринолиза до и после окклюзии сосудов плеча; суммарную антикоагулянтную активность сосудистой стенки выражали индексом в виде частного от деления прогрессивной активности антитромбина III после наложения манжеты на его активность до наложения манжеты.
Исследование антигена фактора Виллебранда (vWF:Ag) проводили в плазме крови высокочувствительным количественным методом твердофазного иммуноферментного анализа, наборами ELISA (США) по инструкции.
Завершили исследование 69 женщин основной группы и 66 женщин группы контроля. Оценку долгосрочной эффективности лечения (кардиопротективные эффекты МГТ) проводили по регистрации новых случаев артериальной гипертонии, сахарного диабета и/или других вариантов нарушений углеводного обмена.
Исследования рисков MГT были сосредоточены на таких событиях, как рак молочной железы и рак эндометрия, венозная тромбоэмболия, инсульт и инфаркт миокарда.
Статистическая обработка данных выполнена с помощью программы Statistica 10.0. В случае нормального распределения изучаемые признаки представлены в виде M±SD и в виде медианы и интерквартильного интервала [Ме (25%;75%)] если изучаемые признаки не имели нормального распределения. Для качественных показателей вычисляли абсолютные и относительные частоты. При анализе межгрупповых различий количественных показателей использовался в случае нормальных распределений t-критерий Стьюдента и непараметрический критерий Манна–Уитни, если изучаемые признаки не имели нормального распределения. Для выявления существующих различий по качественным признакам использовали точный критерий Фишера, критерий χ2. Отношение шансов рассчитывали с использованием четырехпольных таблиц. Различия считались значимыми, если 95% доверительный интервал не включал значение 1,0. Критический уровень значимости в исследовании принимался р<0,05.
Результаты и обсуждение
Клиническая характеристика женщин, включенных в исследование представлена в табл. 1.
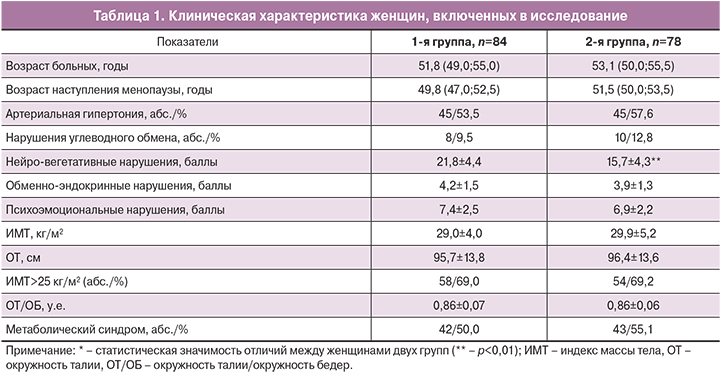
Существенных различий между женщинами двух групп по основным анализируемым показателям не выявлено. Более половины женщин имели артериальную гипертонию, длительность которой составила 1,3 (0,6;2,5) года. У половины женщин был диагностирован МС.
Несмотря на схожую структуру жалоб женщин двух групп, тяжесть климактерических проявлений по результатам анкетирования ММИ у женщин основной группы была более выражена, что также явилось дополнительным фактором обоснованности назначения МГТ (табл. 1).
Важным свойством ДРСП является его способность воздействовать на висцеральную жировую ткань и дифференцировку адипоцитов, что препятствует увеличению объема висцерального жира [10].
В проведенном нами исследовании установлено достоверное снижение ИМТ на фоне приема МГТ на протяжении всего периода наблюдения. Снижение ИМТ к окончанию исследования отмечено у 23 (33,3%) пациенток в среднем на 2,6 кг/м2, у 41 (59,4%) пациентки масса тела не изменялась и лишь у 5 (7,2%) вес увеличился на 2,1 кг/м2.
У женщин контрольной группы наблюдался иной характер изменений – достоверное увеличение ИМТ к окончанию исследования. Повышение ИМТ к окончанию исследования установлено у 45 (68,2%) женщин в среднем на 3,4 кг/м2, снижение массы тела выявлено лишь у 7 (10,6%) пациенток, а неизменной масса тела оставалась у 14 (21,2%) женщин.
На фоне длительной МГТ 1 мг E2/2 мг ДРСП отмечено изменение выраженности висцерального ожирения. У женщин основной группы установлено достоверное снижение ОТ и отношения ОТ/ОБ на протяжении всего периода наблюдения. К окончанию исследования снижение ОТ установлено у 27 (39,1%) женщин в среднем на 3,1 см, отсутствие изменений ОТ – у 34 (49,3%) женщин, увеличение ОТ выявлено только у 8 (11,6%) женщин в среднем на 3,4 см.
У женщин группы контроля отмечен иной характер изменений – достоверное возрастание величины этих показателей к окончанию исследования. Увеличение ОТ выявлено у 50 (75,7%) женщин в среднем на 3,7 см, отсутствие динамики – у 11 (16,7%) женщин и уменьшение ОТ установлено только у 5 (7,6%) пациенток.
В этом контексте уместно отметить наличие у женщин фобий относительно повышения массы тела на фоне проведения МГТ. Как показало наше исследование комбинация 1 мг E2/2 мг ДРСП, восполняя гормональный дефицит, способствует, если не снижению, то, по крайней мере, стабилизации массы тела.
На сегодняшний день недостаточно данных для рекомендации МГТ с целью профилактики сахарного диабета. В то же время сахарный диабет 2-го типа не является противопоказанием к назначению МГТ. Однако у женщин с сахарным диабетом 2-го типа повышен риск ишемической болезни сердца, он ассоциирован с дислипидемией, ожирением, артериальной гипертонией. В этой связи следует отдавать предпочтение МГТ с нейтральным гестагеновым компонентом, что делает актуальным использование выбранной комбинации у этой категории женщин [11].

В некоторых исследованиях была показана возможность МГТ оказывать положительное влияние на уровень инсулина крови, уменьшать выраженность инсулинорезистентности, однако ограничением этих исследований явилась их малая продолжительность. В этой связи вызывает интерес изучение долгосрочного влияния комбинированной МГТ 1 мг E2/2 мг ДРСП на частоту возникновения новых случаев сахарного диабета и других вариантов нарушений углеводного обмена [10, 12].
К окончанию исследования у пациенток основной группы отмечено достоверное уменьшение уровня глюкозы крови натощак с 5,5 (4,8;5,8) ммоль/л исходно до 5,1 (4,1;5,7) ммоль/л к окончанию исследования (p<0,05); отмечено снижение уровня постпрандиальной глюкозы при проведении теста толерантности к глюкозе с 6,8 (6,1;7,3) ммоль/л до 6,2 (5,3;6,6) ммоль/л соответственно (p<0,05). При этом изменение величины этих параметров сочеталось с уменьшением выраженности абдоминального ожирения.
У женщин группы контроля значимых изменений величины этих показателей не выявлено: уровень глюкозы крови натощак – 5,6 (4,9;6,0) ммоль/л исходно и 5,8 (5,2;6,5) ммоль/л – к окончанию исследования. При проведении теста толерантности к глюкозе – 6,9 (6,2;7,1) ммоль/л и 7,3 (6,3;8,2) соответственно, p>0,05 для всех значений.
За период проведения исследования у женщин на фоне МГТ было зарегистрировано два случая сахарного диабета 2-го типа и один случай нарушенной толерантности к глюкозе. У женщин группы контроля впервые диагностировано четыре случая сахарного диабета 2-го типа и два случая нарушенной толерантности к глюкозе.
Таким образом, длительное применение комбинации 1 мг E2/2 мг ДРСП ассоциируется с отчетливым уменьшением вероятности развития нарушений углеводного обмена (ОШ 0,42 при 95% ДИ 0,17;1,04).
Артериальная гипертония у женщин в течение долгого времени может оставаться не диагностированной и представлять существенную опасность для здоровья женщин. В литературе имеются указания на то, что адекватное лечение артериальной гипертонии у женщин в возрасте старше 55 лет связано со снижением фатальных и нефатальных цереброваскулярных событий на 38% [13].
Некоторыми исследователями была показана возможность использования МГТ в комплексном лечении климактерических расстройств у пациенток с артериальной гипертонией. Наличие у ДРСП антиминералкортикоидной активности определяет его главное преимущество при использовании у женщин с артериальной гипертонией, поскольку, влияя на активность ренин-ангиотензин-альдостероновой системы, он уменьшает задержку жидкости и натрия, оказывает нормализующее влияние на уровень артериального давления [14, 15].
Однако ограничением большинства из этих исследований являлась недостаточная длительность наблюдения. Нами была проведена оценка суточного профиля АД, изучена частота возникновения новых случаев артериальной гипертонии на фоне МГТ, что служило одним из критериев оценки клинической эффективности данной комбинации.
При первичном обследовании у 90 (55,5%) постменопаузальных женщин установлена артериальная гипертония, при этом регулярную антигипертензивную терапию не получала ни одна из женщин. У 18 (40%) пациенток основной и у 19 (42,2%) женщин контрольной групп диагноз артериальной гипертонии был установлен впервые.
Большинству пациенток для достижения целевых значений АД потребовалась комбинированная антигипертензивная терапия: к окончанию исследования только 16 (35,5%) женщин основной группы и 14 (31,1%) женщин группы контроля для достижения целевого уровня АД использовали монотерапию.
К окончанию исследования целевого уровня АД достигли 29 (72,5%) женщин основной группы и 29 (65,9%) женщин группы контроля (критерий χ2=0,43, p>0,05). Среди окончивших исследование женщин у 40 (57,9%) женщин основной группы и у 44 (72,1%) пациенток группы контроля выявлена артериальная гипертония. Таким образом, отмечена отчетливая тенденция к увеличению частоты артериальной гипертонии у женщин, не получавших МГТ (ОШ 0,69 при 95% ДИ 0,34;1,38). Возможно, одним из ограничений проведенного исследования является недостаточное число наблюдений, что не позволило получить достоверных отличий.
В настоящее время имеется мало информации о суточном профиле АД на фоне МГТ. Исходно достоверных отличий в частоте встречаемости различных вариантов суточного профиля АД у женщин обеих групп выявлено не было. У женщин на фоне комбинированной МГТ отмечена нормализация суточного профиля систолического и диастолического АД за счет уменьшения числа пациенток с избыточным снижением АД в ночные часы и ночной артериальной гипертонией и увеличением числа пациенток с нормальным суточным профилем АД и недостаточным его ночным снижением, что является более благоприятным фактором (рис. 1).
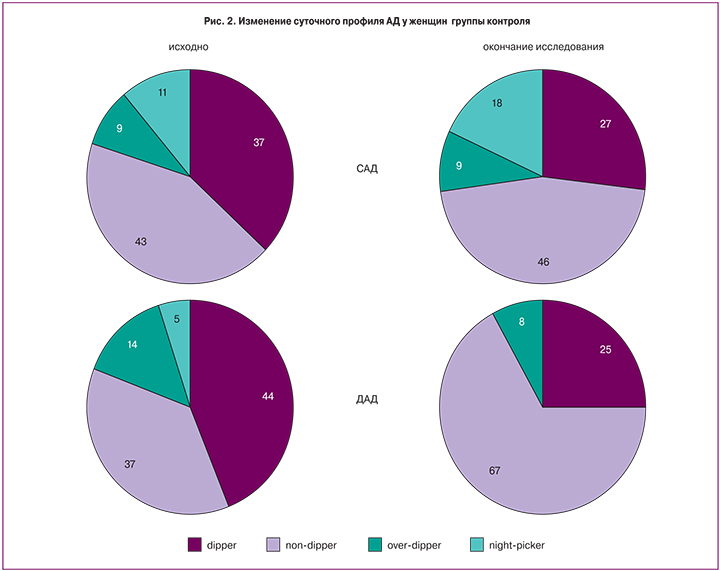
Иные изменения суточного профиля АД отмечены у женщин группы контроля – к окончанию исследования установлено уменьшение числа пациенток с нормальным суточным профилем АД и увеличение числа женщин с недостаточным ночным снижением АД и ночной артериальной гипертонией (рис. 2).
Завершили исследование 69 женщин основной группы и 66 женщин группы контроля. В 8 случаях у пациенток основной группы выявлены противопоказания к дальнейшему приему МГТ, в 4 случаях – отказ от дальнейшего участия в исследовании из-за опасений пациенток длительного приема гормональной терапии, в 3 случаях – потеря связи с больным в связи с переездом на другое место жительства.
Считается, что гормонотерапия создает некоторое гиперкоагуляционное состояние, однако интерпретация результатов затруднена вследствие сочетания противоположных эффектов эстрогенов и прогестинов, входящих в состав комбинаций. В этой связи большое значение могут играть не только низкая доза эстрогена, но и характеристики прогестагена в составе комбинированного режима МГТ [16].
Учитывая возможность повышения риска развития сосудистых осложнений на фоне МГТ, проведена оценка показателей гемостаза у пациенток обеих групп. Сосудистый эндотелий обладает высокой тромборезистентностью и играет важную роль в сохранении жидкого состояния циркулирующей крови. Вместе с тем, эндотелий обладает уникальной способностью менять свой антитромботический потенциал на тромбогенный при повреждении сосудистой стенки; при этом сосудистая стенка утрачивает тромборезистентность, что существенно увеличивает риск развития тромбоза.
Результаты исследования антитромбогенной активности сосудистой стенки на фоне приема МГТ представлены в табл. 2.
Исходно достоверных отличий АДФ-индуцированной агрегации тромбоцитов до и после проведения манжеточной пробы у женщин обеих групп выявлено не было. Результаты манжеточной пробы свидетельствуют о сниженной антиагрегационной активности сосудистой стенки (ААСС).
К окончанию исследования изменение ААСС у женщин обеих групп значимо отличались. У женщин на фоне приема МГТ существенных изменений ААСС не выявлено, а у пациенток группы контроля установлено снижение антиагрегационного потенциала сосудистой стенки, что выражалось в увеличении индекса ААСС.
Исходно значимых отличий антикоагулянтной активности сосудистой стенки (АКАСС) у женщин обеих групп отмечено не было. К окончанию исследования АКАСС у женщин обследуемых групп существенно не отличалась и характеризовалась достоверным увеличением активности АТ III в ответ на окклюзию сосуда.
Исходно фибринолитическая активность плазмы крови у женщин обеих групп значимо не отличалась. После кратковременной окклюзии сосуда фибринолитическая активность крови у обследованных женщин оставалась без изменений, что может указывать на сниженную способность сосудистой стенки синтезировать и выделять в кровоток компоненты системы фибринолиза, поддерживающие его активность.
К окончанию исследования у женщин на фоне приема МГТ отмечено увеличение фибринолитической активности сосудистой стенки (ФАСС), что выражалось в увеличении индекса ФАСС, а у женщин контрольной группы значимых изменений ФАСС не выявлено.
У женщин основной группы отсутствовали изменения уровня vWF:Ag на протяжении всего периода наблюдения, а у женщин группы контроля отмечено повышение уровня vWF:Ag.
Таким образом, изменения уровней маркеров функциональной активности эндотелия могут указывать на отсутствие негативного влияния на эндотелий сосудов проводимой комбинированной МГТ 1 мг E2/2 мг ДРСП.
За весь период наблюдения серьезных осложнений МГТ, включающих развитие онкологических заболеваний, выявлено не было. В целом переносимость терапии была удовлетворительной. Не было отмечено увеличения риска развития венозного тромбоза и эмболий, ишемического инсульта и случаев острого коронарного синдрома. В качестве положительного момента следует отменить достоверное уменьшение концентрации фибриногена крови у пациенток основной группы к окончанию исследования.
Заключение
Хотя МГТ не показана в настоящее время в качестве профилактики ССЗ, тем не менее, ее применение при наличии показаний и отсутствии противопоказаний обладает дополнительным положительным влиянием на сердечно-сосудистый риск у женщин в ранней постменопаузе с климактерическим синдромом.
Результаты настоящего исследования продемонстрировали, что длительная МГТ, содержащая ДРСП, оказывает благоприятное влияние на метаболические нарушения, а именно способствует уменьшению абдоминального ожирения, оказывает благоприятное влияние на углеводный обмен и уровень АД, не оказывает негативного влияния на сосудистый эндотелий и плазменное звено гемостаза, при этом установлена хорошая переносимость и безопасность используемой комбинации.



