Первое описание извитости пупочного канатика, по мнению H.W. Edmonds [15], было выполнено Berengarius в 1521 г. Наряду с этим долгое время данная особенность строения пуповины не привлекала к себе внимания специалистов. Как заметил в 1967 г. N.J. Eastman [14], «наличие извитости пуповины не имеет никакого практического значения». Однако в дальнейшем, по мере совершенствования ультразвукового исследования (УЗИ) беременных, появилась возможность пренатальной диагностики аномалий пуповины и, соответственно, возрос интерес исследователей к проблеме ее извитости.
Считается, что формирование витков начинается примерно на 8–9 нед внутриутробного развития
[12], то есть в то время, когда отношение объема амниотической жидкости к размеру плода максимальное и плод имеет возможность свободно вращаться вокруг неподвижной плаценты. Число
витков практически не изменяется или незначительно возрастает по мере увеличения срока гестации. Во II и III триместрах формирование завитков минимально из-за ограничения подвижности плода [21]. При этом увеличение длины пуповины ведет не к возрастанию числа витков, а к повышению расстояния между ними. Общее число витков может достигать 40, однако описаны наблюдения
пуповины с 380 витками [2]. Наряду с этим корреляций между степенью извитости и объемом
Вартонова студня не установлено [19].
Направление витков пуповины определяется следующим образом: если витки направлены сверху слева вниз вправо при вертикальном положении пуповины (в виде левой части латинской буквы «V»), такая извитость считается левой или идущей против часовой стрелки. Если витки идут сверху справа вниз налево (правая часть латинской буквы «V»), то речь идет о правой извитости по часовой стрелке (рис. 1).
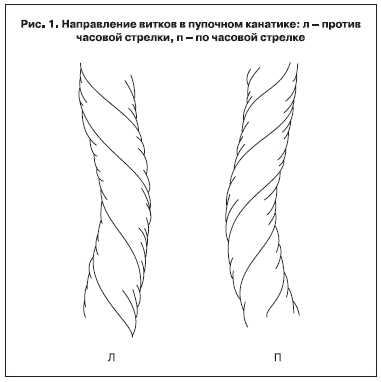
Закручивание пуповины влево, т.е. против часовой стрелки, встречается в 7 раз чаще. В то же время R.V. Lacro и соавт. [20] не выявили связи между направлением витков пуповины и тем, являются ли плод и мать правшами или левшами. При этом авторы показали, что пупочные канатики у близнецов могут быть закручены как в одну, так и в разные стороны, а степень извитости и число витков пуповины у них меньше по сравнению с одноплодной беременностью. Даже у монозиготных близнецов направление
закручивания пуповины может быть различным. Интересным является и тот факт, что в некоторых наблюдениях отмечалось одновременное закручивание пуповины в разных направлениях. Однако следует подчеркнуть, что направление извитости не имеет клинического значения.
При изучении 5 тыс. последов закручивание пуповины против часовой стрелки было выявлено в 79% наблюдений, при этом соотношение между закрученными против и по часовой стрелке пуповинами составило 3,7/1,0. В наблюдениях двоен пупочные канатики, закрученные против часовой стрелки, встречались в 61%, тогда как сочетание извитости по/против часовой стрелки было выявлено в 26% [3]. В отличие от предыдущих исследователей [20], W. Blackburn и соавт. [3] обнаружили совпадение в направлении закручивания пуповины у всех близнецов. В наблюдениях единственной артерии пуповины соотношение между извитостью по и против часовой стрелки составило 1,0/1,5 [2].
Точные причины формирования извитости пуповины не установлены. Ранее исследователи [30] полагали, что извитость пуповины может быть связана с вращением Земли, вследствие чего различные направления завитков возникают аналогично разным направлениям закручивания воды в водостоке в северном и южном полушариях. Однако впоследствии было установлено отсутствие различий между направлением закручивания пуповины в разных полушариях земного шара [2].
В настоящее время большинство исследователей считают, что закручивание пуповины является результатом двигательной активности плода, а отсутствие закручивания может свидетельствовать о снижении этой активности или нарушениях со стороны ЦНС. Извитость пуповины, видимо, также связана с гемодинамическими факторами и, прежде всего, с разницей давления в пупочных артериях различного диаметра (этим объясняют гиперизвитость пуповины у близнеца-реципиента при синдроме фето-фетальной гемотрансфузии) и некоторыми анатомическими особенностями, в частности наличием мышцы Роаха [5, 8, 29]. По данным J. Rana и соавт. [27], наличие множества завитков пуповины связано с употреблением матерью кокаина и высокой частотой преждевременных родов.
В 1994 г. T.H. Strong и соавт. [32] предложили рассчитывать индекс извитости пуповины (ИИП) как отношение между числом витков и ее длиной в сантиметрах. Средние нормальные значения ИИП составляют 1 виток на 5 см или 0,2±0,1 витка на 1 см. Подобные различия могут быть связаны с тем, что величина индекса при нормальной беременности зависит от срока гестации и от участка пуповины, на котором проводится измерение: бóльшие значения ИИП отмечаются в участке, прилежащем к плодно-
му концу [4]. Пуповины женщин европеоидной расы более извитые, чем у чернокожих представительниц [33]. Кроме того, точная оценка ИИП часто затруднена, поскольку на орфологическое исследование поступает не вся пуповина, что делает невозможным измерение ее длины [22]. Тем не менее при значении ИИП выше 90-го центиля (>0.4) пупочный канатик считается гиперизвитым, ниже 10-го центиля (<0.1) – гипоизвитым.
К сожалению, большинство патологоанатомов не уделяют должного внимания нарушениям извитости пуповины. Видимо, это связано с тем, что в большинстве наблюдений гипер- и гипоизвитых пуповин никаких осложнений беременности и родов не наблюдается [29]. Тем не менее многие случаи стеноза пупочных сосудов связаны с той или иной степенью гиперизвитости пуповины. Достаточно часто гиперизвитость пуповины сочетается с тромбозом ее сосудов и сосудов хорионической площадки [2, 16], а также с нарушениями созревания плаценты [9].
В наблюдениях гиперизвитых пуповин чаще отмечались нарушения сердечного ритма у плода, чаще проводились оперативные роды по поводу дистресса плода, ниже была средняя масса ребенка при рождении и его гестационный возраст [27]. При гиперизвитости пуповины, по данным M.W. De Laat [7], повышается риск неблагоприятных исходов для новорожденных с низкой массой тела (для данного гестационного возраста), чаще отмечается внутриутробная задержка роста плода, асфиксия и ацидоз в родах [18, 25]. Гиперизвитость пуповины часто сочетается с врожденными пороками развития (трисомией), а также с наличием единственной пупочной артерии. Вследствие этого ИИП можно использовать для ориентировочной оценки перинатальных рисков [32].
В литературе имеются несколько противоречивые данные о зависимости кровотока в сосудах пуповины от ее извитости. По данным G.M. Dado и соавт. [6], извитость пуповины практически не влияет на кровоток по пупочным сосудам. В то же время R.K. Atalla и соавт. [1] установили, что имеется линейная зависимость между pH и PCO венозной и артериальной крови новорожденного и длиной пуповины, индексом ее извитости и другими структурными особенностями.
В связи с этим возникает вопрос о том, в каких случаях имеется патофизиологическая связь между аномальной извитостью пуповины и перинатальными осложнениями. Считается, что гипоизвитые пуповины более восприимчивы к образованию истинных узлов и, соответственно, к развитию острого нарушения тока крови по пупочным сосудам; при гиперизвитости сопротивление току крови со стороны сосудистой стенки выше, чем при протекании крови по прямым сосудам [31]. В исследовани-
ях, проведенных антенатально, установлено, что чем выше ИИП, тем выше объем и скорость тока крови, протекающей по вене пуповины, но ниже сопротивление току крови со стороны стенок пупочных артерий [26]. Следует отметить, что при высоком ИИП сосуды пуповины более восприимчивы к нарушениям тока крови при их сдавлении [6, 17].
Таким образом, по мере увеличения ИИП происходит повышение скорости тока крови по сосудам пуповины, благодаря так называемому «эффекту пульсометра». Эффект «поршня», или «пульсометра» объясняется следующим механизмом. Так как пульсация артерий и вен происходит в противоположных направлениях, то пульсация артериальной стенки может служить своеобразным поршнем, усиливаю-
щим кровоток по вене. При увеличении числа завитков повышается площадь контакта артерий
и вен и, соответственно, усиливается поршневой эффект [28]. Однако при очень высоком ИИП
усиливается сдавление сосудов и нарушается ток крови по ним, что ведет к развитию тромбоза фетоплацентарных сосудов [10].
В противоположность гиперизвитости в ряде наблюдений встречается отсутствие извитости пуповины. По мнению T.H. Strong и соавт. [31], прогноз течения беременности в таких наблюдениях неблагоприятен. Авторы установили, что извитость пуповины отсутствует в 4,3% наблюдений, которые характеризуются высоким уровнем перинатальной смертности и другими проблемами. По данным УЗИ, у 4,9% беременных выявляется отсутствие извитости пупочного канатика [27], что расценивалось авторами как признак возможных нарушений созревания плода. Однако метод внутриутробной оценки ИИП при УЗИ обладает низкой (не более 40%) чувствительностью при диагностике гипо- и гиперизви-
тых пуповин [7].
Показано, что извитость пуповины чаще отсутствовала в наблюдениях двоен вне зависимости от би- или монохориального типа [3]. В наблюдениях, когда имелось тесное прилежание плода к поверхности плаценты (прежде всего за счет амниотических спаек), отмечалось не только уменьшение длины пуповины, но и снижение ИПП вплоть до полного отсутствия завитков [2]. В литературе имеется описание аномалии плода с аномально короткой неизвитой пуповиной, вызывавшей снижение подвижности плода [13]. Подобная особенность пуповины встречалась в наблюдениях, когда вытянутые эмбрионы располагались в относительно узких дополнительных рогах матки, что мешает нормальному вращению эмбриона. Таким образом, можно сделать вывод о том, что завитки пуповины образуются в результате вращения эмбриона вокруг ее оси.
Малая извитость пуповины или ее отсутствие, уменьшение ее диаметра нередко сочетается с нарушением кровотока в пупочной вене, а также внутриутробной задержкой роста и дистрессом плода в родах [11]. При малой извитости пуповины часто отмечается ее аномальное прикрепление, что может быть причиной развития перинатальной патологии [22].
Существует множество исследований, связывающих аномалии извитости пуповины с различными перинатальными и постнатальными заболеваниями плода. Так, гипоизвитость часто сочетается с внутриутробной гибелью плода, низкими оценками новорожденного по шкале Апгар, врожденными пороками развития, оболочечным прикреплением пуповины и единственной артерией пуповины. При ИИП ниже 10-го центиля чаще встречаются хромосомные аномалии (трисомия), респираторный дистресс-синдром, окрашивание околоплодных вод меконием. Примечательно, что на ранних сроках гестации при синдроме Дауна (трисомия 21) по сравнению с нормальными плодами значительно чаще отмечаются неизвитые пуповины и большее содержание в них гиалуроновой кислоты [26]. Более
того, отсутствие извитости пуповины наблюдается у мертворожденных с различными хромосомными аномалиями и врожденными синдромами (например, синдромом Pena Shokeir). Именно поэтому малая извитость пуповины или ее отсутствие расцениваются в качестве прогностически неблагоприятных признаков [31]. Разная выраженность степени извитости в различных участках пупочного канатика также может приводить к внутриутробным осложнениям, в частности, обвитию неизвитого участка пуповины вокруг шеи или туловища, при этом оставшиеся сегменты пуповины характеризуются гиперизвитостью [23].
Собственное наблюдение.
Женщина М., 34 года, поступила в НЦ АГиП с диагнозом: Беременность 38–39 нед. Головное предлежание. Отеки беременных. Ожирение I степени. Миопия средней степени. Транзиторный
гипертиреоз. Первородящая 34 года. Предвестники родов. Из анамнеза известно, что 3 года назад произошел самопроизвольный выкидыш в сроке 12 нед. Настоящая беременность: I триместр – угроза выкидыша в сроке 8–9 нед (стационарное лечение), II триместр – уреаплазмоз (проводилось лечение), транзиторный гипертиреоз, III триместр – отеки беременных.
Состояние пациентки удовлетворительное, жалоб нет, зрение ясное. ЧСС 76 в мин, АД – 110/70 мм рт. ст., живот правильной овоидной формы, матка возбудима при пальпации, регулярной родовой деятельности нет. Положение плода продольное, предлежит головка плода, прижата ко входу в малый таз, сердцебиение ясное, ритмичное, 140–150 уд/мин. Шевеления плода ощущает хорошо. Околоплодные воды не изливались, выделения слизистые. Отеки голеней и стоп. При влагалищном исследовании наружные половые органы развиты правильно, влагалище нерожавшей, шейка матки
укорочена до 2 см, плотноватой консистенции. Цервикальный канал проходим для 1 пальца. Плодный пузырь цел. Предлежит головка плода, прижата ко входу в малый таз. Экзостозов с малом тазу нет, мыс недостижим.
При УЗИ визуализация органов и структур плода удовлетворительная, пуповина имеет три сосуда, без обвития, околоплодные воды на уровне верхней границы нормы. Плацента расположена на задней стенке матки, толщина ее 3,9 см, нижний край высоко от внутреннего зева.
В связи с отсутствием регулярной родовой деятельности решено проводить динамическое наблюдение за состоянием женщины и плода. На 2-й день после поступления пациентка предъявила жалобы на отсутствие шевеления плода. При аускультации сердцебиение плода не выслушивается. При УЗИ в полости матки визуализируется один плод в головном предлежании, сердцебиение его не определяется. При допплерометрии сосудов пуповины пульсация отсутствует.
На следующий день произошли самопроизвольные роды в головном предлежании. Родился мертвый доношенный мальчик массой 3172 г длиной 52 см.
На патологоанатомическое вскрытие доставлен плод мужского пола массой 3172 г, длиной 52 см, правильного телосложения, умеренного питания. Окружность головы – 35 см, окружность груди – 33,5 см. Кожные покровы бледно-синюшные, мацерированы. Волосы на голове длиной 1 см. Видимые слизистые оболочки красновато-розоватые. Хрящи ушных раковин мягкие. Подкожно-жировая клетчатка на груди и животе развита умеренно. Мышцы развиты умеренно. Яички опущены в мошонку. Пупочное кольцо располагается на границе средней и нижней трети брюшной стенки. Пуповинный остаток у плода длиной 33 см с выраженными полнокровными артериями, отмечается гиперизвитость пуповины (14 витков на 33 см, – индекс извитости – 0,42 см) по часовой стрелке (рис. 2, см. на вклейке). Микроскопически в пуповине определяется расширение артерий с явлениями полнокровия и стаза, малокровие вены, плазматическое пропитывание Вартонова студня.
Органы грудной и брюшной полости расположены и сформированы правильно. В полостях тела небольшое количество серозно-геморрагической жидкости (посмертные изменения). Внутренние
органы по массе и размерам соответствуют сроку гестации. Отмечаются явления венозного полнокровия и аутолиза. Мелкоточечные кровоизлияния в серозные оболочки. Головной мозг с признаками отека. Мягкая мозговая оболочка полнокровная, тонкая, прозрачная, с мелкоточечными кровоизлияниями.
Плацента в виде двух фрагментов общей массой 450 г, размерами 20х16х2,5 см, на плодной поверхности небольшие участки фибриноида, на материнской поверхности небольшие участки
обызвествления. Пуповина прикреплена эксцентрично, ее длина 28 см без витков.
При гистологическом исследовании основную массу ворсинчатого дерева плаценты составляют терминальные ворсины, стволовые ворсины – немногочисленны, зрелые промежуточные – единичны, что соответствует доношенной беременности. Определяются многочисленные синцитиальные узелки. Многочисленный фибриноид расположен преимущественно между ворсинами, а также в зоне decidua basalis. Экстраплацентарные оболочки – без особенностей. Пуповина правильного строения, малокро-
вие сосудов.
Таким образом, в представленном наблюдении пупочный канатик характеризовался разной степенью извитости: со стороны плода ИИП равнялся 0,42, со стороны плаценты – без витков. На пограничном участке произошел перекрут пуповины, который привел к прекращению кровотока в ее сосудах с развитием внутриутробной гипоксии и, соответственно, гибели плода.



