Регулярный овуляторный менструальный цикл является жизненно важным показателем женского здоровья. Нарушения менструального цикла (НМЦ) включают множество симптомов и состояний, связанных с нарушением функции репродуктивной системы женщины. Международная федерация гинекологии и акушерства (FIGO) предложила термин «аномальное маточное кровотечение (АМК)» для описания любых расстройств, связанных с объемом, регулярностью, продолжительностью и/или частотой менструаций у небеременных женщин [1]. Термин АМК охватывает состояния, ранее известные как дисфункциональные маточные кровотечения, нерегулярные менструации, меноррагии и другие.
НМЦ является распространенной проблемой среди женщин в течение всего репродуктивного периода, особенно часто встречающейся у девочек-подростков и женщин в перименопаузе, когда НМЦ преимущественно связано с овуляторной дисфункцией. Заболеваемость НМЦ среди женщин репродуктивного возраста составляет около 20% [2], в то время как зарегистрированная распространенность НМЦ у подростков значительно выше и достигает 64,5% [3]. Более того, НМЦ имеет тенденцию становиться хронической проблемой здоровья для большинства подростков [4–7], что требует правильной диагностики и лечения.
Данные свидетельствуют о том, что установление полноценного менструального цикла может занять до 6 лет после менархе. В этот период могут наблюдаться нерегулярные (редкие) циклы и аномальные кровотечения. Из-за незрелости гипоталамо-гипофизарно-яичниковой оси во время пубертатного перехода овуляторная дисфункция затрагивает около 50% девочек-подростков [8–11]. Примерно к 18 годам нерегулярность менструального цикла обычно проходит, и продолжительность цикла, а также его характеристики становятся аналогичными тем, что наблюдаются у взрослых [8, 9]. Таким образом, нарушение регуляции менструального цикла в течение первых нескольких лет после менархе можно считать частью физиологического развития. Согласно последней классификации овуляторных нарушений FIGO, «в репродуктивном возрасте и при отсутствии беременности, лактации или использования фармакологических средств, таких как контрацептивные гормональные препараты, овуляция предсказуема и циклична» [11]. С этой точки зрения овуляторную дисфункцию нельзя считать нормой, поэтому нарушенный цикл следует восстанавливать с помощью эффективной и безопасной терапии [11], а не подавлять овуляцию.
НМЦ могут существенно влиять на качество физической, психологической и социальной жизни в подростковом возрасте, представляя собой значительную медицинскую проблему, на которую обратила внимание FIGO [7, 11–15]. АМК может быть связано с будущими репродуктивными проблемами и влиять на преждевременную смертность [16]. Поэтому лечение гинекологических заболеваний у подростков имеет решающее значение, и для этой возрастной группы необходимы соответствующие варианты терапии.
В России существует ограниченное количество одобренных вариантов лечения НМЦ с соответствующей доказательной базой у подростков. После отзыва разрешения на использование гестагенов у подростков в 2016 г. НМЦ у подростков часто лечат комбинированными оральными контрацептивами (КОК). Однако КОК не одобрены для лечения НМЦ и не могут быть методом выбора при АМК, поскольку они подавляют гормональную регуляцию менструального цикла, включая овуляцию. Более того, во время приема КОК у женщин наблюдается только регулярная менструальноподобная реакция, которая не может считаться физиологическим овуляторным менструальным циклом [17]. Врачи, имеющие ограниченные варианты лечения, предпочитают назначать КОК даже пациенткам, которые не хотят или не нуждаются в контрацепции, подвергая их неоптимальному лечению.
Напротив, препарат «Дюфастон» (дидрогестерон 10 мг, таблетки) одобрен для лечения пациентов с АМК, нерегулярным циклом, вторичной аменореей и дисменореей (среди прочих показаний), которые в настоящее время объединены под термином НМЦ согласно современной классификации PALM-COEIN. Эти нарушения в основном относятся к нарушениям овуляции (АМК-О) и могут быть скорректированы путем компенсации дефицита прогестерона или добавления гестагенов. Дидрогестерон обеспечивает патогенетическое лечение НМЦ без подавления овуляции. Дюфастон хорошо известен среди медицинских работников для пациентов подросткового возраста благодаря своему длительному присутствию на российском рынке и успешному применению у этих пациентов до 2016 г., когда допустимый к назначению возраст, согласно общей характеристике лекарственного препарата, был сужен ввиду новых нормативных требований.
В настоящее время существует ограниченное количество публикаций об эффективности гестагенов в подростковой популяции [18–23]. Большинство этих отчетов основано на небольшой выборке, устарели или охватывают узкую группу подростков (старше 12 лет). Тем не менее эти ограниченные отчеты утверждают, что дидрогестерон является хорошо переносимым и эффективным вариантом для лечения НМЦ у девочек до 18 лет. Однако необходимы дополнительные клинические данные о безопасности и эффективности дидрогестерона в этой возрастной группе.
Целью ретроспективной программы исследования реальных данных было получение новой информации об эффективности и безопасности применения дидрогестерона у девочек-подростков с НМЦ в реальной клинической практике в России. Это исследование потенциально может предоставить существенные доказательства эффективности и безопасности терапии для этой возрастной группы пациентов.
Материалы и методы
Дизайн исследования
Ретроспективное многоцентровое пострегистрационное наблюдательное исследование проводилось с использованием медицинских карт пациентов, участвующих в исследовании медицинских учреждений. В исследовании приняли участие 7 клинических центров, расположенных в Москве, Ростове-на-Дону, Ставрополе, Иркутске, Челябинске, Краснодаре и Чебоксарах. Протокол исследования был рассмотрен и одобрен независимыми этическими комитетами (НЭК) всех участвующих центров, а также НЭК ФГБУ «Национальный медицинский исследовательский центр акушерства, гинекологии и перинатологии им. академика В.И. Кулакова» Минздрава России. Исследование проводилось в соответствии с надлежащей клинической и фармакоэпидемиологической практикой и применимыми национальными регламентирующими документами.
Исследователи участвующих центров вручную отбирали медицинские карты пациентов. Выбранные данные оценивались на предмет соответствия критериям включения. Данные из соответствующих записей были анонимизированы и переданы в электронную систему сбора данных для дальнейшего статистического анализа.
Исследователи анализировали медицинские карты пациентов младше 18 лет, которые принимали таблетки дидрогестерона 10 мг (Дюфастон) в соответствии с национальной инструкцией по медицинскому применению в период с июня 2008 г. по декабрь 2016 г., то есть до того, как использование Дюфастона стало ограничено возрастом старше 18 лет. Поскольку единственным одобренным на момент исследования препаратом дидрогестерона в России являлся Дюфастон, другие торговые наименования не рассматривались. Медиана продолжительности лечения составила 84 дня (диапазон от 3 до 699 дней). У большинства пациенток (72,1%) продолжительность лечения дидрогестероном составляла от 1 до 3 циклов.
Преждевременное прекращение лечения было отмечено в 12 медицинских картах (1,2%), ни один случай не был связан с нежелательными реакциями. 3 (0,3%) отказа от лечения были связаны с его неэффективностью, 8 пациенток прекратили лечение по личным предпочтениям или по другим причинам.
Ретроспективные данные собирались с октября 2022 г. по апрель 2023 г.
Отбор пациентов
Для включения в исследование были отобраны медицинские карты следующих пациентов.
1. Пациентки младше 18 лет после менархе.
2. Таблетки дидрогестерона 10 мг были назначены в рамках реальной практики в соответствии с регистрационным удостоверением на момент назначения.
3. Медицинские записи содержали достаточно данных для включения в исследование и по крайней мере одну последующую оценку результата посещения лечащего врача через месяц или позже после назначения дидрогестерона.
Согласно национальным нормам, использование анонимных данных медицинских карт не считается обработкой персональных данных, поэтому информированное согласие пациента/законного представителя на использование информации из медицинских карт в целях данного исследования не требовалось. Пациенты были отобраны независимо от предшествующей и сопутствующей терапии.
Размер выборки
Исследование и первичный результат носили описательный характер, поэтому в исследовании не использовалась формальная статистическая гипотеза, требующая расчета размера выборки. Предполагаемое целевое количество записей, включенных в исследование, составляло 1000. Этот размер выборки считался достаточным для оценки первичных результатов, а также для проведения анализа подгрупп.
Первичный результат
Первичным результатом считался успех лечения, который определялся лечащим врачом при наличии регулярного менструального цикла после 1 и/или 3 циклов лечения.
Вторичный результат
Ключевым вторичным результатом был ответ, определяемый как наличие регулярных менструаций после 1 и/или 3 циклов лечения или сразу после окончания лечения. Другие вторичные результаты включали распределение пациенток по частоте менструаций, объему менструаций, частоте межменструальных и/или внеплановых маточных кровотечений, режимам приема дидрогестерона, назначаемого в реальной практике, а также продолжительности лечения.
Оценка безопасности на основании показателей частоты нежелательных лекарственных реакций (НЛР), зарегистрированных в медицинских записях, и показателей прекращения лечения из-за неэффективности или НЛР. Данные по безопасности оценивались в течение курса лечения и в течение 30 дней после приема последней дозы назначенного врачом лечения.
Статистический анализ
Описательная статистика использовалась для представления характеристик популяции, первичных и вторичных результатов. Отдельные назначения (курсы лечения) дидрогестерона считались обособленными случаями для целей статистического анализа. Для первичных и основных вторичных результатов (ответ на лечение и показатели нормализации менструального цикла) пациенты с отсутствующими значениями считались не отвечающими на лечение. Первичный результат описывался абсолютным числом и долей пациентов, с расчетом точного двустороннего 95% доверительного интервала Клоппера–Пирсона для биномиальной пропорции.
Непрерывные данные анализировались с использованием теста Вилкоксона, а тест Мак-Немара использовался для сравнения дихотомических данных. Все статистические тесты проводились в описательной манере, и значения p≤0,05 определялись как статистически значимые. Анализ данных проводился с использованием системы SAS версии 9.4 (SAS Institute Inc., Кэри, Северная Каролина).
Результаты
Характеристики исследуемой популяции
Всего в исследовании были использованы медицинские карты 1000 пациенток из 7 исследовательских центров, включая 19 пациенток, которым было проведено 2 курса лечения дидрогестероном (т. е. дидрогестерон использовался в двух отдельных случаях визитов к врачу). Таким образом, в отчете было описано 1019 курсов лечения дидрогестероном. Каждый курс терапии рассматривался как независимый случай. Описательная статистика представлена для 1019 случаев пациентов (далее именуемых случаями).
У всех пациенток было менархе. Продолжительность менструального цикла в днях была известна в 853/1019 случаях (83,7%).
Исходные демографические данные и история болезни участников исследования представлены в таблице 1.
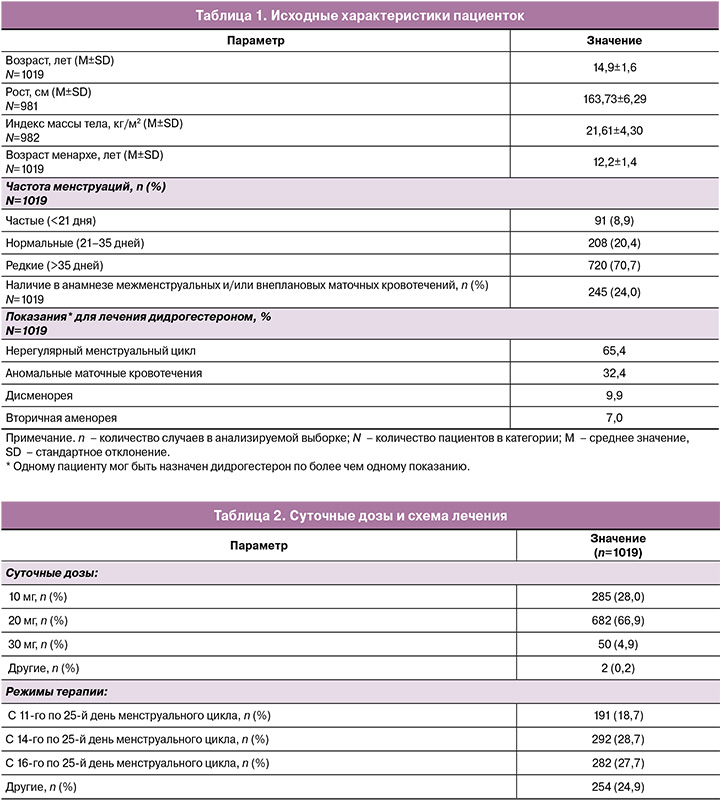
Сводка статистических результатов по суточным дозам дидрогестерона и схемам лечения представлена в таблице 2.
Показатели эффективности
Первичный результат
Успешность лечения нарушений менструального цикла варьировалась от 92,3 до 100,0% в зависимости от диагностического кода по Международной классификации болезней 10-го пересмотра (МКБ-10), которым кодировалось расстройство и при котором назначался дидрогестерон (рис. 1).
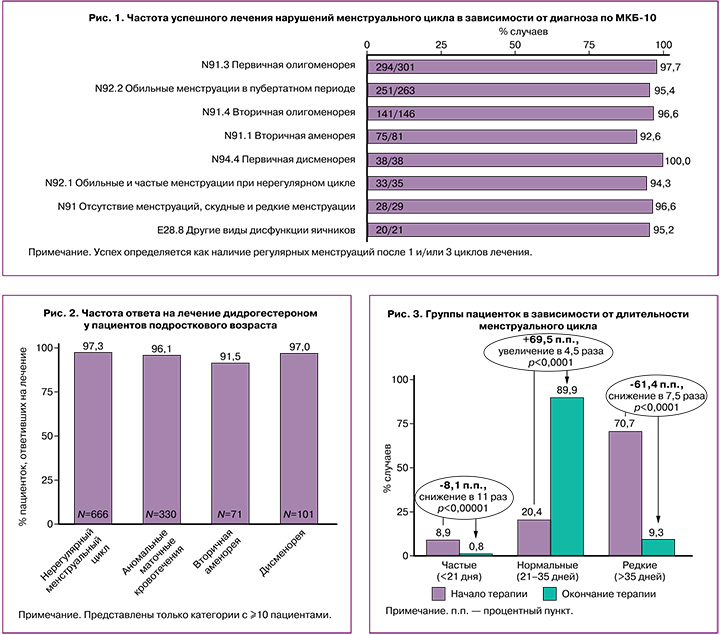
Вторичные результаты
Из 1019 случаев регулярные менструальные циклы в течение 1–3 циклов лечения или после его окончания были достигнуты у 987 (96,9%) пациенток. Показатели ответа варьировались от 91,5 до 100% в зависимости от кодов МКБ-10 (рис. 2). Показатели ответа были схожими независимо от возраста и индекса массы тела (ИМТ).
Изменение частоты менструаций представлено на рисунке 3. Исходно в 70,7% случаев менструации были редкими. К концу лечения доля пациенток с олигоменореей снизилась на 61,4% (p<0,0001). В то же время доля случаев с нормальной частотой менструаций увеличилась на 69,5% – с 20,4% до 89,9% (p<0,0001).
Применение дидрогестерона привело к уменьшению объема менструальной кровопотери с 65,9±22,0 мл на исходном уровне до 60,8±10,4 мл в конце лечения (p<0,0001).
Терапия после дидрогестерона
В целом только в 3,6% из 1019 случаев потребовалось дальнейшее лечение после курса дидрогестерона, включающее оральные контрацептивы (0,6%), экстракты зверобоя (0,4%) и нестероидные противовоспалительные препараты (0,4%). Примечательно, что гомеопатические средства после дидрогестерона применялись в 0,6% случаев.
Оценка безопасности
Нежелательные реакции были зарегистрированы в 3/1019 случаев (0,3%). Одна из них была классифицирована как серьезная из-за резко болезненной регулярной менструальноподобной реакции после отмены дидрогестерона, что потребовало госпитализации с подозрением на острый аппендицит. У пациентки, получавшей 30 мг суточной дозы, была обнаружена тератома яичника. Позднее исследователь уточнил, что сама тератома не имеет отношения к лечению дидрогестероном (является врожденным состоянием). Два других случая были связаны с астенией и зудящей сыпью.
Обычно регистрация нежелательных реакций в ретроспективных неинтервенционных исследованиях низкая. Это может быть связано с ретроспективным характером исследования, где интерпретация историй болезни пациентов может быть затруднена.
В 21 (2,1%) случае пациенты получали лечение анемии (препараты железа) во время лечения дидрогестероном, а в 2 (0,2%) случаях продолжили его после отмены дидрогестерона. В большинстве (13 из 21) этих случаев пациенты имели в анамнезе железодефицитную анемию или латентный дефицит железа.
Обсуждение
Редкие или частые менструации были зарегистрированы почти в 80% случаев. Нерегулярный менструальный цикл был показанием для назначения дидрогестерона в большинстве случаев (65,4%), в то время как 32,4% пациенток получали терапию для лечения других типов НМЦ. Примечательно, что сопутствующий эндометриоз присутствовал в ряде случаев (n=7, 0,7%), включая 2 случая (0,2%), в которых дидрогестерон назначался для терапии эндометриоза в качестве основного показания.
Анализ ретроспективных данных показал, что регулярные менструации после 1 или 3 циклов лечения были достигнуты в 95,8% случаев. Аналогичные показатели (96,9%) были зарегистрированы в отношении регулярной менструации после 1 или 3 циклов лечения и/или к концу лечения. Нормальная частота менструаций была достигнута у 89,9% пациенток к концу лечения по сравнению с 20,4% на исходном уровне. Показатели ответа варьировались от 91,5 до 100% в зависимости от исходного диагноза.
Таким образом, дидрогестерон оказался эффективным при различных проявлениях НМЦ в рамках утвержденных показаний в реальной клинической практике.
НЛР были зарегистрированы в 3 (0,3%) случаях, включая одно серьезное сопутствующее явление дисменореи, описанное как острая болезненная регулярная менструальноподобная реакция после отмены дидрогестерона, требующая госпитализации с подозрением на острый аппендицит.
В данном исследовании использовался ретроспективный дизайн, поскольку планировалось собрать и проанализировать данные с документально подтвержденным применением дидрогестерона в соответствии с местным разрешением на продажу и утвержденными показаниями до 12 декабря 2016 г., когда локальное разрешение на продажу было ограничено возрастом 18 лет и старше.
Это исследование имеет несколько ограничений, присущих его неинтервенционному ретроспективному дизайну. Возможность неправильной оценки состояния пациента существует во всех исследованиях, основанных на ретроспективных данных. Доказательства состояний и событий, основанные на сообщенных диагнозах и кодах, могут не отражать полную клиническую информацию. Медицинские карты пациентов содержат информацию о назначенных лекарствах, но невозможно определить, получали ли пациенты свои лекарства и следовали ли они рекомендациям. Также возможно получение неполных данных при использовании ретроспективных источников.
Ретроспективный дизайн исследования позволил провести анализ большой выборки. Насколько нам известно, это исследование представляет самую большую выборку подростков, лечившихся дидрогестероном при АМК. Tabaste1. J.L. et al. (1984) оценили эффект дидрогестерона 20 мг в день с 16-го по 25-й день цикла (3 цикла) у молодых женщин в постпубертатном возрасте (n=74), заключив, что общая эффективность была удовлетворительной [20].
Chomczyk I. et al. (1999) заявили, что низкодозированная терапия дидрогестероном была эффективна при болезненных менструациях, олигоменорее и/или АМК у девочек в возрасте от 12 до 17 лет (n=116) [19]. Тухватуллина Л.М. и соавт. (2007) в исследовании 52 девочек-подростков с первичной дисменореей указали, что применение дидрогестерона 20 мг в день с 16-го по 25-й день цикла привело к нормализации менструального цикла после одного месяца лечения почти у 20% пациенток, более того, большинство пациенток сообщили об уменьшении интенсивности менструальных болей [22].
Садуакасова Ш.М. и соавт. (2014) сообщили о нормализации менструального цикла у 87% из 32 девочек с дисменореей, получавших дидрогестерон по 20 мг в день в течение 6 месяцев [23]. В недавней статье (2022) Сальникова И.А. и соавт. заявили, что у 50 девочек-подростков дидрогестерон, назначаемый в дозе 20 мг в день с 16-го по 25-й или с 11-го по 25-й дни цикла для лечения АМК, привел к нормализации менструального цикла у 46,7 и 70% пациенток соответственно [21].
Общие результаты нашего исследования согласуются с другими отчетами об эффективности дидрогестерона при лечении НМЦ, полученными во время исследований с использованием препарата «Дюфастон».
В постмаркетинговом исследовании Trivedi N. et al. (2016) говорится об одном серьезном и 31 несерьезных нежелательных явлениях при изучении дидрогестерона (до ≥6 циклов) для терапии НМЦ у 910 женщин [24]. В открытом исследовании Taniguchi F. et al. (2019) сообщили о нежелательных реакциях у 31,8% взрослых японских женщин с дисменореей (n=44), использующих 5 мг дидрогестерона с 5-го по 25-й день цикла, сделав вывод об эффективности и безопасности лечения [25]. В недавнем отчете Wang L. et al. (2020) описано постмаркетинговое неинтервенционное исследование применения дидрогестерона 10 мг в день с 16-го по 25-й день цикла для лечения АМК-О у взрослых китайских женщин (n=114). Сообщается, что показатель успешности лечения составляет 80,9% [26].
Анализ имеющихся публикаций по популяциям, аналогичным выборке данного исследования у взрослых пациентов, позволяет сделать вывод, что полученные результаты по эффективности и безопасности применения дидрогестерона при НМЦ соответствуют данным других авторов. Имеющиеся данные по безопасности ограничены, однако не было выявлено никаких новых проблем безопасности у подростков в возрасте до 18 лет.
Заключение
Важно иметь эффективное лечение с благоприятным профилем безопасности для подростков, которое подходит для становления функции репродуктивной системы, не подавляет овуляцию, патогенетически обосновано и способствует репродуктивному и общему здоровью. Результаты этого ретроспективного исследования реальных данных показали, что использование дидрогестерона у девочек-подростков с НМЦ по показаниям «нерегулярный менструальный цикл», «аномальные маточные кровотечения», «вторичная аменорея» и «дисменорея» является как эффективным, так и хорошо переносимым в реальной клинической практике. Имеющиеся данные по безопасности ограничены, однако не было выявлено никаких новых проблем безопасности у подростков в возрасте до 18 лет. Дидрогестерон является патогенетически обоснованной терапией НМЦ у подростков женского пола с благоприятным профилем безопасности.



