Увеличение средней продолжительности жизни женщины в масштабах глобального старения населения определяет необходимость улучшения качества жизни женщин, находящихся в климактерическом периоде. По данным Всемирной организации здравоохранения, к 2030 году в мире будет около 1,2 млрд женщин в возрасте 50 лет и старше. В связи с этим проблема менопаузы требует особого внимания, так как ее проявления оказывают отрицательное влияние на качество жизни женщин, способствуя развитию кардио-васкулярных рисков, остеопороза, ухудшению когнитивных функций и появлению психологических расстройств [1, 2].
Климактерический период – физиологический период жизни женщины, в течение которого на фоне возрастных изменений организма доминируют инволюционные процессы в репродуктивной системе. Климактерический синдром (КС) – патологическое состояние, возникающее у части женщин в климактерическом периоде и характеризующееся нервно-психическими, вегетативно-сосудистыми и обменно-трофическими расстройствами, значительно ухудшающими качество жизни женщины. Управление симптомами КС, облегчение его проявлений означает управление процессами старения женского организма.
В настоящее время не вызывает сомнений тот факт, что менопаузальная гормональная терапия (МГТ) является самым эффективным методом коррекции климактерических расстройств. Международные общества по менопаузе рекомендуют МГТ как «терапевтический стандарт при лечении «приливов жара» средней и тяжелой степени в период менопаузы» [2–4].
Однако, несмотря на доказанную пользу, МГТ не получила в России достаточно широкого распространения. С одной стороны, у врачей нет полного доверия к МГТ, есть сомнения в ее безопасности, что можно назвать гормонофобией. С другой стороны, растет недоверие к классической (аллопатической) медицине со стороны больных, что можно назвать тенденцией последних лет, поскольку происходит это практически во всех странах. Пациенты требуют от традиционной медицины определенных – чаще абсолютных – гарантий как эффективности, так и безопасности лечения, и в результате все чаще обращаются к альтернативной медицине, которой многое прощают [2–6].
Среди негормональных средств для облегчения симптомов КС чаще всего применяют фитоэстрогены, к которым относятся следующие классы химических соединений: флавоны, изофлавоны (генистеин, дайдзеин, биоханин, формононетин), лигнаны (энтеролактон, энтеродиол), куместаны (куместрол). Изофлавоны в большом количестве содержатся в соевых бобах, горохе, других бобовых культурах, клевере; лигнаны обнаруживаются в масличных семенах (например, семенах льна), отрубях, цельных злаках, овощах, бобовых и фруктах; куместаны содержатся в клевере и люцерне [2–5, 7, 8].
Фитоэстрогены отличаются высокой биологической активностью: они обладают антиоксидантными свойствами; ингибируют протеинкиназы и ферменты, участвующие в метаболизме эстрогенов; влияют на транспорт ионов и глюкозы, синтез белков, пролиферацию клеток, ангиогенез и факторы роста. Фитоэстрогены стимулируют в печени продукцию глобулина, связывающего половые стероиды, что приводит к снижению биологической доступности не только эстрогенов, но и андрогенов, чей относительный избыток в постменопаузе неблагоприятен не столько по косметическим соображениям, сколько с точки зрения риска сердечно-сосудистых заболеваний. Показано, что фитоэстрогены положительно влияют на работу головного мозга, повышают уровень холестерина липопротеидов высокой плотности и понижают уровень холестерина липопротеидов низкой плотности, способствуют расширению коронарных артерий, подавляют гиперплазию эпителия молочных желез и эндометрия [2, 6, 7].
Наиболее близки к эстрогенам по структуре, действию и сродству к рецепторам изофлавоны, в частности, генистеин. В нативной форме генистеин не обладает биологическим эффектом, но после приема внутрь гидролизируется под воздействием кишечной микрофлоры и распадается на углеводный и неуглеводный компоненты. Последний, так называемый агликон, проявляет эстрогенную активность. Генистеин в активной форме (менорил) имеет важные преимущества: он поступает в организм уже в агликолевой форме и его метаболизм не зависит от состояния и качества микрофлоры кишечника. Взаимодействуя с эстрогеновыми рецепторами, фитоэстрогены частично блокируют связывание с ними эндогенного эстрадиола, поэтому, будучи намного слабее его, становятся антагонистами или агонистами в условиях соответственно высокого или низкого уровня эндогенных эстрогенов, то есть являются природными избирательными модуляторами эстрогеновых рецепторов. Избирательность действия объясняется также разным сродством к эстрогеновым рецепторам. Если сродство эстрадиола к рецептору эстрогенов принять за 100%, то сродство генистеина к α-рецепторам составит 5%, к β-рецепторам – 36%, то есть в отношении этих рецепторов активность генистеина сравнима с активностью эстрона. Пролиферативный эффект генистеина относительно слабый: геномный ответ клеток на эстрадиол наблюдается через 0,5 часа и сохраняется до 96 часов, а генистеин, также как и эндогенный эстрадиол, демонстрирует ранний, но кратковременный ответ, и поэтому не способен вызвать гиперплазию или гипертрофию эндометрия [2, 9].
Целью настоящего исследования стало изучить эффективность альтернативной терапии КС генистеином, синтезированным в активной форме.
Материал и методы исследования
Исследование выполнено в период 2014–2015 гг. на клинической базе кафедры акушерства и гинекологии Института последипломного образования ГБОУ ВПО Красноярский государственный медицинский университет им. проф. В.Ф. Войно-Ясенецкого Минздрава России. В исследовании приняли участие 60 женщин в возрасте 45–60 лет. На основании разработанных критериев включения и исключения были сформированы группы исследования. Критерии исключения из исследования – тяжелый КС (согласно менопаузальному индексу Куппермана).
Основную группу составили 30 женщин с легкой и умеренной тяжестью КС.

Критериями включения в исследование были: возраст пациенток от 45 до 60 лет; наличие симптомов КС легкой и средней степени тяжести (согласно менопаузальному индексу Куппермана); отказ от МГТ или противопоказания к МГТ.
Группа контроля включила в себя 30 женщин без значимых проявлений КС (согласно шкале Куппермана), считающих себя здоровыми и, по их мнению, не нуждающихся в лечении.
У всех участниц исследования было получено информированное согласие на проведение обследования и лечения.
 Исследование состояло из нескольких этапов. На первом этапе проводилось определение степени тяжести КС по шкале Куппермана и оценка качества их жизни по результатам унифицированного международного опросника. Дополнительно проводилось анкетирование пациенток по разработанной нами форме, которая включала жалобы, характерные для КС: головные боли, приливы, боли в суставах, слабость, усталость, нарушения сна, сердцебиение, снижение памяти, сухость во влагалище, снижение либидо; психоэмоциональные проблемы (сложности в общении; чувство тревоги, одиночества, беспокойства).
Исследование состояло из нескольких этапов. На первом этапе проводилось определение степени тяжести КС по шкале Куппермана и оценка качества их жизни по результатам унифицированного международного опросника. Дополнительно проводилось анкетирование пациенток по разработанной нами форме, которая включала жалобы, характерные для КС: головные боли, приливы, боли в суставах, слабость, усталость, нарушения сна, сердцебиение, снижение памяти, сухость во влагалище, снижение либидо; психоэмоциональные проблемы (сложности в общении; чувство тревоги, одиночества, беспокойства).
Обследование включало общеклинические, инструментальные методы: сбор анамнеза, систему объективного обследования, мониторинг АД, ультразвуковое исследование органов малого таза, молочной железы; рентгеномаммографию; лабораторные исследования. Осуществляли антропометрию — измерение роста и массы тела; индекс массы тела (ИМТ) определяли по G. Brey: ИМТ=масса тела (кг)/рост (м²).
С целью оценки степени тяжести КС использовался менопаузальный индекс Куппермана в модификации Уваровой – модифицированный менопаузальный индекс (ММИ). Согласно данной шкале, женщины разделяются на 3 группы – с легким, умеренным и тяжелым КС. Для уточнения степени тяжести КС выделены 3 группы симптомов. Первая группа – нейро-вегетативные симптомы (НВС), к которым относятся колебания АД, головные боли, онемение, сухость кожи либо потливость, сердцебиение, нарушения сна и приливы жара. К группе эндокринно-метаболических симптомов (ЭМС) относят ожирение, тиреоидную дисфункцию, сахарный диабет, фиброзно-кистозную мастопатию, мышечно-суставные боли и атрофию гениталий. Психоэмоциональные симптомы (ПЭС) включают в себя утомляемость, снижение памяти, слезливость, возбудимость, изменения аппетита, настроение и либидо. Каждая группа расстройств после анкетирования, опроса и осмотра пациентки набирает определенное количество баллов, которые суммируются. В зависимости от полученной суммы баллов определяется тяжесть КС: легкая: 12–34 балла; умеренная: 35–58 баллов; тяжелая: более 58 баллов.
Для оценки качества жизни женщин использовался унифицированный опросник SF-36 Health Status Surgery. Опросник отражает общее благополучие и степень удовлетворенности теми сторонами жизнедеятельности человека, на которые влияют состояние здоровья. SF-36 состоит из 36 вопросов, сгруппированных в восемь шкал: физическое функционирование, ролевая деятельность, телесная боль, общее здоровье, жизнеспособность, социальное функционирование, эмоциональное состояние и психическое здоровье. Показатели каждой шкалы составлены таким образом, что чем выше значение показателя (от 0 до 100), тем лучше оценка по избранной шкале. Из них формируют два параметра: психологический компонент (ПК) и физический компоненты (ФК) здоровья. При этом удовлетворительными считаются показатели, составляющие 50% и более – по физическому компоненту (ФК) и 50% и более по психическому компоненту (ПК).
Пациенткам основной группы было назначено применение препарата, содержащего генистеин в дозе 30 мг, по 1 капсуле 2 раза в день 90 дней (менорил). После 3 месяцев применения менорила проведено сравнение качества жизни и ММИ у пациенток основной группы до и после лечения.
Статистическая обработка результатов производилась в соответствии с общепринятыми методами медицинской статистики с использованием современных программ Statistica 6.0 и SPSS, Microsoft Excel 7 для Windows 98, Biostat. Показатели опросника MOS SF-36 оценивались по результатам шкалирования с использованием специальных кодов и ключей. Обработка полученных показателей проводилась с оценкой среднего значения показателей (М), средней величины квадратичного отклонения (Е), показателя средней ошибки (m), критерия Стьюдента (t) для средних величин, вероятности ошибки (Р). Различие между сравниваемыми величинами признавалось достоверным при р<0,05 (95% уровень достоверности).
Результаты и обсуждение
Средний возраст исследованных женщин основной группы составил 52,7±1,8 года, в группе контроля – 52,5±1,7 года (р>0,05). Средняя продолжительность предъявляемых жалоб, характерных для КС, в основной группе составила 3,1±0,1 года. В ходе исследования отмечено, что у каждой третьей пациентки исследованных групп проведена гистерэктомия без придатков, что составило 26,6% (n=8) и 33,3% (n=10) (р>0,05) соответственно. ИМТ у пациенток группы контроля – 32,9±1,4 кг/м2, в основной группе 30,9±1,0 кг/м2 (р>0,05). Каждая третья пациентка имела вредные привычки; курение отмечено в 33,3% (n=10) среди женщин основной группы и в 36,6% (n=11) в группе контроля (р>0,05). Интеллектуальным трудом занимались 63,6±2,1% (n=19) и 73,3±2,4% (n=22) женщин основной и контрольной групп (р>0,05), в физическом труде занято 36,6±1,2% (n=11) и 26,6±0,9% (n=8) (р>0,05) соответственно. Заболевания органов кровообращения, органов дыхания, желудочно-кишечного тракта встречались у каждой 3-й женщины как в основной группе, так и в группе контроля.
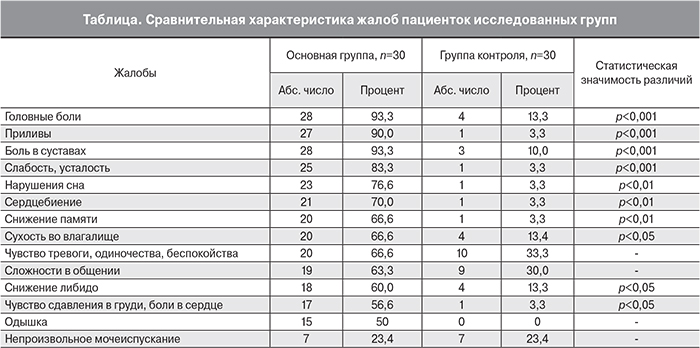
У пациенток основной группы отягощенный акушерский анамнез имел место у 25 пациенток (83,3±2,8%), а в группе контроля у 24 (80,0±2,7%) (р>0,05). Из гинекологических заболеваний миома матки отмечена у 30,0±1,0% (n=9) пациенток основной группы и у 26,6±0,9% (р>0,05) – группы контроля; эндометриоз составил 10±0,3% (n=3) и 6,6±0,2% (n=2) (р>0,05) соответственно. Заболевания шейки матки встречались в 26,6±0,9% (n=8) и 23,3±0,8% (n=7) (р>0,05) у женщин основной и контрольной групп; фиброзно-кистозная мастопатия – у 26,6±0,9% (n=8) в основной группе и 30,0±1,0% (n=9) в группе контроля (р>0,05). Анкетирование пациенток показало, что основными жалобами женщин исследованных групп были НВС, которые статистически чаще встречались в основной группе (таблица)
В ходе исследования мы получили следующую динамику шкалы ММИ. По НВС сумма баллов ММИ в исследуемой группе составила 22,9, а у женщин группы контроля – 6 баллов (р<0,05). После терапии менорилом в дозе 1 капсула 2 раза в день в течение 90 дней мы отметили снижение ММИ в основной группе по НВС до 13,7 балла, при этом получены статистически значимые различия (р<0,05). По группе ЭМС в основной группе они составили 6 баллов против 3,1 в группе сравнения: после применения генистеина в активной форме (менорила) в основной группе сумма баллов ММИ по ЭМС составила 4,46. Что касается ПЭС, в основной группе они составили 4,96 балла против 1,8 балла в группе контроля, а после лечения препаратом менорил уменьшились в основной группе почти в 2 раза – до 4,96 (рис. 1).
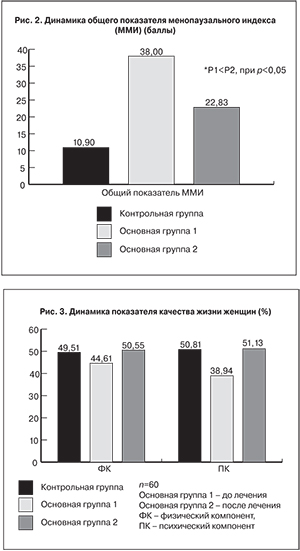
Динамика общего показателя ММИ следующая: суммарный показатель ММИ в основной группе составил 38 баллов, что соответствует КС средней степени тяжести; в группе контроля сумма баллов ММИ составила 10,9. После лечения женщин основной группы генистеином (менорилом) в дозе 30 мг 2 раза в день на протяжении 90 дней суммарный ММИ в этой группе составил 22,83, при этом получены статистически значимые различия (р<0,05) (рис. 2).
Изучение качества жизни женщин показало, что по ФК в исследуемой группе из возможных 100% был получен показатель 44,64%. При этом в группе контроля он также был невысок и составил 49,51%. После лечения генистеином (менорилом) по принятой схеме произошло увеличение показателя качества жизни по ФК в основной группе – до 50,55%, что фактически превысило показатели группы контроля. По ПК эффект от лечения менорилом был еще более выражен. Показатель качества жизни по ПК в основной группе – 38,94%, в контрольной – 50,81%. После терапии менорилом ФК в исследуемой группе повысился до 51,13%, что несколько превысило показатель контрольной группы (рис. 3).
При оценке удовлетворенности женщин результатами терапии было выявлено, что в целом позитивное впечатление от приема препарата осталось у 26 пациенток (86,6±2,9%), у прочих женщин – без перемен. При этом высокая удовлетворенность результатами терапии была у 12 женщин (40,0±1,3%).
Изменений ИМТ на фоне лечения выявлено не было. Обострений хронических соматических заболеваний не отмечалось. Побочных эффектов на прием препарата в ходе нашего исследования мы не отметили ни у одной женщины.
Выводы
- У женщин с КС легкой и средней степени тяжести качество жизни снижено, как по ПК (на 23.3%), так и по ФК (на 9.8%), в сравнении с контрольной группой. Таким образом, основанием для назначения менорила является снижение качества жизни женщин в возрастной категории 45+.
- Эффективность менорила в лечении КС легкой и средней степени тяжести высокая, составила 86.6%, при этом не было отмечено побочных эффектов при приеме препарата.
- На фоне приема генистеина, синтезированного в активной форме (менорила), в суточной дозе 60 мг в течение 3 месяцев, уменьшается выраженность климактерических расстройств на 40% (по ММИ), преимущественно за счет группы НВС.
- Качество жизни женщин с КС средней и легкой степени тяжести на фоне приема менорила по описанной схеме улучшается на 23,8% по ПК и на 11,75% по ФК.
- Менорил можно рассматривать как альтернативу МГТ при противопоказаниях к ней или при отказе женщины от МГТ.
Заключение
Как будет дальше развиваться альтернативная медицина, как будут развиваться ее взаимоотношения с медициной классической, пока не ясно. МГТ, безусловно являясь «золотым стандартом» лечения климактерических расстройств, тем не менее, не может быть назначена абсолютно всем нуждающимся в ней женщинам – в связи с противопоказаниями либо отказом больной от гормонотерапии. В нашем исследовании было показано, что применение генистеина, синтезированного в активной форме (менорил), в суточной дозе 60 мг на протяжении 3 месяцев, способно улучшить качество жизни, снизить частоту и выраженность климактерических симптомов средней и легкой степени тяжести и может рекомендоваться в качестве альтернативной терапии КС.



