Современная концепция перинатальной охраны плода предусматривает не только обеспечение ребенку «здорового старта жизни», снижение перинатальной заболеваемости и смертности, но также и снижение заболеваемости населения, улучшения демографической ситуации в нашей стране [1–3]. В настоящее время общепринятым является положение о существенном влиянии антенатального развития и особенностей нарушения состояния плода во время беременности на повышение заболеваемости детей и взрослых, в том числе и социально значимыми заболеваниями [1, 4, 5]. Резервные возможности плода и его эндокринной системы при патологическом течении беременности определяются генетическими факторами и особенностями течения гестационного процесса [4–6]. Особенности воздействия на рост и развитие плода неблагоприятных факторов, в том числе состояния здоровья беременной и осложнений гестации и реакция на их воздействие со стороны плода, вплоть до тяжелых структурно-функциональных изменений определяется как метаболическое пренатальное программирование [7–9]. В структуре летальности населения Российской Федерации более 57% приходится на социально-значимую патологию, в том числе сердечно-сосудистые заболевания, декомпенсированный сахарный диабет и др. [1]. С этой точки зрения формирование неблагоприятного перморбидного эндокринно-метаболического фона при беременности высокого риска, частота которой достигает 70% и более, приобретает все большую актуальность [5, 8, 10]. Среди всех возможных причин ожирения, метаболического синдрома, сахарного диабета, сердечно-сосудистых заболеваний стала очевидна роль нарушенного антенатального метаболического программирования, особенно при беременности, осложненной плацентарной недостаточностью (ПН) и синдромом задержки роста плода (СЗРП) [6, 11, 12].
Антенатальный период характеризуется как возможностью возникновения структурно-функциональных нарушений состояния плода, так и наличием ряда адаптивных и резервных возможностей развивающегося ребенка и всей системы мать-плацента-плод, которые при развитии ПН и СЗРП, гипоксии плода способствуют формированию так называемого «экономного фенотипа» [8, 9, 12–15]. При постнатальном развитии происходит «растормаживание» и разбалансировка эндокринной регуляции метаболизма, что в последующем способствует накоплению жировой ткани, нарушениям липидного обмена и формированию метаболического синдрома [7, 16–20].
В связи с этим поиск антенатальных прогностических факторов дисфункции эндокринной системы плода позволит оценить функциональное состояние новорожденного, определить прогноз течения неонатального периода и перинатальные исходы при ПН различной степени тяжести, что позволит снизить перинатальную и детскую заболеваемость и смертность [21, 22].
Целью исследования было определение эндокринного статуса плода с использованием эхографической морфометрии щитовидной железы плода, надпочечников, поджелудочной железы, допплерометрии кровотока в данных органах, определения уровня гормонов и метаболитов в пуповинной крови при неосложненной беременности и ПН с формированием СЗРП различной степени тяжести.
Материал и методы исследования
Основную группу составили 320 женщин с одноплодной беременностью, осложнившейся ПН и СЗРП различной степени тяжести. Среди женщин с CЗРП для оценки влияния степени антенатального страдания плода на становление эндокринного и метаболического статуса нами было выделено 3 подгруппы. Компенсированная ПН и СЗРП I степени были выявлены у 165 (51,6%), субкомпенсированная ПН и СЗРП II степени – у 108 (33,8%), декомпенсированная ПН и СЗРП III степени – у 47 (14,7%) беременных. Такой подход согласуется с точкой зрения ведущих специалистов перинатальной медицины [4, 20, 21]. Контрольную группу составили 135 беременных, не имеющих значимой экстрагенитальной патологии и отягощающих факторов акушерско-гинекологического анамнеза, с одноплодной неосложненной беременностью, закончившейся рождением здоровых доношенных нормотрофичных детей. Клинико-лабораторное и инструментальное обследование беременных основной группы с CЗРП различной степени тяжести проводилось амбулаторно (женские консультации г. Москвы) и в стационаре (родильный дом при ГБУЗ ГКБ № 7 ДЗ г. Москвы, с декабря 2015 г. – ГБУЗ ГКБ им. С.С. Юдина ДЗ г. Москвы) в сроки с 18-й по 41-ю неделю гестации. Лабораторное исследование проводилось на базе Лаборатории центра иммунологии и репродукции (Москва).
С целью оценки морфофункционального состояния щитовидной и поджелудочной желез, а также надпочечников плода при неосложненной беременности и при СЗРП всем беременным контрольной и основной групп проводились ультразвуковая динамическая морфометрия указанных органов эндокринной системы плода, допплерометрия кровотока в артериях, их кровоснабжающих (щитовидные артерии, средняя надпочечниковая артерия, верхняя брыжеечная и селезеночная). После рождения ребенка нами проводилось определение уровней гормонов, отражающих ее функциональное состояние (тиреотропный гормон (ТТГ), тироксин (Т4), трийодтиронин (Т3), кортизол, инсулин, соматотропный гормон, С-пептид, аутоантитела к инсулину, лептин, гликозилированный гемоглобин) в пуповинной крови. Беременным также проводилось комплексное динамическое ультразвуковое фетометрическое, плацентографическое и допплерометрическое исследование кровотока в маточных артериях, артерии пуповины, средней мозговой артерии плода и аорте плода.
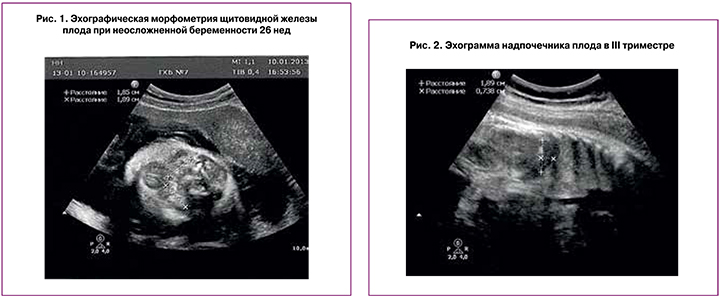
Обследование беременных основной группы проводилось на кафедре акушерства, гинекологии и перинатологии Первого МГМУ им. И.М. Сеченова в лаборатории пренатальной диагностики, в приемном отделении и клинико-диагностическом центре родильного дома ГКБ № 7 (в настоящее время – ГБУЗ ГКБ им. С.С. Юдина ДЗ г. Москвы) с использованием аппаратов ESAOTE MyLab 70 (Италия) и Philips HD15 (Голландия), снабженных датчиком цветного и допплеровского картирования и конвексным электронным датчиком с частотой 2–7 МГц и глубиной сканирования 48–314 мм. С целью проведения ультразвуковой морфометрии поджелудочной железы плода первоначально получали несколько косое поперечное сечение живота плода на уровне визуализации желудка и верхнего полюса левой почки. В дальнейшем придерживались методики, описанной K. Hata и соавт. (1988) и E. Merz (2005) [22–24]. Для проведения оценки размеров щитовидной железы плода добивались визуализации шеи плода в поперечном сечении, основываясь на методике R. Achiron и соавт. (1998) (рис. 1) [25]. Кровоток в щитовидных артериях плода регистрировали в области сосудистых пучков, расположенных по обе стороны железы [16]. Также при допплерометрии проводилось измерение угол независимых параметров кровотока в артериях надпочечников, щитовидной артерии, верхней брыжеечной и селезеночной артериях плода [14, 26].
Оценка состояния новорожденных проводилась на 1-й и 5-й минуте жизни по шкале Апгар; определяли также массу тела при рождении, рост, окружность груди, окружность головы; оценивали соответствие данных параметров гестационному сроку. Анализировали длительность пребывания в родильном доме. После рождения детей, пересечения пуповины, производился забор 10 мл пуповинной крови для оценки гормонального и биохимического статуса новорожденных.
В качестве программного обеспечения статистического анализа полученных данных использовался пакет модулей для статистической обработки данных программы Statistica 64 bit for Windows, а также статистических функций программы Microsoft Office Excel 2007. Вычисления производили с помощью программы на сайтах www.medstatistic.ru и www.medcalc.org. Определяли частоту встречаемости изучаемых факторов в изучаемых группах с использованием метода расчета относительного риска и его 95% доверительного интервала. Различия в частотах считали статистически значимыми при уровне значимости р<0,05, p<0,01 (95% уровень значимости).
Результаты исследования и обсуждение
Средний возраст беременных контрольной группы составил 25,52±3,57 года с индивидуальными колебаниями от 18 до 36 лет. Данная беременность у 100% женщин контрольной группы протекала без осложнений и закончилась своевременными родами у 130 (96,3%) и запоздалыми – у 5 (3,7%). Средний срок беременности к моменту родоразрешения составил 39,4±0,76 недели. Всего в контрольной группе родилось 135 детей. Средняя масса при рождении составила 3540±288 г, с индивидуальными колебаниями от 3055 до 4420 г; средний рост новорожденных – 51,8±2,8 см, с колебаниями от 49 до 57 см.
Средний возраст женщин основной группы составил 33,7±3,4 года, с индивидуальными колебаниями от 24 до 45 лет, и был достоверно выше среднего возраста женщин контрольной группы (p<0,05). Следует отметить высокую частоту гинекологических заболеваний у беременных основной группы: патология шейки матки (вплоть до тяжелой дисплазии с конизацией шейки матки) – у 64 (20,0%); миома матки – у 18 (5,6%) (у 11 – была произведена консервативная миомэктомия до наступления беременности); эндометриоз различной локализации – у 6 (2,22%); воспалительные заболевания органов малого таза – у 114 (35,6%); инфекции, передающиеся половым путем – у 57 (17,8%); опухолевидные образования яичников – у 6 (2,22%); бесплодие первичное или вторичное – у 64 (20,0%), причем у 18 (5,6%) было от 1 до 3 неудачных попыток ЭКО до наступления данной беременности; у 28 (8,8%) женщин данная беременность наступила в результате ЭКО. Общая гинекологическая заболеваемость у женщин основной группы составила 65,6% (n=210), что достоверно выше, чем в контрольной группе (RR=1,65, CI=1,527–4,486). Сочетанная гинекологическая патология отмечалась у каждой третьей (n=110) беременной основной группы (34,4%) (RR=1,34, CI=0,973–1,655).
Первобеременных и первородящих женщин основной группы было 89 (27,8%), повторнобеременных первородящих – 135 (42,2%); повторнобеременных повторнородящих – 96 (30,0%). 28 (12,12%) женщин из повторнобеременных имели в анамнезе от 2 до 4 артифициальных абортов до 12 недель гестации; 36 (15,6%) – самопроизвольные выкидыши и/или неразвивающиеся беременности до 21+6 нед; 21 (9,09%) – преждевременные роды. Рубец на матке после операции кесарева сечения отмечался у 44 (19,1%) беременных, после 2 операций – у 5 (2,16%). Во время данной беременности признаков несостоятельности рубца на матке или врастания плаценты в область рубца не было.
У 213 (66,6%, RR=2,73, CI=1,5988–4,6523) женщин основной группы выявлены соматические заболевания, при этом в 23,44% диагностирована сочетанная патология (RR=3,50, CI=1,1020–11,1158). У беременных основной группы с СЗРП различной степени тяжести обращала на себя внимание относительно высокая частота гипертензивных нарушений – 27,8% (n=89) против 6,7% (n=9) в контрольной группе (RR=4,1667, CI=1,3288–13,0656); заболеваний мочевыводящей системы – 15,62% (n=50) против 4,44% (n=6) в контрольной группе (RR=3,50, CI=0,8311–14,7393). Кроме того, у них чаще были хронические заболевания органов дыхания – 10,0% (n=32) против 2,22% (n=3) в контрольной группе (RR=4,5, CI=0,5882–34,4281); генетические формы тромбофилий – 6,56% (n=21) против 2,22% (n=3) (RR=3,05, CI=0,3723–24,1719). Столь высокая частота соматической и гинекологической патологии у беременных с ПН и СЗРП подтверждают значимость данных патологических состояний в формировании осложнений гестации и нарушений состояния плода [3, 4, 21].
В основной группе своевременными родами закончилась беременность у 256 (80,0%) женщин. 61 (19,06%) беременная были родоразрешены досрочно, у 4 (1,25%) произошли самопроизвольные преждевременные роды на сроках 32–35 недель. Показаниями для досрочного родоразрешения были: декомпенсированная ПН и критическое состояние плода в сочетании с CЗРП III степени – 32 (10,0%); тяжелая преэклампсия с отсутствием эффекта от проводимой терапии – 21 (6,56%); развитие регулярной родовой деятельности при наличии рубца на матке, СЗРП II степени – 4 (1,25%), субкомпенсированная ПН и СЗРП II степени при прогрессировании хронической гипоксии и развитии аритмии у плода – 2 (1,25%).
Путем операции кесарева сечения родоразрешены 132 (41,25%), из них 61 (46,21%) – в срочном порядке. Родилось 320 детей. Средняя масса при рождении составила 2680±320 г с индивидуальными колебаниями от 1640 до 3480 г, средний рост – 46±3,2 см, с индивидуальными колебаниями от 41 до 53 см. Средняя оценка новорожденных по шкале Апгар на 1-й минуте составила 7,2±0,8 балла, на 5 минуте – 8,1±0,6 балла. Оценка по шкале Апгар у новорожденных на 1-й минуте 5 баллов и менее, свидетельствующая о тяжелой гипоксии, выявлена у 21 (6,56%) ребенка.
При неосложненном течении беременности отмечается линейное увеличение размеров щитовидной железы плода: окружности с 21,35±2,9 мм до 61,32±5,37 мм, ширины – с 8,89±1,5 до 26,11±3,48 мм. При ПН и СЗРП различной степени тяжести происходит уменьшение всех размеров щитовидной железы плода по сравнению с нормативными для данного срока беременности. Снижение темпов роста щитовидной железы при СЗРП различной степени происходит неравномерно на протяжении беременности.
Так, при CЗРП I степени снижение темпов прироста морфометрических параметров щитовидной железы происходит в III триместре беременности (в 34–36 недель). Так, окружность щитовидной железы менее нормативных параметров в 34–36 недель на 10,8%, ширина – на 15%. При субкомпенсированной ПН и СЗРП II отмечается равномерное отставание размеров железы на протяжении II и III триместров беременности с 16 недель. В 16–18 недель окружность щитовидной железы на 17,9% меньше нормативных параметров, в 22–24 недели – на 16% меньше, в 28–30 недель – на 9% и в 34–36 недель – на 20,9%.
При декомпенсированной ПН и СЗРП III степени также отмечается выраженное отставание размеров щитовидной железы от должных, начиная с 16 недель. Причем максимально данная тенденция выражена в сроки 28–30 недель, в отличие от менее тяжелых форм. Окружность щитовидной железы при этом менее нормативных значений на 28,6%, в сроки 34–36 недель – на 25,3%. Изучение эхоструктуры щитовидной железы плода при неосложненной беременности и СЗРП различной степени тяжести продемонстрировало отсутствие существенных отличий (нами не выявлено ни в одном наблюдении в основной и контрольной группах объемных образований и кист в толще железы). Однако при декомпенсированной ПН и критическом состоянии плода в 10 (21,3%) из 47 наблюдений отмечено повышение эхогенности ткани щитовидной железы плода.
При исследовании кровотока в щитовидных артериях плода при неосложненной беременности выявлено, что спектр кровотока имеет форму двухфазной кривой. По мере прогрессирования беременности происходит снижение систоло-диастолического отношения (СДО) в щитовидных артериях плода от 4,78±0,27 в 16–18 недель до 3,67±0,19 в 36 недель. При этом максимальное снижение сосудистой резистентности отмечается в раннем фетальном периоде – сроки с 18 по 24 неделю гестации (на 29,9%), что происходит параллельно с завершением второй волны инвазии трофобласта и максимальным снижением сосудистой резистентности в маточно-плацентарном звене кровообращения единой системы мать-плацента-плод. Затем, до конца беременности показатели сосудистого сопротивления остаются стабильными.
При беременности, осложненной развитием СЗРП, отмечается повышение всех показателей сосудистой резистентности в щитовидных артериях по сравнению с нормативными значениями (табл. 1).
При CЗРП I степени в 22 недели показатели СДО превышают нормативные на 23,3%. Затем показатели сосудистого сопротивления снижаются и в сроке 34–36 недель не отличаются от нормы. При СЗРП II степени в сроке 22–24 недели (ранний фетальный период) показатели СДО достоверно выше нормы с последующим снижением к 34–36 неделе на 22,8%, пульсационный индекс (ПИ) – на 18,9%. При декомпенсированной ПН и СЗРП III степени показатели сосудистого сопротивления ниже нормативных в течение всей беременности, начиная с 16 недель. В сроке 34–36 недель СДО ниже, чем в контрольной группе в 1,3 раза, ПИ – в 1,15 раза.
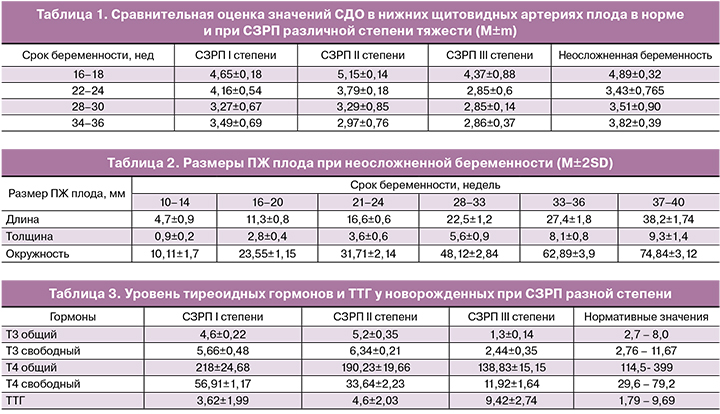
При ультразвуковом исследовании также осуществлялось определение размеров плодовых надпочечников – ширины, высоты и толщины – в сроки 16–20, 21–24, 25–28, 29–32, 33–36 и 37–40 недель гестации (рис. 2). По мере прогрессирования неосложненной беременности происходит линейный рост надпочечников плода от 6,32±0,74 мм по ширине, 3,78±0,8 мм по высоте и 2,73±0,34 мм по толщине с 16 недель и до 23,11±0,86 мм по ширине, 14,1±0,88 мм по высоте и 4,13±0,22 мм по толщине в доношенном сроке, что отражает нормальное морфофункциональное развитие органа. При CЗРП различной степени тяжести характер изменения размеров надпочечников плода зависел от степени СЗРП. При компенсированной ПН и CЗРП I степени отмечалось опережение скорости роста желез по сравнению с контрольной группой на 17,9–21,3% по ширине, 3,9–24,8% по высоте и 16,7–27,6% по толщине; при субкомпенсированной ПН и СЗРП II степени – на 23,8–25,3% по ширине, 9,7–35,2% по высоте и 24–33,4% по толщине.
При появлении признаков СЗРП II степени скорость роста желез становилась гораздо более интенсивной, опережая показатели, характерные для контрольной группы и компенсированной ПН. Далее при достижении положительного эффекта от лечения, когда происходила стабилизация или улучшение маточно-плацентарно-плодового кровотока и прирост параметров фетометрии, темпы роста надпочечников несколько снижались, однако продолжали достоверно (р≤0,05) превышать таковые при неосложненной беременности и компенсированной ПН. При декомпенсированной ПН и CЗРП III степени нами были выявлены несколько иные закономерности роста надпочечников плода. К концу второго триместра при обнаружении достаточно выраженных гемодинамических нарушений в системе мать-плацента-плод и СЗРП размеры надпочечников недостоверно превышали показатели (р≤0,05), характерные для неосложненной беременности (на 10,3% по ширине, 4% по высоте и 4,7% по толщине), но были гораздо меньше параметров, зарегистрированных при компенсированной и субкомпенсированной ПН с положительным эффектом от лечения. Далее, наряду с усугублением внутриутробной гипоксии, скорость роста надпочечников замедлялась вопреки тенденциям, выявленным в предыдущих наблюдениях. К исходу беременности показатели их морфометрии приобретали достоверно (р≤0,05) более низкие численные значения, чем в контрольной группе: ширина становилась меньше на 21,1%, высота – на 18%, толщина – на 8,2%. Чем дольше существовала и тяжелее протекала ПН, тем меньшие размеры желез определялись при эхографическом исследовании.
При исследовании кровотока в артериях надпочечников в условиях неосложненной беременности была выявлена двухфазная кривая, состоявшая сначала из некоторого повышения сосудистого сопротивления с 16 до 29–32 недель, а затем его постепенного снижения к доношенному сроку. Показатели СДО, индекс резистентности (ИР) и ПИ, составлявшие в 16 недель соответственно 2,71±0,45, 0,63±0,06 и 1,13±0,22, несколько повышались к концу второго – началу третьего триместра (29–32 недели). Однако указанные изменения не были значительными: СДО увеличивалось на 8,8% (2,95±0,48), ИР – на 6,3% (0,67±0,07), а ПИ – на 5,3% (1,19±0,24). Некоторое повышение сосудистого сопротивления вызвано, по-видимому, более интенсивным ростом надпочечников (когда происходило почти двукратное увеличение ширины и высоты), что обусловлено повышенной функциональной активностью желез при «критических» периодах развития плода (в 24–27 и 30–32 недели). Затем угол-независимые коэффициенты начинали постепенно уменьшаться, приобретая к доношенному сроку более низкие численные значения, чем в начале исследования (СДО становилось меньше на 1,5% (2,67±0,29), ИР – на 1,6% (0,62±0,04), а ПИ – на 1,8% (1,11±0,2)). Снижение сосудистого сопротивления, очевидно, происходило благодаря становлению процессов ангиогенеза, заключавшихся в интенсивном разрастании и ветвлении надпочечниковых артериол, а также развитии капиллярной сети.
При CЗРП I степени отмечался более выраженный рост сосудистого сопротивления, и СДО было на 14,7%, ИР – на 7,9% и ПИ – на 5,2% выше, чем в контрольной группе, а при субкомпенсированной ПН данное несоответствие для СДО составляло 14,1%, ИР – 9,0% и ПИ – 6,1%. При декомпенсированной ПН и CЗРП III степени СДО было на 7,2%, ИР – на 14,5% и ПИ – на 26,9% выше, чем при неосложненной беременности.
Определение размеров поджелудочной железы (ПЖ) плода при УЗИ при неосложненной беременности показало, что по мере ее прогрессирования происходит линейное увеличение размеров железы (табл. 2).
При компенсированной ПН и СЗРП I степени выявлено уменьшение размеров ПЖ плода по сравнению с неосложненной беременностью только в III триместре (в сроки 33–36 недель). Так, длина железы в сроки 33–36 недель была на 11,3% менее нормативных параметров, толщина – на 6,7%, окружность – на 9,2%. Однако достоверной разницы в размерах ПЖ плода при СЗРП I степени по сравнению с таковыми при неосложненной беременности нами выявлено не было.
При CЗРП II степени нами выявлено равномерное отставание размеров ПЖ плода по сравнению с контрольной группой на протяжении II–III триместров, начиная с 21-й недели беременности. Так, длина ПЖ плода в сроки 21–24 недели в данной клинической ситуации уменьшена на 33,1%, окружность – на 26,2%; в сроки 28–33 недели – на 28% и 21,23% соответственно по сравнению с таковыми при неосложненной беременности. В сроки 33–36 недель длина ПЖ плода при субкомпенсированной ПН и СЗРП II степени уменьшена на 22,8%, окружность железы – на 18,4% соответственно. В сроки 37–40 недель длина железы уменьшена на 21,2%, окружность – на 17,42%. Таким образом, нами отмечалось равномерное уменьшение размеров ПЖ плода при формировании CЗРП II степени. При декомпенсированной ПН и СЗРП III степени отмечалось наиболее выраженное отставание размеров ПЖ плода со сроков 21–22 недели гестации.
При беременности, осложненной ПН и СЗРП, динамика показателей сосудистой резистентности в верхней брыжеечной и селезеночной артериях отлична от таковой при неосложненной беременности. Суммарно повышение сосудистого сопротивления в верхней брыжеечной артерии при СЗРП I степени составило 48,25%. Нарушения органного кровотока характеризуются постепенным повышением индексов сосудистого сопротивления, происходящим сонаправленно с ухудшением маточно-плацентарно-плодового кровообращения, формирования и нарастания СЗРП.
В селезеночной артерии сосудистое сопротивление в данной клинической ситуации было достоверно выше на протяжении всего III триместра (с момента выявления СЗРП I степени) и составило 74,61%. При субкомпенсированной ПН и СЗРП II степени уже со срока 21–24 недели гестации отмечается достоверное повышение сосудистого сопротивления. Суммарное повышение сосудистого сопротивления в верхней брыжеечной артерии при СЗРП II степени составляет 122,27% (то есть в 1,2 раза); в селезеночной артерии – 143,28% (то есть в 1,43 раза), что значимо для существенного ухудшения перфузии развивающегося органа. Наиболее выраженные нарушения органного кровотока в ПЖ нами были отмечены при декомпенсированной ПН и СЗРП III степени. Причем из 47 плодов с СЗРП III степени у 19 было зарегистрировано критическое состояние плодово-плацентарного кровотока (отсутствие диастолического компонента кровотока в артерии пуповины) – 40,43%. В остальных наблюдениях, где диастолический компонент кровотока был сохранен, отмечалось максимальное повышение сосудистого сопротивления в изучаемых сосудах. Суммарно в верхней брыжеечной артерии сосудистое сопротивление в сроки 21–34+6 недель беременности возросло на 127,9%, в селезеночной артерии – на 146%.
Изменения уровней гормонов щитовидной железы и ТТГ при ПН разной степени тяжести представлены в табл. 3. В работе использовались нормативные значения уровней тиреоидных гормонов и ТТГ у новорожденных первых суток жизни, разработанные M.W. Elmlinger и соавт. (2001) [27].
При компенсированной ПН отмечаются наиболее близкие к нормативным концентрации общего и свободного Т4, а также уровень ТТГ, не выходящий за пределы нормативных значений. При субкомпенсированной ПН и СЗРП II–III степени отмечается снижение концентрации общих и свободных фракций тиреоидных гормонов в сыворотке пуповинной крови и повышение концентрации ТТГ, что отражает наличие гипотиреоза у плода и сохранность механизма отрицательной обратной связи в регуляции функции щитовидной железы плода.
Нормальные или повышенные показатели уровня кортизола, отмеченные в контрольной группе (148,2–176,5 нмоль/л), а также при развитии компенсированной ПН (154,7–189,4 нмоль/л) и субкомпенсированной ПН с положительным эффектом от лечения (411,25–485,62 нмоль/л), соответствовали адекватному приспособлению плода к условиям внутриутробной гипоксии, что сопровождалось благоприятными перинатальными исходами. Низкая концентрация кортизола при прогрессирующей субкомпенсированной ПН (121,16–123,3 нмоль/л) и декомпенсированной ПН (105,8 нмоль/л) свидетельствовала о нарушениях адаптации с последующим возникновением тяжелых осложнений в раннем неонатальном и постнатальном периодах. Клиническое значение оценки морфофункционального состояния надпочечников плода при патологическом течении беременности позволило прогнозировать тяжесть развития ПН, ее осложнения и исходы [15]. Это помогло определить рациональную тактику ведения таких пациенток, выявить оптимальные сроки и методы родоразрешения, что привело к снижению перинатальной заболеваемости.
C целью изучения функционального состояния ПЖ плода и новорожденного при неосложненной беременности и СЗРП различной степени тяжести мы определяли уровни глюкозы, инсулина, соматотропного гормона, С-пептида, аутоантител к инсулину, лептина, гликозилированного гемоглобина и панкреатической амилазы в сыворотке пуповинной крови, полученной сразу после пересечения пуповины.
Следует отметить, что аутоантитела к инсулину в пуповинной крови ни в одном наблюдении в основной и контрольной группах нами не выявлены. Таким образом, в нашем исследовании не было отмечено связи генетической предрасположенности к инсулинзависимому сахарному диабету 1-го типа (аутоиммунного типа) с антенатальными нарушениями трофики ПЖ плода при СЗРП. Cуществует прямая корреляция между выявляемыми нарушениями гормональной регуляции углеводного обмена, уровнем глюкозы в крови новорожденного, нарушением и экзо- и эндокринной функции ПЖ плода и степенью тяжести ПН и СЗРП. Так, нами выявлено достоверное снижением уровня глюкозы в пуповинной крови, инсулина, С-пептида (отражающего уровень инсулина в течение более длительного времени), инсулинзависимого фактора роста-1 (соматомедина С), лептина (отражающего функции жирового обмена, участвующего в регуляции энергетического обмена и массы тела), гликированного гемоглобина (уровень которого зависит от среднего уровня глюкозы в крови на протяжении срока жизни эритроцитов плода) и амилазы. Причем снижение данных гормонов, ферментов и биохимических показателей особенно значимо при декомпенсированной ПН и СЗРП III степени. Однако уже при субкомпенсированной ПН и СЗРП II степени отмечено достоверное снижение уровня соматомедина С, С-пептида, лептина и особенно амилазы.
Интересен тот факт, что в целом при ПН и СЗРП уровень инсулина был понижен у 216 из 320 (67,5%) новорожденных при анализе пуповинной крови, у остальных 104 (32,5%) отмечались нормальные показатели инсулина. Нормальные показатели были отмечены только у новорожденных с СЗРП I степени. Ни в одном наблюдении нами не было выявлено высоких значений инсулина, несмотря на гипогликемию у новорожденных при декомпенсированной ПН.
При декомпенсированной ПН отмечалось снижение уровня глюкозы в пуповинной крови в среднем в 2,3 раза с развитием гипогликемии, инсулина – в 3,62 раза (уровень инсулина ниже нижней границы нормативных значений, что свидетельствует о существенном нарушении функции ПЖ плода, причем наиболее выражено снижение было при отсутствии диастолического компонента кровотока в сосудах, кровоснабжающих ПЖ плода). Уровень С-пептида при СЗРП III степени был снижен в 4 раза. Особенно значимым оказалось снижение уровня инсулинзависимого фактора роста-1 (соматомедина С), что четко указывает на патогенетическую связь нарушений роста плода с прогрессирующими изменениями его метаболизма – в 5,2 раза. Обращает на себя внимание и снижение экзокринной функции ПЖ плода при тяжелой задержке роста, что отражается уменьшением уровня амилазы в 4,6 раза. Следует отметить, что срок родоразрешения при декомпенсированной ПН был не позднее 35-й недели гестации и, возможно, столь низкие показатели, полученные нами, обусловлены недоношенностью новорожденного, что еще больше усугубляет нарушения его углеводного и жирового обмена, и далее – более высокую детскую заболеваемость [4, 7, 27].
Заключение
Таким образом, проведенные нами исследования показывают, что при ПН происходят существенные отклонения от нормы в анатомо-функциональном становлении и развитии эндокринной системы плода, существенно нарушающие регуляцию метаболизма у новорожденного, а в последующем у ребенка, нарушающими его рост и развитие. Изучение особенностей морфофункционального состояния щитовидной, поджелудочной желез плода, его надпочечников, включающее ультразвуковую морфометрию, допплерометрическое исследование кровотока в кровоснабжающих их сосудах (щитовидные артерии, артерии надпочечников, верхняя брыжеечная и селезеночная артерия), а также исследование гормонального статуса и параметров метаболизма в пуповинной крови новорожденного дает дополнительные критерии оценки тяжести ПН и нарушений состояния плода, которые позволяют уточнить и индивидуализировать акушерскую тактику. Кроме того, указанные данные помогут разработать протоколы ведения ребенка с учетом высокого риска развития социально значимых обменно-метаболических и эндокринных нарушений (нарушение роста и малорослость, метаболический синдром и сахарный диабет, нарушение функции желудочно-кишечного тракта, хронические панкреатиты, гастродуодениты и др.).



