Сегодня дисменорея является, пожалуй, самым распространенным заболеванием в сфере женского здоровья, преимущественно у молодых женщин [1–3]. Среди подростков при этом дисменорея встречается в 43–90%, при этом частота встречаемости увеличивается с гинекологическим возрастом и достигает пика к 5-му году менархе [1]. Дисменорея определенно оказывает существенное влияние на качество жизни. Данное заболевание является одной из основных причин отсутствия женщин фертильного возраста на работе или учебе по медицинским основаниям: 10–15% нетрудоспособны в течение 1–3 дней ежемесячно [2, 4].
Как известно, дисменорея представляет собой циклический патологический процесс, который проявляется широким спектром нейровегетативных, эндокринных, психоэмоциональных отклонений с болевым синдромом в качестве ведущего проявления – выраженными болями внизу живота в дни менструации. Абдоминальная боль может сопровождаться общей слабостью, тошнотой, рвотой, головной болью, головокружением, отсутствием аппетита, сухостью во рту, слюнотечением, метеоризмом, диареей, ощущением «ватных» ног, усилением потоотделения, обмороками и другими эмоциональными и вегетативными расстройствами [2, 5, 6].
Выделяют первичную и вторичную дисменорею. При первичной дисменорее отсутствует патология половых органов, она широко распространена (встречается более чем у 50% женщин) и характеризуется тяжелым течением приблизительно у 5–15% женщин. В противоположность этому при вторичной дисменорее боли являются следствием каких-либо заболеваний органов малого таза. К развитию вторичной дисменореи может привести целый ряд заболеваний и состояний: эндометриоз, пороки развития матки и влагалища, воспалительные заболевания органов малого таза, миома матки, инородное тело в полости матки (внутриматочная спираль) и др., соответственно, клиническая картина, прогноз, а также подходы к терапии при вторичной дисменорее определяются особенностями первичного заболевания [1, 2, 6].
Патогенез дисменореи связан с нарушением циклической секреции гонадотропных гормонов и высоким уровнем простагландинов в менструальном эндометрии, которые являются стимуляторами сократительной активности гладкой мускулатуры матки, приводя к спазму сосудов, локальной ишемии, раздражению нервных окончаний и возникновению боли, обусловленной спазмом [2, 7].
Боль при дисменорее относится к висцеральным болям, то есть вызванным патологическими импульсами, воздействующими на внутренние органы. Висцеральная боль обычно тупого характера (схваткообразная, тянущая, жгущая), возникает в стороне от средней линии живота. Точная локализация висцеральных болей достаточно сложна, поскольку иннервация большинства внутренних органов мультисегментарна: сравнительно недавнее открытие перекреста между различными висцеральными афферентными нервами может объяснить явное диффузное усиление болевых ощущений у пациентов с заболеваниями, проявляющимися висцеральными болями [8]. Лечение висцеральных болей включает два параллельных процесса: лечение подлежащей патологии, если она определена, и снятие симптомов. Лечение висцеральных болей должно полагаться на фармакотерапию не только классическими обезболивающими средствами, к каким относятся нестероидные противовоспалительные средства (НПВС), но и препаратами, которые сами по себе не являются обезболивающими, но снижают боль в особых обстоятельствах путем воздействия на причину возникновения боли. В число последних входят антагонисты гистаминовых рецепторов в желудочно-кишечном тракте или ингибиторы протонных насосов, которые облегчают боль при язве или гастрите, снижая кислотность желудка, и спазмолитические препараты, которые снимают боль, возникающую в результате обструкции полых органов, путем прерывания рефлекторного сокращения внутренних органов [8].
Дротаверина гидрохлорид является сильным спазмолитическим агентом, действующим на гладкую мускулатуру [9]. Дротаверин представляет собой производное изохинолина, родственное папаверину. Однако по сравнению с папаверином дротаверин обладает более мощным действием и более надежной эффективностью после перорального приема. Дротаверин не вызывает антихолинергических эффектов. Тем не менее, его можно выгодно комбинировать с антихолинергическими и ненаркотическими обезболивающими средствами. Спазмолитическое действие дротаверина обусловлено специфическим ингибированием фермента фосфодиэстеразы 4-го типа (ФДЭ4), которое приводит к накоплению внутри клетки циклического аденозинмонофосфата (цАМФ) и, в конце концов, к ингибированию кальций-опосредованных сокращений гладкой мускулатуры. Он хорошо и практически полностью всасывается после приема внутрь и быстро распределяется в организме [1, 9].
Однако в настоящее время как в России, так и за рубежом нет единых подходов к ведению пациентов с дисменореей. Национальные рекомендации и протоколы нуждаются в уточнении и консолидации. По-прежнему неясно, когда можно отдавать предпочтение монотерапии дротаверином, а в каких случаях полезно комбинировать его с НПВС и другими лекарственными средствами для достижения необходимого эффекта. Кроме того, ощущается недостаток современных данных о методах ведения пациентов с дисменореей в условиях рутинной врачебной практики. Поэтому при разработке дизайна международного наблюдательного исследования ведения пациентов с абдоминальными болями, обусловленными спазмом, было принято решение включить дисменорею в качестве одной из подлежащих изучению нозологий наряду с заболеваниями желудочно-кишечного тракта, желчевыводящих путей и мочеполовой системы.
Цель исследования: оценить эффективность оригинального дротаверина (препарат но-шпа) в повседневной практике лечения спастической боли в животе, обусловленной заболеваниями желудочно-кишечного тракта, желчевыводящих путей и урологического тракта, а также дисменореи. Среди задач исследования также было определение структуры пациентов, получающих при спастической абдоминальной боли дротаверин перорально вместе с другими видами лечения и определение быстроты действия дротаверина.
Материал и методы исследования
Международное, многоцентровое, проспективное, описательное, неинтервенционное регистровое исследование проводилось в Мексике, Казахстане и России.
Дизайн исследования
Регистр включал 2 части:
- Перекрестную часть, направленную на оценку заинтересованности и осведомленности врачей в отношении лечения спастической боли в животе в повседневной практике.
- Долговременную часть, которая включала 2 фазы:
- Фаза I – Предписываемая регистрация (Prescription Registry, PR): каждый врач вносил в предписываемую регистрацию данные обо всех последовательных, подходящих для участия в исследовании пациентов с болевым приступом спастического характера;
- Фаза II – Долговременная регистрация (Longitudinal Registry, LREG): каждый врач проводил 5-дневное (+3) исследование последующего наблюдения за первыми пятью последовательными, походящими для участия в исследовании пациентами, получающими препарат но-шпа.
Было запланировано три визита: визит включения (V1), визит последующего наблюдения (V2) через 3 полных дня лечения препаратом но-шпа и визит завершения (V3) через 5 (+3) дней после V1.
Лечение назначалось обычным способом и в соответствии с условиями одобренного регуляторными органами Регистрационного удостоверения препарата но-шпа.
В исследовании принимали участие 210 специалистов (из них 115 – российские врачи). В PR-фазу были включены 5507 пациентов, в LREG – 1116 пациентов, в том числе в России – 3000 и 600 пациентов соответственно.
Критериями включения в PR-фазу были: амбулаторные пациенты мужского или женского пола, в возрасте 18–65 лет с умеренной или сильной спастической болью в животе (≥4 по Цифровой рейтинговой шкале боли) в течение предшествующих 12 часов и острыми недавними эпизодами спастической боли (<12 часов), обусловленной урологическими заболеваниями (наличие камней в мочеточнике, пиелит), гастроэнтерологическими заболеваниями (синдром раздраженной толстой кишки (только в Мексике), холецистолитиаз, холангиолитиаз, холецистит, перихолецистит, холангит, папиллит), гинекологическими заболеваниями (дисменорея) после подписания формы информированного согласия перед включением. В LREG-фазе добавлялось лечение препаратом но-шпа.

Критериями исключения были пациенты с болью иного происхождения (например, боль при раке, невропатическая боль, суставная или мышечная боль), хирургический абдоминальный синдром, для LREG-фазы кроме вышеперечисленных критериев – препятствие последующему наблюдению, предшествующее участие в данном исследовании либо участие в другом исследовании.
В PR-фазе на строго анонимной основе регистрировали следующие данные: дату подписи информированного согласия, возраст, демографические показатели, критерии включения/невключения, диагноз, оценку боли пациентом, назначенное лечение в соответствии с различными типами спастической боли в животе (медикаментозное, другие виды лечения), а также количество дней отпуска по болезни из-за боли в течение недели перед включением в иследование. Использовалась Цифровая рейтинговая шкала боли (Numeric Pain Rating Scale, NPRS), где 0 было отсутствие боли, а 10 – самая сильная боль на протяжении последних 12 часов.
В LREG-фазе данные собирали с помощью индивидуальных регистрационных карт, заполняемых в ходе трех визитов следующим образом:
- При визите включения (V1): критерии включения/невключения, основные показатели жизнедеятельности организма (вес, рост), описание боли: продолжительность текущего приступа, предшествующее лечение (тип, продолжительность), доза и продолжительность приема препарата но-шпа.
- При визите последующего наблюдения (V2) спустя 3 полных дня лечения: анамнез боли со времени последнего визита (начало действия после первого приема препарата по визуальной аналоговой шкале (Visual Analogue Scale, VAS), количество дней нетрудоспособности по болезни из-за боли), оценка боли пациентом (NPRS) на протяжении предшествующих 12 часов, назначенное лечение (продолжительность лечения препаратом но-шпа, изменения в назначенном лечении препаратом но-шпа, другие виды лечения).
- При визите завершения (V3) 5 (+3) дней после V1: кроме того, что указано выше, собирали анамнез боли со времени последнего визита (посещения врача, неотложное лечение), но без оценки по VAS, а также общую оценку эффективности лечения по мнению врача.
Данные, собранные с помощью опросника врача, предоставляли информацию об его/ее возрасте, поле, специализации (урология, гастроэнтерология, гинекология, врач общей практики), стаже работы, расположении участка (городской, сельский) и его типе (офис, клиника), общем количестве пациентов, осматриваемых каждый месяц, и общем количестве пациентов с острой болью в месяц, общем количестве коек (если таковые предусмотрены), знании Руководств/Рекомендаций, заинтересованности и использовании Руководств/Рекомендаций.
Статистические методы. Количественные переменные были рассчитаны с помощью следующих параметров: количество не пропущенных данных, среднее (m) и стандартное (SD) отклонение, двусторонний 95% доверительный интервал среднего, медиана, минимум и максимум. Качественные переменные были подытожены с помощью следующих параметров: количество не пропущенных данных, подсчеты и проценты. Пропущенные данные или неизвестные ответы в процентах не учитывались. В отношении анализов основных и дополнительных критериев сравнения между группами проводили посредством дисперсионного анализа (ANOVA) количественных данных (проводимого на упорядоченных данных в случае отклонения от распределения Гаусса); точного критерия Фишера для неупорядоченных качественных данных; критерия Крускала–Уоллиса для упорядоченных качественных данных.
Результаты
Большинство участвующих в исследовании врачей были гинекологами (52,9%), гастроэнтерологи составили 23,1%, врачи общей практики – 13,0% и урологи – 8,7%. Исследование было завершено 821 пациентом, что соответствует 14,9% изначально включенных пациентов и 73,6% пациентов, включенных в LREG-фазу. Преждевременно вышли из исследования 60 человек. Основными причинами преждевременного выхода из исследования было прекращение боли (n=56, 93,3%), решение пациента (n=2, 3,3%), госпитализация (n=1, 1,6%) и только у одного пациента – отсутствие эффективности (n=1, 1,6%), что позволяет сделать вывод, что но-шпа – препарат, обладающий высокой эффективностью.
Среди пациентов PR-популяции большинство были женщинами (85,7%). Средний возраст составлял 34,9±12,7 года с диапазоном 18–65 лет, а три четверти пациентов (75,8%) относились к возрастной группе 18–45 лет. Дисменореей страдали 61,4% принявших участие в исследовании женщин. Кроме того, женщины с дисменореей были самыми молодыми, их средний возраст составлял 27,7±7,2 года.
Средняя оценка по шкале NPRS составляла 6,8±1,6 балла. 75,5% проходили лечение препаратом но-шпа со средней продолжительностью 5,3±2,7 дня, из них большинство (72,2%) проходили это лечение в виде монотерапии.
Продолжительность лечения пациентов с диагнозом дисменорея была самой короткой – 4,8±1,8 дня (самая большая средняя продолжительность лечения препаратом но-шпа наблюдалась у пациентов с холецистолитиазом – 6,5±3,6 дня).
Среди пациентов LREG популяции также большинство пациентов были женщинами (85,7%). Средний возраст составлял 34,2±12,5 года с диапазоном 18–65 лет. Дисменореей страдали 53,5% пациентов. Средняя оценка по Цифровой рейтинговой шкале боли составляла 7,3±1,5. Из 881 пациентов, которым был назначен препарат но-шпа, большинство проходили это лечение в виде монотерапии (76,3%). Лечение препаратом но-шпа было назначено в средней суточной дозе 149,3±58,5 мг (медиана: 120 мг), средняя продолжительность лечения составляла 5,7±4,0 дня. В отношении схемы лечения средняя суточная доза дротаверина, а также продолжительность лечения были немного выше у пациентов, принимающих препарат но-шпа в комбинации с другими препаратами, чем при монотерапии (соответственно 165,4±65,3 мг в сравнении с 144±55,4 мг и 6,1±2,8 дня в сравнении с 5,6±4,6 дня; в каждом случае p<0,0001). 327 пациентам (37,1%) ранее назначалась фармакотерапия, чаще всего неопиоидными анальгетиками (24,2%) и дротаверином (7,2%), другими препаратами пользовались 7,7% пациентов. Всем пациентам из LREG популяции в соответствии с дизайном исследования назначали дротаверин, при этом приблизительно четверти (235 пациентов, 26,7%) назначили сопутствующую терапию. Чаще всего сопутствующими препаратами были неопиоидные анальгетики (14,6%), другие лекарственные средства назначались в 9,6% случаев.
В ходе исследования была отмечена высокая доля ответивших на терапию (88,9%). При дисменорее этот показатель составил 89,4% (табл. 1).
Оценка по шкале NPRS
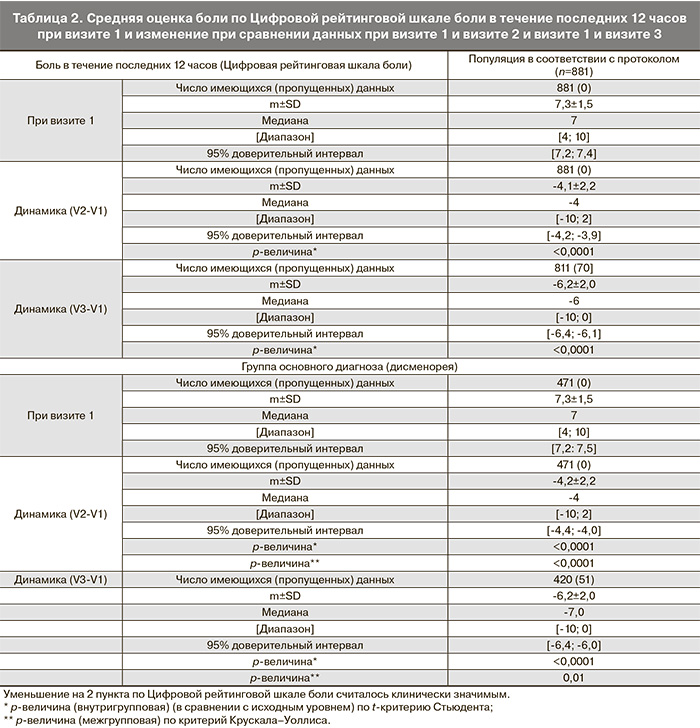
По шкале NPRS, отражающей выраженность боли в течение последних 12 часов, по сравнению с исходным уровнем (V1) отмечалось выраженное и статистически значимое уменьшение средних оценок боли при визите 2 (V2) (-4,1±2,2) и при визите 3 (V3) (-6,2±2,0) (p<0,0001 при обоих визитах). Это было справедливо и в группе пациенток с дисменореей: среднее изменение по сравнению с исходным уровнем составило -4,2±2,2 при визите 2 (V2) и -6,2±2,0 при визите 3 (V3) (p<0,0001 при обоих визитах). Между группами монотерапии и комбинированной терапии не отмечалось статистически значимых различий в изменении средних оценок по NPRS (соответственно -4,1±2,2 в сравнении с -4,2±2,2 между V1 и V2 (p=0,6379); и -6,2±2,0 в сравнении с -6,3±2,0 между V1 и V3 (p=0,9634)) (табл. 2).
На рис. 1 (см. на вклейке) графически представлена динамика средних оценок боли при каждом визите в соответствии с группами по диагнозам. Независимо от диагноза средняя оценка боли в ходе исследования от визита 1 до визита 3 выраженно и последовательно снижалась.
Оценка по визуальной аналоговой шкале (VAS)
По сравнению с первой оценкой, выполненной через 15 минут после приема (ВАШ15 мин), средняя тяжесть боли неуклонно уменьшалась через 30 (-2,2±1,3; p<0,0001) и через 60 минут после приема препарата но-шпа (-4,4±1,9; p<0,0001). Различия были статистически достоверными как в группе пациентов, страдающих дисменореей (p<0,0001), так и в остальных группах пациентов. Статистически значимая разница между этими группами по диагнозу отмечалось только через 60 минут после приема (p=0,0074) (рис. 2 см. на вклейке).
Кроме того, среднее уменьшение тяжести боли было незначительно более выражено у пациентов, принимающих препарат но-шпа в виде монотерапии, чем у пациентов, получающих этот препарат при комбинированной терапии в промежуток времени между 15 и 30 минутами после приема препарата (соответственно -2,2±1,4 в сравнении с -2,2±1,2; p=0,0265); но в промежуток времени между 15 и 60 минутами после приема препарата не отмечалось статистически значимой разницы (соответственно -4,5±1,9 в сравнении с -4,4±1,8; p=0,3624).
В целом 66,1% пациентов были удовлетворены эффективностью лечения, а 27,2% были в высшей степени удовлетворены. 5,9% из них были отчасти удовлетворены, и только 0,5% не предоставили однозначного ответа. Следует отметить, что сообщений о нежелательных явлениях в ходе исследования не поступало.
Обсуждение
Данное исследование было направлено на оценку применения в реальной практике препарата но-шпа (дротаверина) при лечении абдоминальных болей, обусловленных спазмом гладкой мускулатуры, при дисменорее, а также заболеваниях желудочно-кишечного тракта, желчевыводящих путей и мочевого тракта. Имея достаточно представительную выборку, исследование проводили в условиях рутинной врачебной практики. Такой тип исследования позволяет расширить знания об эффективности и безопасности дротаверина у пациентов, страдающих от спастической боли в животе. Как известно, чаще всего абдоминальная боль вызвана спазмом гладкой мускулатуры [3]. Блокируя простагландины как медиаторы воспаления и боли, монокомпонентные ненаркотические анальгетики, отпускаемые без рецепта врача, блокируют боль [10], но спазм при этом может остаться. Дротаверин снимает спазм, и вместе со спазмом уходит боль.
Подавляющее большинство пациентов, включенных в исследование, составляли женщины. Чаще всего сообщаемым диагнозом в этом исследовании была дисменорея. Этот результат не является неожиданным, поскольку гинекология была основной специализацией участвующих врачей (52,9%), а первичная дисменорея – это распространенное гинекологическое заболевание. Кроме того, пациенты, включенные в регистр, были относительно молодыми (их средний возраст составлял 31 год). Такой возрастной профиль характерен для женщин, страдающих от дисменореи, поскольку распространенность этого заболевания значительно сокращается по мере увеличения возраста; молодой возраст, а также курение и неприменение комбинированных оральных контрацептивов (КОК) являются независимыми факторами риска при первичной дисменорее. Доказано, что эстроген-содержащие КОК снижают выбросы простагландинов, в результате чего уменьшается сократительная маточная активность и боль. Имеются данные о снижении симптомов первичной дисменореи при использовании КОК до 70–80% [2, 3, 11, 12]. Однако хорошо известно, что использование КОК может быть связано с повышенным выведением магния из организма, поэтому целесообразно в составе комплексной терапии использовать цитрат и пидолат магния в комбинации с пиридоксином. Восполнение дефицита магния также способствует укреплению способности противостоять стрессу, обусловленному в том числе болезненными менструациями и сопутствующим снижением качества жизни [13, 14].
Что касается эффективности дротаверина, применяемого в средней суточной дозе 120 мг, то в ходе данного исследования отмечался высокий процент респондеров (88,9% – 783 из 881 вошедших в LREG-фазу). В связи с отсутствием эффекта вышел из исследования только 1 пациент из 881 LREG популяции. Также показательно статистически значимое снижение средних оценок боли в течение последних 12 часов (Цифровая рейтинговая шкала боли NPRS) в промежутках между визитами и значимое снижение тяжести боли через 30 и 60 минут после первого приема препарата. Эти данные в целом соответствуют данным российских и зарубежных исследований предыдущих лет. Так, в 4-летнем проспективном исследовании оценивалась эффективность использования дротаверина у 1400 пациенток с гинекологическими заболеваниями (нарушениями менструаций, воспалением органов гениталий, овуляционной болью и др.), в том числе у 175 женщин с дисменореей. Препарат но-шпа применялся в виде инъекций или перорально в дозе 120 мг/сут.
Эффективность препарата но-шпа у больных дисменореей была отмечена в 57,1% наблюдений [15, 16]. В другом ретроспективном исследованим эффективности спазмолитического действия препарата но-шпа с участием 358 женщин с заболеваниями репродуктивной системы (главным образом дисменореей) у 85% больных отмечено полное купирование боли, у 10% – частичное; при этом у 85% пациенток эффект отмечался в течение 30 мин [17, 18].
Полученные данные позволяют сделать вывод об эффективности дротаверина в терапии дисменореи и других болевых синдромов, вызванных спазмом гладкой мускулатуры, поскольку большинство пациентов были удовлетворены или очень удовлетворены лечением (93,3%). При этом не отмечалось значимых различий в эффективности препарата при монотерапии или комбинированной терапии.
Вышеперечисленные доказательства эффективности препарата но-шпа в терапии дисменореи в условиях реальной клинической практики, а также высокая безопасность препарата (не было сообщений о нежелательных явлениях) позволяют поставить вопрос о включении дротаверина в национальные рекомендации по ведению пациентов с дисменореей.



