Тромбоз воротной вены (ТВВ) – это обструкция ствола воротной вены и ее ветвей тромботическими массами, приводящая к нарушению кровотока в печени и желудочно-кишечном тракте. Существует множество приобретенных и наследственных факторов риска ТВВ. Среди приобретенных факторов часто отмечаются цирроз печени, солидный рак, миелопролиферативные заболевания, воспалительные заболевания кишечника, беременность, применение оральных контрацептивов. Наследственные факторы риска ТВВ включают в себя дефицит протеинов C, S, антитромбина III. Реже всего встречаются лейденская мутация фактора V, мутация фактора II, мутации гена метилентетрагидрофолатредуктазы (МТГФР), мутация JAK2V617F [1, 2].
На протяжении всей своей жизни женщины подвержены воздействию эстрогенов не только естественным путем во время репродуктивного периода и беременности, но и из-за экзогенного введения эстрогенсодержащих лекарств, таких как комбинированные оральные контрацептивы (КОК) [3]. Хоть и считается, что протромботические состояния редко встречаются среди здоровых женщин репродуктивного возраста (5–10 случаев на 10 000 женщин), однако имеются данные о влиянии КОК на риск тромбообразования путем воздействия эстрогенов на гемостатические факторы [4]. Использование КОК вызывает ряд изменений прокоагулянтного, антикоагулянтного и фибринолитического путей. Повышается уровень циркулирующих в плазме прокоагулянтных факторов, таких как фибриноген, протромбин, факторы VII, VIII и X, а также снижается содержание прокоагулянтного фактора V. На антикоагулянтном пути в плазме снижается уровень естественных ингибиторов гемостаза, таких как антитромбин и ингибитор пути тканевого фактора. На фибринолитическом пути наблюдаются повышенные уровни тканевого активатора плазминогена и плазминогена, а также пониженные уровни ингибитора 1 активатора плазминогена [3].
Развитие тромбоза на фоне заболевания новой коронавирусной инфекцией состоит из нескольких звеньев. Во-первых, это коагулопатия, связанная с повышением уровней фибриногена, D-димера и протромбина. Во-вторых, активируется воспалительный процесс с развитием «цитокинового шторма»: повышается уровень фактора некроза опухоли, интерлейкинов-6, -1β, что способствует нарушению свертываемости крови. В-третьих, вирус SARS-CoV-2 способен проникать в эндотелиоциты, что вызывает повреждение стенки сосуда с развитием эндотелиита [5].
Перечисленные процессы усугубляются у женщин с врожденной или приобретенной предрасположенностью к тромбозам (состояние гиперкоагуляции, тромбофилия) [3]. В качестве демонстрации данного положения приводим собственное клиническое наблюдение.
Клиническое наблюдение
Пациентка Н., 42 года, обратилась за помощью в дежурную хирургическую службу Первой Республиканской клинической больницы (1-й РКБ) Министерства здравоохранения Удмуртской Республики с жалобами на опоясывающие боли в животе спастического характера в течение дня, общую слабость, повышение температуры тела до 37,5°С.
Анамнез заболевания. Заболела остро 03.07.2021 г., когда на фоне полного здоровья появились нестерпимые постоянные боли в животе нарастающего характера. Обратилась за помощью к терапевту, были назначены спазмолитики, 09.07.2021 г. выполнена фиброгастродуоденоскопия, в ходе которой выявлены геморрагический Нр-ассоциированный рефлюкс-гастрит, катаральный бульбит. Периодически отмечала повышение температуры до 37,5°С. Прием дротаверина не оказывал желаемого эффекта. В связи с усилением болевого синдрома обратилась в приемное отделение 1-й РКБ, где была осмотрена дежурным хирургом. С целью дифференциальной диагностики было выполнено ультразвуковое исследование (УЗИ) органов брюшной полости, выявлены признаки тромбоза воротной системы. Пациентке предложена госпитализация, от которой она отказалась. Рекомендована консультация сосудистого хирурга. Осмотрена сосудистым хирургом в приемном отделении Республиканского клинико-диагностического центра, рекомендовано лечение в хирургическом отделении. Пациентка повторно обратилась в 1-ю РКБ 10.07.2021 г., была госпитализирована в хирургическое отделение, где получала консервативное лечение до 22.07.2021 г. с диагнозом: Подострый флеботромбоз воротной вены на фоне приема КОК? Получала эноксапарин 0,6 мл 2 раза в день, кеторолак, омепразол, диклофенак, ацетилсалициловую кислоту, урсодезоксихолевую кислоту (УДХК). На фоне терапии наблюдалась положительная динамика: уменьшение болевого синдрома (уменьшилась потребность в нестероидных противовоспалительных препаратах (НПВП) до 1 раза в сутки). В связи с отсутствием показаний к оперативному лечению, длительностью тромбоза вен, а также учитывая наличие коллатерального кровотока 22.07.2021 г. переведена в гастроэнтерологическое отделение 1 РКБ для продолжения консервативного лечения.
Из анамнеза известно, что в течение полугода принимает КОК (Мидиана). Пациентка замужем, в анамнезе 2 беременности, 1 роды, которые закончились рождением здорового ребенка, 1 аборт. Имеет отягощенную наследственность – у матери тромбофлебит, у бабушки тромбофлебит вен руки, тромбоэмболия легочной артерии. Перенесла COVID-19 3 месяца назад в легкой форме.
Объективно. Общее состояние удовлетворительное. Сознание ясное. Положение активное. Конституция нормостеническая. Состояние питания нормальное. Кожные покровы бледные, достаточной влажности, нормальной температуры. Запах кожных покровов физиологический. Зев чистый, миндалины в норме. Дыхание везикулярное, хрипов нет. Частота дыхательных движений – 16 в минуту. Тоны сердца ясные, ритмичные. Частота сердечных сокращений – 88 в минуту, АД – 130/70 мм рт. ст. Язык влажный, обложен белым налетом. Живот при пальпации мягкий, безболезненный. Печень выступает из-под края реберной дуги на 3 см. Селезенка, почки не пальпируются. Периферических отеков нет.
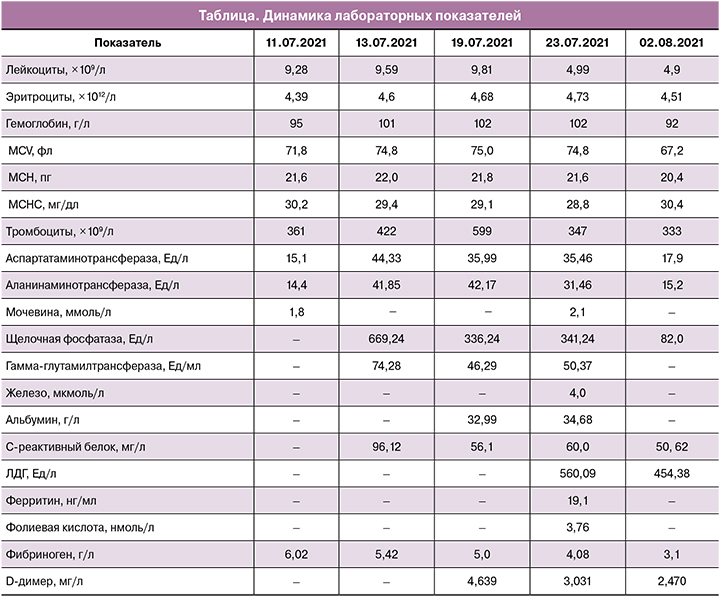
В анализах крови выявлены гипохромная анемия, холестатический, цитолитический и воспалительный синдромы, активация гемокоагуляции (таблица).
При исследовании кала от 27.07.2021 г. обнаружено: положительная реакция на скрытую кровь (++++), перевариваемые мышечные волокна (++), неперевариваемые (+), неперевариваемая клетчатка (++), перевариваемая (++), крахмал (+++), яйца глистов не найдены. Токсины А и В Clostridium difficile не найдены. Фекальный кальпротектин (02.08.2021 г.) – 48 мкг/г.
Определение однонуклеотидных полиморфизмов генов системы свертывания крови и фолатного цикла методом полимеразной цепной реакции (ПЦР) от 23.07.2021 г. выявило у пациентки мутантную гомозиготу PAI-1 – ген активатора плазминогена (серпин). ПЦР «real-time» на Jak-2 от 02.08.2021 г. – мутация не найдена.
При посеве крови и кала (02.08.2021 г.) роста патогенных микроорганизмов не обнаружено.
УЗИ органов брюшной полости от 12.07.2021 г.: Тромбоз портальной системы. Свободная жидкость в брюшной полости. Деформация желчного пузыря.
Спиральная компьютерная томография (СКТ) органов брюшной полости с внутривенным болюсным контрастированием, мультипланарной и трехмерной реконструкцией от 20.07.2021 г. (рис. 1, 2): КТ-картина тотального тромбоза портальной системы (воротная, селезеночная и брыжеечная вены). КТ-признаки формирования коллатерального портального кровотока в воротах печени, вторичного компенсаторного усиления артериального кровоснабжения печени. Признаки преходящих перфузионных нарушений в паренхиме печени. Спленомегалия. Дополнительная долька селезенки. Умеренное утолщение стенок тонкой кишки (вероятно, на фоне нарушения венозного оттока). Малый асцит.

Видеоколоноскопия от 28.07.2021 г.: Изъязвления подвздошной кишки, очаговая гиперплазия сигмовидной кишки, долихосигма.
На основании жалоб, данных анамнеза, объективного осмотра и лабораторно-инструментальных методов исследования был выставлен окончательный диагноз:
Основной: Тотальный тромбоз вен портальной системы от 03.07.2021 г. смешанного генеза (мутация гена PAI-1 активатора плазминогена (серпин) + прием КОК + постковидный синдром).
Осложнения: Портальная гипертензия (расширение селезеночной вены, спленомегалия, малый асцит). Вторичный гепатит (на фоне тромбоза вен портальной системы), активность 1-й степени. Гепатоцеллюлярная недостаточность 1-й степени. Вторичный эрозивный терминальный илеит смешанной этиологии (НПВП-ассоциированный + нарушение венозного оттока). Полидефицитная (железо-, фолиеводефицитная) анемия 2-й степени.
Сопутствующий: Хронический гастрит, ассоциированный с Нelicobacter рylori и дуоденогастральным рефлюксом, обострение. Очаговая гиперплазия сигмовидной кишки на фоне долихосигмы.
С 10.07.2021 г. по 23.07.2021 г. в хирургическом отделении пациентка получала следующее лечение: эноксапарин, кеторолак, омепразол, диклофенак, аспирин, УДХК, с 23.07.2021 г. по 03.08.2021 г. в гастроэнтерологическом отделении: дротаверин, кеторолак, адеметионин, омепразол, ацетилсалициловая кислота, УДХК, железа 3-гидроксидполимальтозат, фолиевая кислота, ребамипид.
Пациентка выписана 03.08.2021 г. с улучшением состояния. На фоне проведенной терапии наблюдались уменьшение абдоминального болевого синдрома, регресс лабораторных синдромов (цитолиза, холестаза, общевоспалительного), а также коагулопатии на фоне применения антикоагулянтов.
При выписке было рекомендовано: диспансерный учет у терапевта, наблюдение гематолога и гинеколога (с целью подбора метода контрацепции с учетом противопоказания для приема КОК), прием дабигатрана этексилата, ацетилсалициловой кислоты под контролем коагулограммы (протромбиновый индекс, D-димер, антитромбин-III 1 раз в месяц), ребамипида, железа 3-гидроксидполимальтозата (гемоглобин не менее 120 г/л), фолиевой кислоты. Начать прием витаминов группы В (цианокобаламин, пиридоксин, тиамин), при болях принимать гиосцина бутилбромид (при неэффективности метамизол натрия 500 мг однократно). Запланировать эрадикационную терапию 1-й линии не ранее чем через 6 месяцев: амоксициллин 1000 мг 2 раза в день + кларитромицин 500 мг 2 раза в день, эзомепразол 20 мг 2 раза в день 14 дней с последующим контролем эффективности эрадикационной терапии путем сдачи кала на Нelicobacter рylori через 2 месяца после эрадикационной терапии. Контрольное УЗИ органов брюшной полости с эластометрией печени и колоноскопия через 12 месяцев.
Обсуждение
Основная роль в развитии тромбозов редкой локализации принадлежит генетическим дефектам в системе гемостаза. Часто генетическим аномалиям сопутствуют приобретенные [6], что и описано в данном клиническом случае. У пациентки был диагностирован тотальный тромбоз вен портальной системы, который возник на фоне мутации гена PAI-1 активатора плазминогена (серпин). Наличие наследственной тромбофилии усугубилось приемом КОК, содержащих в своем составе эстроген (этинилэстрадиол) и гестаген (дроспиренон). Эстрогены обладают способностью к вазодилатации, что приводит к венозному застою. Кроме того, известно, что эстрогены увеличивают концентрацию VIII фактора, снижают уровень антитромбина III, протеина C и усиливают образование тромбина. Гестагены также оказывают существенное влияние на риск венозного тромбоза. Имеются данные об усилении ими тромботической активности эстрогенов [7].
Одним из клинически значимых нарушений у пациентов с COVID-19 является коагулопатия, характеризующаяся повышением концентрации фибриногена, протромбина и D-димера в плазме крови [8]. У описанной пациентки в анамнезе указывается новая коронавирусная инфекция, которая, очевидно, вызвала увеличение данных показателей и нарушения в системе гемостаза.
В условиях пандемии пациенткам, нуждающимся в контрацепции, но не желающим установить внутриматочную спираль, важно выбрать оптимальный метод регуляции репродуктивной функции. Существуют алгоритмы ведения женщин с диагнозом COVID-19, принимающих КОК, предложенные группой экспертов медицинских научных сообществ Испании. Согласно этим рекомендациям, при наличии факторов риска развития тромбоза (наследственная предрасположенность, сахарный диабет, пожилой возраст, артериальная гипертензия, заболевания сердечно-сосудистой системы, продолжительный стаж курения и т.д.), рекомендуется перейти на препараты, содержащие в своем составе прогестаген, в сочетании с низкомолекулярными гепаринами (НМГ) в профилактических дозах. Госпитализированным пациенткам, а также пациенткам в тяжелом состоянии рекомендуется прекратить прием КОК и начать использование НМГ в соответствии с протоколами лечения [9, 10].
Отсутствие полной ясности в понимании патогенеза абдоминальной (в том числе сосудистой) патологии у перенесших COVID-19, а также четкости в лечебных подходах при ТВВ предопределяет необходимость продолжения сбора клинических наблюдений данного состояния с целью разработки лечебно-диагностического алгоритма ведения таких больных [11, 12].
Заключение
Вопросы, касающиеся назначения КОК в условиях распространения инфекции COVID-19, до сих пор остаются нерешенными. Имеющиеся рекомендации вызывают сомнения в связи с недостаточной доказательной базой исследований. Рекомендации о продолжении приема КОК у пациенток с COVID-19 игнорируют тот факт, что при данном заболевании возможны нарушения свертывания крови, которые предполагают состояние гиперкоагуляции. Решение о продолжении применения КОК должно быть принято с учетом индивидуальных особенностей пациенток. Особого внимания при этом требуют пациентки с врожденными аномалиями системы гемостаза.



