HELLP-синдром является серьезным осложнением преэклампсии с высоким риском материнской (от 3,4 до 24,2%) и перинатальной (7,9%) смертности [1–4]. В случае образования субкапсулярной гематомы печени (СГП) материнская смертность возрастает до 86%, а перинатальная – до 80% [5–7]. Вместе с тем, это очень редкое осложнение гестационного процесса и единого мнения по лечению и тактике ведения таких пациентов не существует [5, 8–10]. В настоящем описании мы представляем клиническое наблюдение консервативного ведения пациентки с большой СГП, возникшей вследствие HELLP-синдрома.
Клиническое наблюдение
Первобеременная А., 30 лет, индекс массы тела 23,5 кг/м2, наблюдалась в женской консультации с раннего срока. До беременности отмечала эпизоды повышения артериального давления до 150/90 мм рт. ст., самостоятельно и нерегулярно принимала гипотензивные препараты. До 35 недель беременности артериальное давление не превышало 120/80 мм рт. ст. В течении одной недели появляются отеки нижних конечностей, артериальное давление повышается до 140/90–150/90 мм рт. ст. на фоне антигипертензивной терапии (метилдопа). Анализ мочи на суточную протеинурию отрицательный. На сроке 36 недель 6 дней остро возникли боли в эпигастральной области и диспептические расстройства – тошнота и рвота. Экстренно госпитализирована, проведена консультация хирурга для исключения острой хирургической патологии. При лабораторном обследовании наблюдалось относительное прогрессирование тромбоцитопении (со 180 до 160×109/л), повышение уровня трансаминаз (АЛТ 981 Ед/л, АСТ 1200 Ед/л, ЛДГ 1195 Ед/л), коагулограмма в пределах нормы. На этапе подготовки к родоразрешению проводится медикаментозная терапия: раствор сульфата магния 6 мл/ч, эгилок 25 мг 2 р/д, раствор альбумина 100,0 в/в кап., эниксум 0,3 п/к 1р/д. Однако, в этот же день в связи с тяжелой преэклампсией и HELLP-синдромом на сроке 37 недель была родоразрешена путем операции кесарева сечения. Операция была выполнена лапаротомией по Пфанненштилю, поперечным разрезом матки в нижнем сегменте, без технических сложностей. Был извлечен плод мужского пола массой 3440 г, рост 50 см, оценка по шкале Апгар 7–8 баллов. Кровопотеря по данным гравиметрического учета составила 610 мл. Однако, через два часа после операции были отмечены клинические признаки постгеморрагической анемии и снижение гемоглобина в периферической крови с исходного до операции 110 г/л до 87 г/л. Коагулограмма – АЧТВ 34 сек, ПТИ 70%, МНО 1,2, фибриноген 4,24 г/л, протромбин 17,0 сек. Наружного кровотечения не отмечено. По данным УЗИ свободной жидкости в брюшной полости не выявлено. Правая доля печени имеет размеры 142×102×65 мм, левая – 82×122×63 мм. На передней поверхности правой доли печени субкапсульно было обнаружено жидкостное образование с негомогенным содержимым размерами 144×59 мм, объемом 380 мл. С целью уточнения диагноза проведено РКТ с введением контраста. По ее результатам печень увеличена краниокаудально до 201 мм, структура паренхимы неоднородная за счет множественных и неравномерных скоплений контраста, в передних отделах правой доли субкапсулярно определяется неоднородная гематома размерами 166×69×146 мм. По данным МРТ (рис. 1) также подтверждено наличие подкапсульной гематомы верхних, передних и наружных отделов правой доли печени линзовидной формы, размерами 165×65×140 мм, неоднородной структуры с Т1-гипер- и Т2-гипоинтенсивными сгустками и жидкостным компонентом (лизированной кровью).
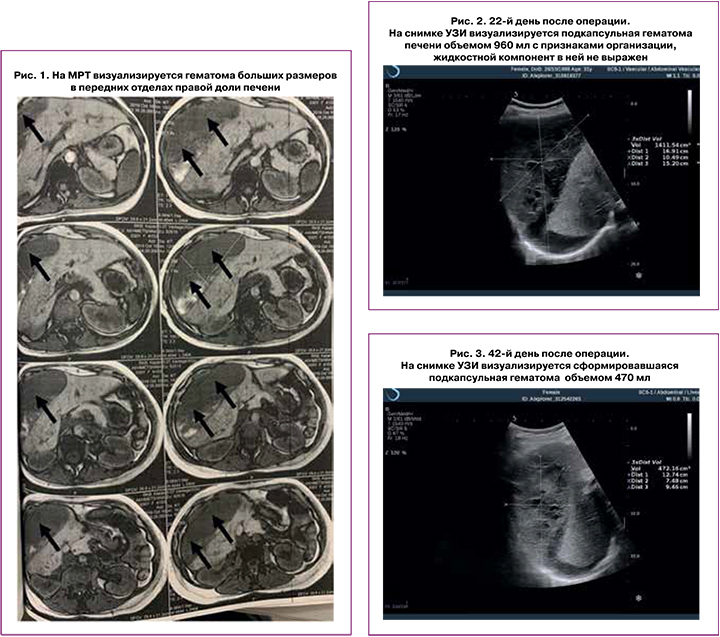
Учитывая высокий риск разрыва капсулы печени при хирургическом вмешательстве, отсутствие данных в литературе по лечению гематом таких больших размеров, принято решение о консервативном ведении пациентки. Продолжалась антианемическая и антигипертензивная терапия, эластичная компрессия нижних конечностей. Но решающим было постоянное наблюдение за жизненно важными функциями организма и состоянием гематомы, а в случае возможных осложнений, оказать оперативную помощь.
На 10-й день после операции появились жалобы на боли в правом подреберье при положении лежа на правом боку, усиливающиеся при смене положения и при движении. До данным УЗИ отмечено увеличение размеров гематомы (172×130 мм), с неоднородным содержимым и наличием свежих компонентов. Лабораторные данные: гемоглобин 110 г/л, лейкоциты 11,1×109/л, тромбоциты 374 000×109/л, АЛТ 66 ЕД/л, АСТ 33 ЕД/л. Решением междисциплинарного консилиума от оперативного вмешательства решено воздержаться и продолжить консервативную терапию под контролем витальных функции, лабораторных показателей и данных лучевых методов исследования.
На 15-й день во время очередного УЗИ был обнаружен окклюзирующий тромб в венах маточного сплетения справа и яичниковой вене, а также флотирующий тромб в нижне-полой вене. Дистанционно были проведены консультации с НИИ им. Н.В. Склифосовского и НМИЦ акушерства, гинекологии и перинатологии им. академика В.И. Кулакова. Учитывая наличие флотирующего венозного тромба, трансягулярным доступом справа был имплантирован удаляемый cava-фильтр фирмы «Cook». После имплантации cava-фильтра была назначена антикоагулянтная терапия низкомолекулярными гепаринами с последующим переводом на терапию антикоагулянтом непрямого действия – варфарином.
При последующем ультразвуковом контроле, выполненном на 22-й день после операции (рис. 2), были отмечены признаки организации подкапсульной гематомы правой доли печени, а также эхографические признаки начальной реканализации яичниковой вены и внутренней подвздошной вены справа.
При ультразвуковом исследовании органов брюшной полости, выполненном на 42-й день после операции (рис. 3), визуализировалась под диафрагмой и латерально от правой доли и верхней трети правого бокового кармана гематома объемом до 470 мл. В толще гематомы сосудов нет.
Обсуждение
Субкапсулярная гематома печени больших размеров у женщин с HELLP- синдромом и тяжелой преэклампсией редкое, но опасное осложнение с высоким риском массивного кровотечения. Развитие микроангиопатии и нарушение целостности эндотелия приводит к разрушению и оседанию эритроцитов в спазмированных сосудах. Изменение кровотока в сосудах печени нарушает работу печеночных клеток, повышается уровень трансаминаз с последующим развитием печеночной недостаточности. Повышение внутрипеченочного давления и перерастяжение фиброзной оболочки печени могло привести к формированию субкапсулярной гематомы. Описание данного клинического наблюдения демонстрирует не только такое редкое осложнение преэклампсии, но и особенности диагностики, течения и ведения после родоразрешения. Любая интервенция в гематому не давала гарантированного благоприятного исхода. Вынужденный отказ от медикаментозной профилактики тромбоэмболических осложнений на фоне подострой большой гематомы и развитие окклюзирующего тромбоза гроздевидного, маточного сплетений, яичниковой вены с формированием флотирующего тромба в нижне-полой вене усугубило клиническую ситуацию.
Заключение
Мы постарались проиллюстрировать возможность благоприятного исхода тяжелого жизнеугрожающего состояния в результате своевременно установленного диагноза, быстрого родоразрешения и бережного перевода в условия отделения анестезиологии-реанимации и интенсивной терапии крупного многопрофильного стационара. Междисциплинарное взаимодействие специалистов с регулярным и постоянным мониторингом с использованием лучевых и лабораторных методов позволило выбрать правильную тактику лечения. Приведенный клинический случай показывает, что при данном осложнении в условиях гемодинамической стабильности пациента возможно и предпочтительно консервативное ведение.



