Гистероскопия является инвазивным методом диагностики и лечения, который следует за неинвазивным трансвагинальным ультразвуковым исследованием (УЗИ), позволяющим с высокой точностью характеризовать внутриматочную патодогию (ВП) и получить информацию о состоянии стенок матки, и проводить довольно широкий спектр внутриматочных хирургических вмешательств [1–3].
Опыт проведения гистероскопий, накопленный в различных учреждениях России и мира, невозможно подвергнуть тщательному сравнительному анализу в связи с различными взглядами на оценку их исходов, а также в связи с отсутствием общепринятой классификации осложнений. Одни авторы, приводя статистику тысяч операций, просто перечисляют осложнения, другие выделяют «большие и малые повреждения», третьи оценку неблагоприятных ситуаций при гистероскопии ставят в зависимость от тяжести и опасности для жизни больного [4–6].
Воздушная эмболия (ВЭ) относится к интраоперационным осложнениям гистероскопии. Несвоевременное выявление ВЭ может привести к инвалидизации пациенток и стать причиной летальных исходов [7, 8].
 Corson и соавт. (1988) экспериментально доказал на овцах и козах прямым введением углекислого газа (СО2) в сосудистое русло (СО2 вводился от 30 до 90 мл в минуту), что использование СО2 как газовой среды расширения полости матки довольно эффективно из-за его способности быстрого растворения в крови, при этом отметив, что наличие у пациенток дефекта межжелудочковой перегородки и легочной гипертензии может привести к развитию газовой эмболии [8, 9].
Corson и соавт. (1988) экспериментально доказал на овцах и козах прямым введением углекислого газа (СО2) в сосудистое русло (СО2 вводился от 30 до 90 мл в минуту), что использование СО2 как газовой среды расширения полости матки довольно эффективно из-за его способности быстрого растворения в крови, при этом отметив, что наличие у пациенток дефекта межжелудочковой перегородки и легочной гипертензии может привести к развитию газовой эмболии [8, 9].
Bloomstone и соавт. (2002) описали случай, когда после проведения пациентке гистерорезектоскопии с использованием монополярной электрохирургии пузырьки воздуха обнаруживались в печеночных венах и правых отделах сердца, и предположили, что пузырьки газа появились на месте коагуляции тканей и проникли в сосудистое русло через небольшие по диаметру участки травм шейки матки [9, 10].
Целью исследования стало совершенствование методов профилактики ВЭ во время гистероскопии с учетом накопленного клинического опыта.
Материал и методы исследования
Проведено обсервационное продольное ретроспективное исследование по типу «случай – контроль» на базе ГКБ им. С.П. Боткина. Анализ хода вмешательств гистероскопий и развития ВЭ проводился путем исследования историй болезней 4590 женщин с ВП в возрасте от 19 до 85 лет, которым проводилась гистероскопия в период с января 2010 по январь 2013 года, из них у 815 (17,8%) пациенток проводились гистерорезектоскопии.
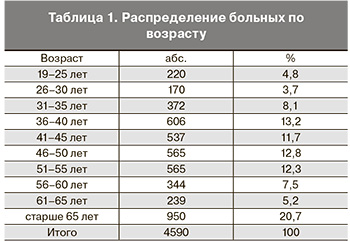
Распределение 4590 больных с ВП, которым проводилась диагностическая и оперативная гистероскопия, по возрасту представлено в табл. 1.
Всем женщинам до операции проводилось общеклиническое обследование, включавшее в себя лабораторные анализы крови, определение групповой принадлежности и резус-фактора крови, биохимических показателей, анализ крови на ВИЧ, реакцию Вассермана, HBS-антиген и HСV-антитела, общий анализ мочи и анализ выделений из влагалища на степень чистоты. Все женщины были осмотрены терапевтом, а при необходимости консультированы врачами смежных специальностей.
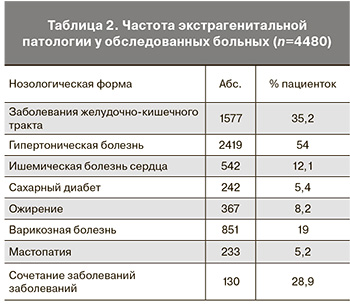
Сопутствующими заболеваниями страдали 4480 (97,6%) пациенток, нередко выявлялось сочетание нескольких заболеваний. В табл. 2 представлены данные об экстрагенитальных заболеваниях.
Для внутриматочной хирургии мы использовали 9-мм резектоскоп с телескопом диметром 4 мм и углами обзора в 00 и 120, диапевтические гистероскопии осуществляли с помощью панорамного операционного (терапевтического) двухканального (постоянно-проточного) гистероскопа с наружным диметром 8 мм – 30° и рабочим каналом 7 Fr для введения гибких и полугибких инструментов (щипцы, ножницы, электроды).
Полость матки расширяли жидкостями в зависимости от конкретной клинической ситуации, в объеме, определявшемся адекватностью расширения, достаточном для проведения операции.
 В качестве низковязких жидкостей для расширения полости матки мы использовали любую стерильную прозрачную кровесовместимую жидкость с учетом того, что при применении монополярной электрохирургической технологии используемая жидкость должна быть диэлектриком. Повседневные условия лечебной деятельности позволяли нам в качестве среды расширения полости матки при диагностических гистероскопиях использовать 5% раствор глюкозы ввиду возможного перехода на электрохирургическую технологию. При наличии противопоказаний для применения монополярной технологии применялась биполярная технология и физиологический раствор как среда расширения полости матки.
В качестве низковязких жидкостей для расширения полости матки мы использовали любую стерильную прозрачную кровесовместимую жидкость с учетом того, что при применении монополярной электрохирургической технологии используемая жидкость должна быть диэлектриком. Повседневные условия лечебной деятельности позволяли нам в качестве среды расширения полости матки при диагностических гистероскопиях использовать 5% раствор глюкозы ввиду возможного перехода на электрохирургическую технологию. При наличии противопоказаний для применения монополярной технологии применялась биполярная технология и физиологический раствор как среда расширения полости матки.
В своей практике мы использовали гравиметрический (весовой) метод контроля интравазации утероматом. Разработанная система включает в себя роликовый насос для подачи жидкости в заданном режиме и электронные весы, на которые устанавливается емкость для сбора жидкости, оттекающей из влагалища и гистероскопа. По ходу операции электронная система автоматически вычисляет разницу между притоком и оттоком, и выводит на экран монитора цифры израсходованной жидкости, объем интравазации, желаемые цифры внутриматочного давления и потока жидкости, а также объективно существующее (истинное) внутриматочное давление.
Трансвагинальное УЗИ как более информативное в плане выявления патологических процессов в матке и придатках применялось нами на этапах дооперационного исследования, интраоперационно и в послеоперационном периоде. Выполняли продольное и поперечное сканирование с определением положения, размеров матки, характеристики внутренней структуры, срединного маточного эха (М-эха) и состояния придатков матки.
Морфологические исследования биоптатов и операционного материала проводились в патологоанатомическом отделении больницы им. С.П. Боткина.
Обработку полученных данных выполняли с помощью пакета программ Statistica for Windows 6.0 Stat-Soft.
Результаты и их обсуждение
В проведенном исследовании мы не наблюдали развития ВЭ во время гистероскопии у больных с ВП.
Вследствие четкого соблюдения нами технологии проведения жидкостной гистероскопии у 3750 (81,7%) женщин с ВП без электрохирургических вмешательств не было даже условий для возникновения ВЭ:
- Горизонтальное положение тела больной во время проведения гистероскопии (исключение положения Тренделенбурга).
- Отсутствие пузырьков воздуха в системе подачи жидкости.
- Исключение попадания пузырьков воздуха в сосудистое русло.
- Применение роликового утеромата в качестве инструмента нагнетания жидкости.
- Введение гистероскопа в полость матки с предшествующей струей жидкости.
Несмотря на то что оперативная гистероскопия проводится с расширением полости матки жидкими средами, существует опасность возникновения ВЭ [11, 12]. Следует учитывать несколько механизмов возникновения ВЭ:
- Воздух находится в системе подачи жидкости;
- При извлечении гистероскопа из полости матки и его повторном введении воздух «вдавливается» в сосудистую систему;
- При расширенном цервикальном канале отрицательное давление в венозной системе может привести к аспирации воздуха;
- Повреждение стенки матки в области перешейка (часто при расширении);
- Электрохирургическая деструкция ткани в режиме «резки», «коагуляции», «вапоризации» сопровождается повышенным газообразованием [13–15].
Для исключения первого фактора ВЭ требуется освобождение системы подающих шлангов и гистероскопа от пузырьков воздуха, а также по возможности отказ от применения систем подачи жидкости, использующих давление воздуха.
Второй фактор часто встречается при применении резекционных технологий, когда требуется удаление из полости матки резецированных участков ткани. В этих случаях профилактика ВЭ сводится к созданию условий свободной эвакуации пузырьков воздуха из полости матки. Введение гистероскопа осуществляется в собранном виде с предшествующей подачей жидкости и с полностью открытым краном системы оттока.
Третий фактор – аспирация воздуха из окружающей среды возможен при применении положения Тренделенбурга в сочетании с оставленным в цервикальном канале открытым «наружным» стволом резектоскопа (например, замена электродов). Профилактика сводится к обтурации просвета «наружного» ствола мандреном.
Чтобы исключить четвертый фактор ВЭ, мы предлагаем медленную поступательную дилатацию цервикального канала и дозированное усилие при введении металлических расширителей.
Чаще всего по ходу вмешательства создаются условия для возникновения пятого фактора ВЭ. Образующиеся в процессе электрохирургической термической деструкции тканей пузырьки газа по своему составу ближе к «воздуху» и скапливаются под передней стенкой матки и в области трубных углов. Эвакуация образующихся пузырьков газа может потребовать значительного времени, превышающего зачастую непосредственно время деструкции тканей матки. Помимо риска «газовой – воздушной» эмболии, активация электрода в газовой среде может привести к взрывоподобной вспышке скопившегося в полости матки газа.
Мы рекомендуем следующие приемы эвакуации образующихся пузырьков газа и профилактики ВЭ:
- Положение больной в позиции Тренделенбурга;
- Обеспечение постоянной внутриматочной циркуляции жидкости;
- Подведение перфорированного конца резектоскопа (начало системы оттока) к месту скопления пузырьков газа;
- Расположение рукоятки резектоскопа выше уровня полости матки.
В случае применения коагуляционной технологии в первую очередь обрабатывается передняя стенка матки с целью перекрытия просвета сосудов, а при необходимости резекции эндомиометрия передняя стенка подвергается деструкции в последнюю очередь.
Использование полученных нами данных позволит уменьшить возможные случаи ВЭ во время выполнения гистероскопии, а предлагаемые методы профилактики обеспечат безопасность вмешательства.



