Преждевременные роды (ПР) являются значимой мировой проблемой акушерства и неонатологии. По оценкам ВОЗ ежегодно до 15 млн детей рождаются преждевременно, а 1 млн умирает из-за осложнений, связанных с ПР. По данным ВОЗ на долю недоношенных детей приходится до 60–70% ранней неонатальной смертности, а мертворождаемость при ПР выше в 8–13 раз [1]. С учетом изменившейся статистики за 2012 г. не только увеличилось количество ПР, но и значительно изменились такие показатели, как ранняя неонатальная смертность и мертворождаемость. Во всем мире они являются критериями оценки не только женского здоровья и эффективности работы акушерско-гинекологической службы, но и в целом социально-экономического благополучия всей страны.
На сегодняшний день уже разработаны определенные меры, направленные на снижение количества ПР и соответственно перинатальных потерь. Согласно клиническому протоколу по ПР к достоверным методам диагностики ПР следует отнести определение фибронектина в цервикальной слизи и трансвагинальную цервикометрию [2].
Определение фибронектина информативно только после 22 недель гестации [3] и пока не является общедоступным. В отношении цервикометрии доказано, что риск спонтанных ПР обратно пропорционален длине шейки матки. А при длине цервикального канала 15 мм и менее риск ПР возрастает экспоненциально [4–6].
К факторам риска ПР относят:
- Анамнестические: одни и более ПР в анамнезе (приводят к увеличению риска ПР в 2,5 раза), два и более выскабливания полости матки, в том числе искусственные аборты; конизация или ампутация шейки матки.
- Факторы риска во время данной беременности: курение, низкий социально-экономический уровень жизни; низкий индекс массы тела, ожирение; стрессовая ситуация на работе и в семье, хронический стресс, депрессия; возраст младше 18 или старше 35 лет; интервал между беременностями менее 6 месяцев, многоплодная беременность; индуцированная беременность, многоводие или маловодие; тяжелые экстрагенитальные заболевания в стадии декомпенсации; инфекция мочевыводящих путей (в том числе бессимптомная бактериурия); пародонтит; цервико-вагинальная инфекция; маточные кровотечения в I и II триместрах беременности; предлежание плаценты; преждевременная отслойка нормально расположенной плаценты; хирургические вмешательства на органах брюшной полости; травмы; а также мужской пол плода и предраковые состояния шейки матки.
Внедрение протоколов в ежедневную клиническую практику, ранжирование пациенток по факторам риска и своевременное применение профилактических мероприятий является важной задачей амбулаторного звена акушерско-гинекологической службы.
Цель исследования: оценить эффективность мероприятий по профилактике ПР в группе риска, которая формируется на основании определения факторов риска и результатов цервикометрии в первом триместре беременности.
Материал и методы исследования
Исследование включало два основных этапа: ретроспективный и проспективный. В рамках ретроспективного исследования проведен анализ 198 историй родов в сроке гестации 22–28 недель. Анализ факторов риска ПР выполнен на основании данных анкетирования 2138 беременных в первом триместре.
Ультразвуковое исследование выполнено на аппарате Samsung Medison Accuvix A30, SonoAce R7. Цервикометрия проводилась трансвагинально. Все специалисты имеют сертификат фонда фетальной медицины (FetalMedicineFoundation – FMF).
При проспективном исследовании были изучены исходы беременности (816 случаев).
 Результаты
Результаты
Учитывая актуальность проблемы очень ранних преждевременных родов (ОРПР) и их вклад в перинатальные потери первой задачей исследования стало изучение факторов риска у рожениц в сроках гестации 22–28 недель (196 случаев). При стабильно высоких показателях диспансерного наблюдения беременных в женских консультациях (94-92%), среди рожениц в сроках 22–28 недель до 8% не находились на диспансерном учете. Анализ паритета показал, что 19% рожениц были первобеременными, на долю первородящих приходится 41%. Полученные данные говорят о том, что почти половина женщин, беременность которых закончилась ОРПР, изначально не входили в группу риска по ПР, соответственно не проведены в должном объеме профилактические мероприятия. Аналогичные данные представлены и FMF (https://fetalmedicine.org): лишь 15% женщин со спонтанными ПР имеют в анамнезе ПР или поздний самопроизвольный выкидыш, на их долю приходится только 3% всех беременных. Оставшиеся 85% составляют первородящие и женщины, имеющие в анамнезе срочные роды. Поэтому любая стратегия, направленная только на группу беременных, имеющих ПР в анамнезе, будет иметь очень небольшой вклад в снижении общей частоты ПР.
В 2013 г. в Перми разработана и внедрена в практику система пренатальной диагностики первого триместра. Проведена централизация ультразвукового и биохимического скрининга на базе Центра пренатальной диагностики и планирования семьи при Пермском государственном медицинском университете им. академика Е.А. Вагнера, что позволило расширить рамки ультразвукового скрининга и начать работу по профилактике акушерских осложнений, в том числе ПР.
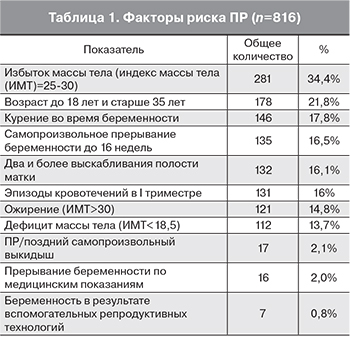
На этапе первичного приема акушера-гинеколога проводится консультирование и анкетирование беременных на раннем сроке с целью выявления групп риска по ПР. В результате первичного консультирования 2138 пациенток в сроке гестации до 12 недель 816 женщин имели 2 и более фактора риска ПР, что позволило отнести их в группу высокого риска. Как видно из данных, представленных в табл. 1, лидирующее место среди факторов риска занимает нарушение жирового обмена. Более половины пациенток (63%) имели отклонения.
Ожирение – одно из самых социально значимых хронических заболеваний, принявшее масштабы эпидемии. Постоянно растущие темпы распространения ожирения во всем мире, а также связанная с ожирением повышенная заболеваемость и смертность сделали его одной из наиболее актуальных проблем современного здравоохранения, причем все большее внимание привлекает ожирение беременных. Несмотря на постоянные усовершенствования системы антенатального наблюдения и родовспоможения, число беременных с ожирением в экономически развитых странах достигает 15,5–26,9% и постоянно увеличивается, в связи с чем актуальность этой проблемы приобретает особую значимость [7].
Одним из немногих предотвратимых факторов, обусловливающих рождение детей с низкой массой тела, ПР и перинатальную смертность, является курение. По нашим данным курение во время беременности занимало третье место среди всех факторов риска. Причем учитывали только факт активного курения самой пациенткой.
В последние десятилетия многочисленными научными исследованиями было доказано повреждающее воздействие табакокурения на репродуктивную функцию женщин и мужчин, включая все аспекты от фертильности до развития плода и ребенка, а также возможные исходы беременности. Это связано с содержанием 7000 токсических веществ в табачном дыме, из которых несколько тысяч непосредственно включаются в патологические механизмы, приводящие к нарушению репродуктивной функции и развития плода [8]. Во многих научных исследованиях изучены патологические механизмы воздействия угарного газа, металлов, полициклических ароматических углеводородов, находящихся как в прямом, так и в боковом потоке сигареты, которые попадают в организм беременной женщины как при активном, так и пассивном курении [9, 10].
Взаимосвязь активного табакокурения с ПР была установлена в результате мета-анализа 20 проспективных исследований (OR=1,27). Если учитывать интенсивность курения, то OR при легком курении равнялся 1,25, при средней интенсивности – 1,38, при высокой – 1,31. Также показана взаимосвязь между пассивным курением и ПР (OR=1,29 (95% CI, 0,97–1,72)) [11].
Следует отметить высокий процент внутриматочных вмешательств: самопроизвольное прерывание беременности до 16 недель – 16,5%; два и более выскабливания – 16,1%; прерывание беременности по медицинским показаниям – 2,0%.
Интересным является тот факт, что если стратегию рисков выстраивать с учетом ПР и поздних самопроизвольных выкидышей, то в группу риска будут отнесены только 2,0% пациенток.
Еще одним методом выявления пациенток группы риска по ПР является проведение цервикометрии. Сроки выполнения цервикометрии широко обсуждаются. Эффективность скрининга длины шейки матки в первом триместре беременности зависит от точности ее измерения [12]. Следует отметить, что существуют некоторые особенности проведения цервикометрии в первом триместре, регламентированные FMF. Оценка длины шейки матки проводится только трансвагинально. Необходим четкий сагитальный срез по всей длине цервикального канала с должным увеличением изображения. Измерить необходимо только эндоцервикс, не включая внутренний зев. В результате проведенного исследования, в котором участвовали 10 870 беременных, K.H. Nicolaides и соавт. пришли к выводу, что в 55% случаев благодаря цервикометрии в 12–14 недель можно спрогнозировать ПР до 34 недель при ложно-положительном результате в 10%. При этом спрогнозировать ПР в сроке 34–36 недель гестации возможно только в 20%. Следует отметить, что из исследования исключены беременные, принимавшие препараты прогестерона, а также женщины со швом на шейке матки [12].
В результате проведенной цервикометрии (рис. 1, 2) у 816 беременных группы риска по ПР средняя длина шейки матки составила 34±4,5 мм, укорочение шейки менее 30 мм зарегистрировано у 183 человек (22,4%): I группа – 163 беременных, у которых длина шейки варьировала от 29 до 26 мм (средняя длина 27 мм); II группа – 20 беременных – с длиной шейки 25 мм и менее (средняя длина 23 мм, минимальная 11 мм).
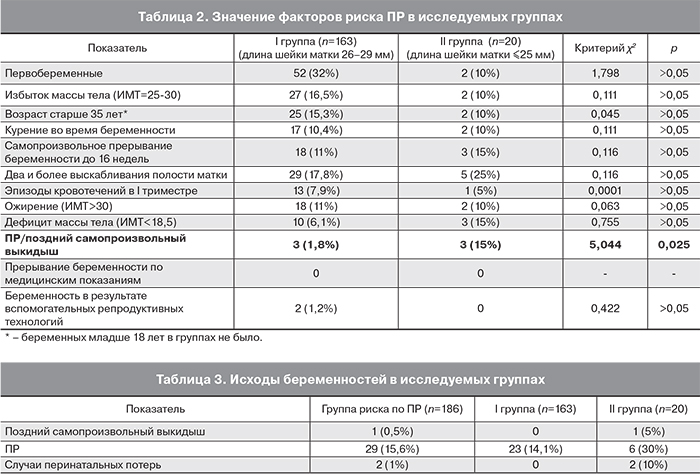
Сравнительный анализ факторов риска (табл. 2) показал, что группы имели достоверное различие только по одному фактору – наличие в анамнезе ПР или поздних самопроизвольных выкидышей. Представленные результаты говорят о необходимости включения цервикометрии в скрининг первого триместра. Однако следует помнить о необходимости тщательной подготовки кадров и увеличении времени, которое выделяется на проведение исследования.
Следующим и очень важным звеном комбинированного скрининга является консультирование пациенток по результатам исследований. С этой целью был организован специализированный прием беременных группы риска по ПР, задачей которого является индивидуальная оценка факторов риска и составление программы эффективных профилактических мероприятий.
Основой профилактики ПР на сегодняшний день является применение препаратов прогестерона в течение беременности до 34 недель [2]. Согласно протоколу по ПР, рекомендован микронизированный прогестерон 100–200 мг/сут вагинально. Однако на этапе первичного консультирования (срок беременности 6–9 недель) из 861 беременной, которые были отнесены в группу высокого риска, только 198 человек (23%) применяли препараты: 122 (62%) – использовали дидрогестерон (дюфастон) и 76 (38%) – микронизированный прогестерон (утрожестан). Принимая во внимание на проведенные ранее исследования, а также приверженность к применению одного гестагенного компонента в течение беременности, смену применяемого препарата не приветствовали.
В I группе тактика ведения заключалась в применении препаратов прогестерона: дидрогестерон 20 мг/сут, микронизированный прогестерон 200 мг/сут (выбор препарата зависел от выбора пациенткой пути введения и наличия побочных эффектов).
Контрольная цервикометрия, проведенная в сроке 18–21 недель, выявила в 29 случаях (17,8%) укорочение шейки матки до 25–23 мм. Опираясь на необходимость пролонгированного приема препаратов прогестерона и индивидуального информированного согласия, оба препарата применяли до 28 недель.
Эффективность проводимых профилактических мероприятий оценивалась по двум критериям: доношенная беременность и отсутствие перинатальных потерь. Срочными родами закончились 140 беременностей (85,9%), ПР – 23 (14,1%): в 28–33 недель – 5 (3,1%) случаев; в 34–36 недель – 18 случаев (11%). Случаев перинатальных потерь не зарегистрировано (табл. 3).
Тактика ведения беременных II группы несколько менялась с учетом исходных данных цервикометрии. Дидрогестерон применяли по схеме: 40 мг однократно, с последующим приемом по 10 мг через 8 часов. Микронизированный прогестерон назначали по 600 мг/сут вагинально. Контрольная цервикометрия проводилась через 10 дней и в сроке 16 и 18 недель гестации. В зависимости от результатов цервикометрии проводилась корректировка дозы с постепенным снижением до профилактических.
Исходы беременностей у женщин II группы являются менее позитивными. Однако следует учитывать изначальную клиническую ситуацию и малочисленность группы. ПР наблюдались в 6 случаях (30%), в 1 (5%) случае имел место поздний самопроизвольный выкидыш в сроке 20 недель (исходная длина шейки матки 18 мм). ОРПР в сроке 25 недель были в 1 случае (5%, при исходной длине шейки матки 22 мм), роды в сроке 28–33 недель в – 2 (10%) и в сроке 34–36 недель – в 3 (15%) случаях.
Таким образом, внедрение стратегии определения факторов риска ПР с момента первого обращения беременной позволяет значимо расширить группу риска, которая требует назначения гестагенов в профилактических дозах на ранних сроках. Полученные результаты позволяют рекомендовать проведение цервикометрии у пациенток группы риска по ПР в сроках 11–13 недель 6 дней.



