Наиболее частым осложнением во время родов являются акушерские кровотечения, частота которых составляет по данным зарубежных и отечественных авторов от 1 до 5% [1]. Акушерские кровотечения занимают одно из первых мест в структуре материнской заболеваемости и смертности во многих странах мира. На последовый и ранний послеродовый период приходится наибольшее число акушерских кровотечений. Наиболее частой причиной кровотечения в послеродовом периоде является гипотония матки. Среди факторов, приводящих к атонии матки, наиболее частыми являются: перерастяжение матки вследствие многоплодной беременности, многоводия, больших размеров плод; внутриматочная инфекция; длительные роды, родовозбуждение или активации родовой деятельности; наличие частей последа в матке; аномальное прикрепление плаценты. Нередко атония матки возникает у родильниц без выявленных факторов риска. Помимо этого, необходимо помнить, что иногда происходит снижение сократительной активности не всей матки, а только ее участков. Хорошо сократившееся дно матки может сочетаться с атонией нижнего маточного сегмента.
В опубликованном систематическом обзоре (2012) по результатам проведенных 7 исследований у 8247 пациенток показана эффективность активной тактики ведения третьего периода родов для профилактики гипотонических кровотечений у рожениц с высокими факторами риска [2]. Основная роль в активной тактике ведения третьего периода родов отводится утеротоникам, однако остается дискутабельным вопрос о выборе препарата. В нашей стране и за рубежом в качестве утеротоника используются синтетические аналоги окситоцина, алкалоиды спорыньи (эргометрин), простагландины. Наиболее широко используется окситоцин. Существенным минусом этого препарата является быстрый период полувыведения, что требует постоянного его введения. Применение метилэргометрина и простагландинов достаточно эффективно в качестве средств профилактики кровотечений в акушерстве, но их использование связано с высокой частотой побочных эффектов у пациенток: гипотония, тахикардия, увеличение сердечного выброса, ишемия миокарда, гиперемия, тошнота, рвота [2, 3].
 Карбетоцин является длительно действующим аналогом окситоцина, имеет аналогичные с натуральным окситоцином фармакологические свойства. Связываясь с рецепторами гладкой мускулатуры матки, вызывает ритмичные сокращения, повышая частоту сокращений и тонус матки. Потенциальным преимуществом карбетоцина перед окситоцином является большая продолжительность его действия. Одной дозы карбетоцина 100 мкг достаточно для того, чтобы сохранялись адекватные сокращения матки, что можно сравнить с введением окситоцина, действующим в течение нескольких часов. Как показали исследования D.J. Hunter и соавт. (1992), однократное введение карбетоцина в дозе 8–30 мкг (болюсно, внутривенно) или 10–70 мкг (внутримышечно) вызывают тетанические сокращения матки, после чего наступают ритмические сокращения в течение 60 минут при внутривенном введении и в течение 120 минут при внутримышечном введении препарата [4].
Карбетоцин является длительно действующим аналогом окситоцина, имеет аналогичные с натуральным окситоцином фармакологические свойства. Связываясь с рецепторами гладкой мускулатуры матки, вызывает ритмичные сокращения, повышая частоту сокращений и тонус матки. Потенциальным преимуществом карбетоцина перед окситоцином является большая продолжительность его действия. Одной дозы карбетоцина 100 мкг достаточно для того, чтобы сохранялись адекватные сокращения матки, что можно сравнить с введением окситоцина, действующим в течение нескольких часов. Как показали исследования D.J. Hunter и соавт. (1992), однократное введение карбетоцина в дозе 8–30 мкг (болюсно, внутривенно) или 10–70 мкг (внутримышечно) вызывают тетанические сокращения матки, после чего наступают ритмические сокращения в течение 60 минут при внутривенном введении и в течение 120 минут при внутримышечном введении препарата [4].
В ряде работ показано, что применение карбетоцина в дозировке от 75 до 125 мкг сопровождалось меньшей частотой послеродовых кровотечений (ПРК), использования дополнительных утеротоников у пациентов после кесарева сечения, меньшим объемом кровопотери после кесарева сечения и более низкой частотой побочных эффектов при самопроизвольных и оперативных родах [5]. Однако есть работы, в которых показана эффективность более низкой дозировки [6]. Спектр токсичности карбетоцина подобен окситоцину.
Целью настоящей работы явилась оценка эффективности препарата карбетоцин для профилактики ПРК при самопроизвольных родах.
Материал и методы исследования
За период с июля 2013 г. по сентябрь 2014 г. в акушерских стационарах ГК «Мать и дитя» (Перинатальный медицинский центр, Клинический госпиталь Лапино) с целью профилактики ПРК при самопроизвольных родах у пациенток высокого риска 229 роженицам вводился карбетоцин. В группу сравнения были включены 200 пациенток у которых с этой же целью применялся окситоцин. Показанием для применения вышеуказанных препаратов стало наличие хотя бы одного фактора риска по кровотечению: высокий паритет, перерастяжение матки, значительное число внутриматочных вмешательств в анамнезе, внутриматочные инфекции, нарушение родовой деятельности, длительная активация родов окситоцином (более 6 часов), ПРК в анамнезе.
Роженицы обеих групп были сопоставимы по возрасту, паритету, весо-ростовым характеристикам. Все беременности были одноплодными, срок гестации составил более 36 недель.
В исследование не были включены пациентки с рубцом на матке, с многоплодной беременностью, низкой плацентацией, с нарушениями свертывающей системы крови, гестозом, тяжелыми экстрагенитальными заболеваниями.
При анализе структуры факторов риска акушерских кровотечений выявлено, что наибольшую долю составили большие размеры плода – 29,9%. Далее по частоте следовали высокий паритет – 27,0% и многоводие – 10,7%. Данные о частоте аномалий родовой деятельности, длительного второго периода родов и ПРК в анамнезе у наблюдаемых пациенток представлены в табл. 1.
У 376 родильниц (87,6%) был выявлен один фактор риска, у 36 (8,4%) – два фактора риска, у 10 (2,3%) – три фактора.
Карбетоцин вводился сразу после выделения последа в дозировке 100 мкг, однократно болюсно и внутримышечно. Окситоцин вводился внутривенно 10 ЕД в 400 мл 0,9 % раствора хлорида натрия в течение 30–60 мин.
В обеих группах наблюдения нами был изучен объем кровопотери, частота ПРК (кровопотеря, превышающая 0,5% от массы тела), проведения ручного обследования матки и наружно-внутренней компрессии матки на кулаке, частота трансфузии компонентов крови. Объем кровопотери рассчитывался гравиметрическим методом. Помимо этого, нами изучена частота побочных реакций, связанных с применением карбетоцина и окситоцина, возникших в течение часа после введения препаратов.
Результаты
 Возраст обследованных варьировал от 21 до 40 лет и в среднем составил 34±5,5 года. Из гинекологических заболеваний у 27 (6,3%) был неспецифический кольпит, по поводу которого проводилось лечение во время беременности, у 17 (4,0%) пациенток была миома матки малых размеров. В анамнезе у 120 (28,0%) женщин были артифициальные аборты, причем у 21 (4,9%) беременной было 4 и более абортов, кровотечение в раннем послеродовом периоде – у 22 (5,1%) женщин. Сопутствующих тяжелых хронических соматических заболеваний, осложняющих течение беременности, выявлено не было.
Возраст обследованных варьировал от 21 до 40 лет и в среднем составил 34±5,5 года. Из гинекологических заболеваний у 27 (6,3%) был неспецифический кольпит, по поводу которого проводилось лечение во время беременности, у 17 (4,0%) пациенток была миома матки малых размеров. В анамнезе у 120 (28,0%) женщин были артифициальные аборты, причем у 21 (4,9%) беременной было 4 и более абортов, кровотечение в раннем послеродовом периоде – у 22 (5,1%) женщин. Сопутствующих тяжелых хронических соматических заболеваний, осложняющих течение беременности, выявлено не было.
Среди обследованных женщин большую долю составили повторнородящие – 272 пациентки (63,4%). Вторые роды предстояли 154 (35,9%), третьи – 87 (20,3%), 4 и более роды – 31 (7,2%) беременной.
Продолжительность последового периода у пациенток обеих групп была одинаковой и составила в среднем 12,3±6,5 мин.
При оценке кровопотери выявлено, что доля пациенток с физиологической кровопотерей (менее 0,5% от массы тела) была больше в 1-й группе – 93,9% (n=215) против 90,5% (n=181). При этом средний объем кровопотери у таких пациенток составил 344,6±79,5 мл и 363,6±72,3 мл соответственно. У 12 (5,2%) пациенток основной группы и у 16 (8,0%) пациенток контрольной группы объем кровопотери составил более 0,5% массы тела (но не более 1 л), в среднем 678,8±106,5 и 695,3±127,5 мл в 1-й и 2-й группе соответственно. Кровотечение развилось в раннем послеродовом периоде, в среднем через 25±13 минут после выделения последа. Кровотечение потребовало проведения наружного массажа матки, введения дополнительной дозы окситоцина (одномоментно 5 ЕД внутримышечно и поддерживающая доза 10 ЕД в 500 мл физиологического раствора внутривенно) в течение 2–3 часов у всех пациенток с кровотечением; ручного обследования матки и наружно-внутренней компрессии матки на кулаке у 12 пациенток (5,2%) основной группы и 16 родильниц (8,0%) 2-й группы.
Кровопотеря более 1 л произошла у 2 (0,9%) рожениц 1-й группы (кровопотеря 1000 мл и 1200 мл) и у 3 (1,5%) из 2-й группы (кровопотеря от 1100 до 1500 мл). Все пациентки были повторнородящими, у 1 из них в анамнезе были неоднократные внутриматочные вмешательства по поводу медицинских абортов, у 2 родильниц длительность родов составила более 18 часов, проводилась родоактивация окситоцином. Одновременно с введением утеротонических препаратов пациенткам с кровопотерей более 1 литра произведено прошивание нисходящих ветвей маточных артерий, проводилась инфузионная терапия, вводилась свежезамороженная плазма из расчета 10 мл/кг массы тела. Гемодинамические показатели и показатели крови (гемоглобин, гематокрит, показатели свертывающей системы крови) у всех пациенток в течение последового и раннего послеродового периодов были в пределах нормы.
При анализе побочных реакций, связанных с применением карбетоцина и окситоцина, выявлено, что доля вышеуказанных осложнений была выше у родильниц после введения окситоцина – 22,0% (n=44). После использования карбетоцина реакции возникли у 17,0% (n=40). Основную долю пациенток, у которых отмечены побочные реакции, составили родильницы с одним осложнением – 35 из 40 (87,5%) в 1-й группе и 33 из 44 (75,0%) – во 2-й группе.
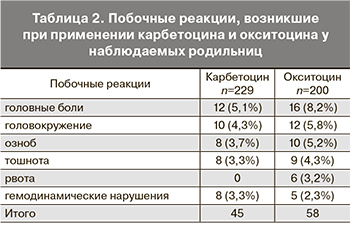
Введение карбетоцина сопровождалось меньшей частотой всех побочных реакций по сравнению с использованием окситоцина: головные боли, головокружение, озноб, тошнота, рвота, гемодинамические нарушения (гипертензия, гипотензия). Наиболее часто в обеих группах отмечены головные боли – у 5,1 и 8,2% в 1-й и во 2-й группе соответственно. Следующим по частоте следует головокружение – 4,3 и 5,8%, далее – озноб – 3,7 и 5,2% соответственно (табл. 2).
Следует отметить, что вышеперечисленные реакции могут быть клиническими признаками кровотечения, поэтому, несмотря на полученные результаты о частоте побочных эффектов, возникших после применения вышеуказанных препаратов, мы не можем достоверно утверждать о том, что возникшие реакции были связаны с введением препаратов, а не были вызваны возникшим кровотечением.
Заключение
Таким образом, результаты проведенного исследования показали высокую эффективность как карбетоцина, так и окситоцина для профилактики акушерских кровотечений у пациенток высокого риска. Однако доля пациенток с физиологической кровопотерей была выше в группе родильниц, у которых применялся карбетоцин, в то время как в группе пациенток, у которых использовался окситоцин, частота кровопотери более 0,5% массы тела и кровотечения более 1 литра была выше, хотя различия были статистически не достоверны. Отличительной особенностью карбетоцина является быстрота и пролонгированность действия препарата после однократного применения.



