Проблема менопаузы в XXI веке приобрела особое значение в связи со значительным увеличением продолжительности жизни женщин. Это особенно характерно для развитых стран. В частности, по данным Института экономики, к 2050 году средняя продолжительность жизни российских женщин увеличится до 84,5 года [1]. При этом возраст наступления менопаузы не меняется. В связи с этим более остро встают проблемы, связанные с этим периодом (развитие климактерических расстройств и различных патологических состояний). Главным пусковым механизмом в каскаде взаимосвязанных нарушений, приводящих к проблеме урогенитальных расстройств (УГР), является дефицит женских половых гормонов.
УГР – комплекс вагинальных и мочевых симптомов, связанных с развитием атрофических и дистрофических процессов в эстрогензависимых тканях и структурах нижней трети мочеполового тракта: мочевом пузыре, уретре, влагалище, связочном аппарате малого таза и мышцах тазового дна [2].
К вагинальным симптомам относятся: сухость, зуд, жжение во влагалище, опущение стенок влагалища, диспареуния, сексуальные нарушения, контактные кровянистые выделения, рецидивирующие выделения из влагалища.
Симптомы со стороны мочевыводящих путей достаточно разнообразны: частые болезненные мочеиспускания, рецидивирующие инфекции мочевых путей, поллакиурия (мочеиспускание более 8 раз в сутки), ноктурия (более одного эпизода мочеиспускания за ночь), ургентные позывы к мочеиспусканию, а также ургентный, стрессовый и смешанный тип недержания мочи.
Большинство пациенток с УГР умалчивают о существовании данной проблемы, так как считают это нормальным проявлением климакса. Урогенитальная атрофия (УГА) встречается у 30% женщин в возрасте 55 лет и у 75% в возрасте 70 лет.
В Бразилии было проведено исследование, включающее 622 женщины в возрасте от 50 лет и старше. Недержание мочи выявлено у 52,3% женщин, причем превалировал смешанный тип недержания мочи [3, 4].
Уменьшение уровня эндогенного эстрогена способствует развитию диспареунии у женщин в постменопаузе – истончение эпителия, уменьшение глубины и просвета вагинального канала, утрата складчатости влагалища, снижение любрикации, появление сухости вызывают боль и дискомфорт во время коитуса. Американскими и канадскими учеными было продемонстрировано улучшение сексуального здоровья женщины, имеющей начальные проявления УГР, при использовании местных увлажняющих смазок во время полового акта [5].
Урогенитальный тракт развивается из одних и тех же эмбриональных структур и имеет рецепторы с высокой чувствительностью к стероидным гормонам. Дистальная часть уретры, как и слизистая оболочка влагалища, покрыта многослойным ороговевающим эпителием, включающим 4 слоя последовательных клеток: базальный, парабазальный, промежуточный и поверхностный [6]. Снижение уровня эстрогенов в постменопаузальном периоде приводит к прекращению пролиферативных процессов в нем, вследствие чего происходит исчезновение слоев его промежуточных и поверхностных клеток. По данным C.M. Kunin и соавт., физиологическая десквамация клеток уретры представляет собой защитный механизм уретры. На поверхностных клетках происходит адгезия уропатогенов, которые легко вымываются с потоком мочи. Этот процесс препятствует развитию восходящей инфекции мочеполовых путей. В менопаузальном периоде адгезия уропатогенов происходит на базальных и парабазальных клетках, которые представляют собой резервуар. Поэтому риск возникновения инфекции мочеполовых путей в климактерическом периоде жизни женщины достаточно велик [7]. При этом установлено, что число рецидивов возрастает с увеличением длительности менопаузального периода.
Исчезновение промежуточных и поверхностных клеток в слизистой оболочке влагалища ведет к нарушению процесса образования гликогена и снижению количества лактобактерий, следствием чего является защелачивание вагинального содержимого до 5,5–6,8. Эти изменения снижают защитный механизм эпителия влагалища к факультативной флоре [8]. В ряде исследований было доказано, что при рН 5,4 во влагалище увеличивается Gardnerella vaginalis и Mobiluncus, при рН 5,7 – Clostridium sordellii, при рН 6,5 – бактерии вида Enterobactericeae, при рН 8,0 – Peptostreptococcus. Щелочная среда во влагалище повышает риск развития рецидивирующих инфекций мочеполовой системы. Около 10–15% женщин страдают от повторных эпизодов рецидивирующих инфекций мочевых путей [9]. Бессимптомная бактериурия наблюдается у 20% женщин старше 65 лет [10].
Рецепторы к эстрогенам расположены в нижней трети мочеточников, детрузоре, сосудистых сплетениях уретры, уротелии, матке, мышцах и эпителии влагалища (базальный, парабазальный слой), сосудах, мышцах тазового дна и связочном аппарате малого таза. Сравнительно недавно были опубликованы результаты зарубежных исследований, где с помощью иммунологических и иммуногистохимических методов были обнаружены эстроген-связывающие рецепторы – ERRα, ERRβ, ERRγ. На уровне ДНК они схожи с эстрогеновыми рецепторами ER. В исследовании приняли участие 40 женщин, которые были разделены на две группы по возрастному принципу. Первую группу составили женщины пременопаузального периода (возраст 47,1±3,7 года) с регулярным менструальным циклом; вторая группа женщин находилась в менопаузальном периоде (возраст 61,1±4,0 года). Материал для исследования был взят из задней стенки влагалища. В результате уровень ERRβ и ERα был одинаков в двух группах исследованных женщин, а ERRα, ERRγ и ERβ ниже в группе женщин, находящихся в менопаузальном периоде [11].
Согласно иммуногистохимии, ERα были обнаружены в большом количестве в эпителии, а ERβ – в гладкомышечных стенках сосудов слизистой влагалища. Присутствие ERβ в этих клетках подтверждает теорию о возможности восстановления кровообращения в слизистых мочеполового тракта при воздействии локальных форм эстриола.
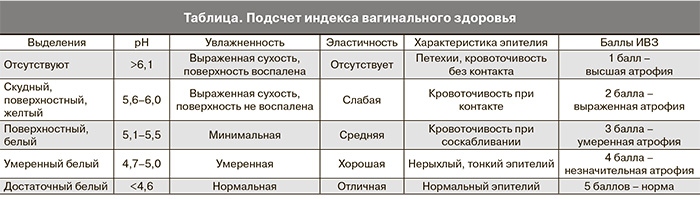
Наличие рецепторов эстрогенов в области влагалища объясняет высокую эффективность местного лечения вульвовагинальной атрофии. Эта терапия наиболее эффективна для уменьшения симптомов УГР [12]. Диагностика УГР осуществляется на основании жалоб, подробно собранного анамнеза и осмотра пациентки. Оценить вульвовагинальную атрофию возможно с помощью подсчета индекса вагинального здоровья (ИВЗ), используя такие показатели, как объем, качество, рН влагалищных выделений, состояние эпителия влагалища (таблица) [13].
В диагностике степени выраженности атрофических процессов во влагалище и оценке симптомов УГР используют 5-бальную шкалу D. Barlow. Незначительная проблема, не оказывающая влияния на повседневную жизнь – 1 балл; дискомфорт, периодически влияющий на повседневную жизнь – 2 балла; выраженная рецидивирующая проблема, влияющая на повседневную жизнь – 3 балла; выраженная проблема, влияющая на повседневную жизнь изо дня в день – 4 балла; крайне выраженная проблема, постоянно влияющая на повседневную жизнь – 5 баллов.
Для более точной оценки степени вульвовагинальной атрофии используют индекс созревания (ИС), представляющий собой численное соотношение всех парабазальных, промежуточных и поверхностных клеток в вагинальном мазке, выраженное в процентах. ИС обозначается в виде формулы, где слева записывается количество парабазальных клеток, посередине – промежуточных, справа – поверхностных. В случае отсутствия какого-либо вида клеток в соответствующем месте ставится цифра 0. При выраженной атрофии в мазках обнаруживаются только парабазальные клетки, промежуточные и поверхностные клетки отсутствуют, ИС=100/0/0. Картина умеренной атрофии соответствует формулам 70/30/0 или 50/50/0. На фоне пика эстрогенов ИС составляет 0/15/85 или 0/10/100. Таким образом, ИС оценивается по сдвигу формулы: сдвиг формулы влево свидетельствует об эстрогенном дефиците в организме женщины и развитии атрофии влагалища, вправо – о процессе пролиферации эпителия под воздействием эстрогенов.
Эстрогенная недостаточность в менопаузальном периоде приводит к приостановке пролиферации уротелия и возникновению хронического воспаления в мочевыводящих путях [14]. За счет этого увеличивается синтез нейроактивных субстанций в субуретральном пространстве мочевого пузыря: фактора роста нервов, цитокинов, простагландинов Е2, нейрокининов А, что приводит к нарушению синаптической передачи и повышению сократительной активности мышечных волокон детрузора и уретры [15, 16].
Терапия симптомов УГР включает применение гормональных и не гормональных препаратов. Гормональные препараты включают препараты системного и местного действия.
L. Cardozo и соавт. [17] было установлено, что местное применение эстрогенов значительно снижает выраженность симптомов нарушений мочеиспускания по сравнению с плацебо. В исследованиях принимали участие 466 женщин, из которых 236 получали эстрогенсодержащие препараты, 230 – плацебо. Из методологических неточностей отмечаются использование различных эстрогенов, короткие сроки применения и отсутствие четких критериев отбора пациенток. На фоне проводимой терапии отмечен дозозависимый эффект для системного применения. Местная терапия оказалась наиболее эффективной и предпочтительной при лечении гиперактивного мочевого пузыря у женщин старше 50 лет.
Проведенный мета-анализ 54 исследований выявил снижение симптомов УГР у женщин в постменопаузе при лечении локальными формами эстрогенов. Максимальная эффективность отмечалась к 3-му месяцу проводимой терапии [18–20]. В ряде исследований было установлено, что лечение УГР местными формами эстрогенов наиболее эффективно по сравнению с системной терапией. Локальные эстрогены не вызывают побочных явлений в виде тошноты, вульвовагинального кандидоза и нагрубания молочных желез.
К натуральным эстрогенам относятся эстрадиол, эстрон и эстриол. Преимуществом эстриола как препарата локального действия является короткий период нахождения в ядре клетки. Эстриол селективно связывается с рецепторами тканей мочеполовых путей на 2–4 часа, что, в свою очередь, не вызывает пролиферативных изменений в эндометрии матки [21, 22]. Для пролиферации эпителия уретры, вульвы и влагалища этого времени вполне достаточно. Таким образом, при вагинальном применении эстриол не оказывает системного действия и не требует добавления прогестагенов. Так, в Швеции не проводят систематических медицинских осмотров пациенткам, принимающим вагинальные формы эстриола на протяжении длительного периода времени.
В России давно и успешно применяют препарат овестин с действующим веществом эстриол. Несмотря на многолетний опыт применения этого препарата, спрос на него не только не угасает, но и увеличивается. Проведено множество исследований, которые продемонстрировали эффективность препарата в отношении УГА, приводящей к УГР. Овестин выпускается в виде вагинальных суппозиториев (в 1 суппозитории содержится 0,5 мг эстриола), крема (в 1 г – 1 мг эстриола, что соответствует 0,5 мг в дозе для введения) и таблеток (в 1 таблетке 2 мг эстриола). При местной терапии эстриолом лечебная доза составляет 0,5 мг ежедневно в течение 2–3 недель. Поддерживающая доза – 0,5 мг два раза в неделю, длительно. Эффект от проводимой терапии ощутим через 3–4 недели после начала лечения. Пациентки отмечают значительное уменьшение расстройств мочеиспускания, зуда, сухости, жжения и диспареунии. Овестин стимулирует пролиферацию эпителия влагалища, восстанавливает нормальную структуру слизистой влагалища и мочевого пузыря, препятствует развитию воспалительных процессов. На фоне лечения происходит сдвиг ИС эпителия вправо, изменяется рН (закисление) и ИВЗ [23]. Для полной пролиферации эпителия и появления достаточного количество транссудата необходимо проводить лечение на протяжении не менее 6 месяцев [6]. Эффективность лечения УГР выше в том случае, когда терапия пациентке назначена на начальных проявлениях УГА [10]. Было доказано, что 10% женщин предъявляют жалобы на сухость и зуд во влагалище в пременопаузальном периоде. Это связано с эстрогенным дефицитом, приводящим к нарушению кровообращения в слизистой. Уже с этого периода возможен индивидуальный подбор дозы препарата для предупреждения развития тяжелых форм УГР.
В 2011 г. была изучена динамика УГР в постменопаузальном периоде на фоне терапии овестином. Через 6 месяцев лечения большинство пациенток достоверно отмечали нормализацию мочеиспускания и снижение на 20% смешанного типа недержания мочи. Существенно изменились в сравнении с исходными данными показатели по шкале D. Barlow. В целом интенсивность симптомов снизилась от 4–5 баллов до 1–2 баллов. Пациентки ощущали значительное улучшение качества жизни по результатам анкетирования (настроение, работоспособность, отношение с партнером, чувство уверенности в себе и др.).
Применение овестина также показано в обследовании пациенток с неясной цитологической картиной. Под действием эстриола происходит пролиферация эпителия. Атрофический эпителий превращается в нормальный, а характеристика диспластичного эпителия не изменяется. Полученные данные позволяют применять овестин для дифференциальной диагностики при наличии сомнительных цитологических результатов.
Применяя овестин в виде крема или свечей, с успехом добиваются снижения симптомов УГР за счет следующих факторов:
- улучшение кровоснабжения влагалищной стенки, восстановление транссудации и ее эластичности;
- пролиферация влагалищного эпителия, увеличение синтеза гликогена, восстановление популяции лактобацилл во влагалищном биотопе, восстановление кислой среды влагалищного содержимого;
- улучшение кровоснабжения всех слоев уретры, восстановление ее мышечного тонуса, количества и качества коллагеновых структур, пролиферативных процессов в уротелии и увеличение слизи, что ведет к увеличению внутриуретрального давления и уменьшению симптомов стрессового недержания мочи;
- улучшение кровоснабжения детрузора и нормализация сократительной его активности путем улучшения трофики и развития адренорецепторов, а также мускариновых рецепторов, что повышает способность мочевого пузыря отвечать на эндогенную адренергическую стимуляцию;
- улучшение кровообращения, трофики и сократительной активности мышц тазового дна, коллагеновых структур, входящих в состав связочного аппарата малого таза, что также способствует удержанию мочи и препятствует опущению органов малого таза;
- секреция иммуноглобулинов парауретральными железами, что может являться одним из факторов, препятствующих развитию восходящей инфекции.
Заключение
Таким образом, терапевтическим стандартом коррекции УГР, вызванных атрофией слизистых, являются локальные формы эстрогенов. Овестин в форме крема и свечей является эффективным и безопасным препаратом, применяемым в комплексной терапии заболеваний, вызванных снижением содержания эстрогенов в организме женщины в менопаузальном периоде.



