Генитоуринарный менопаузальный синдром (ГУМС) – хроническое прогрессирующее заболевание, которое привлекает большое внимание специалистов в области женского здоровья во всем мире в связи с увеличением продолжительности жизни женщин и акцентом на качество жизни [1]. ГУМС представляет собой комплекс вагинальных, мочевых симптомов и сексуальных нарушений, возникающих вследствие дефицита эстрогенов и других половых стероидов и развивающихся на этом фоне анатомо-физиологических изменений во влагалище, уретре, мочевом пузыре, наружных половых органах, промежности и мышечно-связочном аппарате малого таза [2, 3]. По данным литературы симптомы и признаки ГУМС и вульвовагинальной атрофии (ВВА) встречаются у 27–84% женщин в пери- и постменопаузе [4]. В обзоре Donders G. et al. сообщается, что 15% женщин в пременопаузе также испытывают явные симптомы ВВА вследствие развития различных гипоэстрогенных состояний: дисгенезии гонад, преждевременной недостаточности яичников, функциональной гипоталамической аменореи, лечения препаратами с антиэстрогенным эффектом, длительного использования комбинированных гормональных контрацептивов, лактации [1]. Таким образом, проблема ГУМС/ВВА выходит за рамки только возраст-ассоциированных заболеваний. Важно также отметить, что выраженность симптоматики не всегда сопоставима с реальной тяжестью объективных признаков урогенитальной атрофии [5], но при этом может значительно ухудшить состояние здоровья, сексуальную функцию, приводить к серьезным психосоциальным проблемам [6, 7].
Знание современных научных данных в отношении эффективности и безопасности методов лечения ГУМС необходимо для оказания своевременной помощи женщинам, учитывая его крайне негативное влияние на качество жизни. «Золотым стандартом» лечения симптомов ГУМС является локальная терапия эстрогенами, показавшая высокую эффективность в клинических исследованиях [8, 9] и рекомендованная профессиональными сообществами специалистов [10–12]. Альтернативные методы лечения с использованием оспемифена и вагинального дегидроэпиандростерона (прастерона) продемонстрировали многообещающие результаты у женщин с симптомами ГУМС в постменопаузе [13–16].
Однако существующие противопоказания и ограничения по применению гормональной терапии, особенно эстрогенов (наличие эстрогенозависимых злокачественных новообразований, артериовенозные тромбозы в анамнезе, генетические тромбофилии высокого риска, порфирии) а также, в ряде случаев, гормонофобия и нежелание женщины использовать гормональные препараты, побуждают к поиску новых негормональных, эффективных и безопасных методов лечения ГУМС/ВВА [17, 18].
Цель исследования: оценить собственный опыт применения негормонального крема с гиалуроновой кислотой, фитокомплексом и лактобактериями у пациенток в пери- и постменопаузе для коррекции симптомов ГУМС/ВВА.
Продукт, использованный в исследовании
Крем дозированный «Триофемин» (свидетельство о государственной регистрации СГР ТС № KG.11.01.09.001.R.004629.09.24 от 16.09.2024) представляет комбинацию гиалуроновой кислоты, фитокомплекса и лактобактерий. Основой крема дозированного является натриевая соль гиалуроновой кислоты, которая агрегирует на себе молекулы воды и обеспечивает выраженный увлажняющий эффект. Фитокомплекс «Триофемина» представлен экстрактами дикого ямса, центеллы азиатской, красного клевера, листьев алоэ, обладающими тонизирующим, регенерирующим, противовоспалительным, антиоксидантным эффектами, а также стимулирующим процессы неоколлагенеза. Два штамма лактобактерий – Lactobacillus acidophilus, Lactobacillus casei rhamnosus Doderleini – способствуют восстановлению баланса микрофлоры, улучшают местные обменные процессы, восстанавливают защитные функции эпителия влагалища и нижних мочевых путей. «Триофемин» крем сформирован в виде свечей, каждая содержит дозу применения, что облегчает использование. «Триофемин» имеет безопасный состав по критериям ВОЗ [19].
Материалы и методы
В наблюдательное проспективное исследование, которое проводилось на базе отделения гинекологической эндокринологии ФГБУ НМИЦ АГП им. В.И. Кулакова МЗ РФ в период с ноября 2024 г. по сентябрь 2025 г., включено 40 пациенток с симптомами ГУМС/ВВА в возрасте от 46 до 75 лет.
На визите скрининга, после оценки состояния и подписания информированного согласия женщины получали крем «Триофемин», который использовали по следующей схеме: по 1 дозе на ночь во влагалище ежедневно в течение 4 недель, затем по 1 дозе 3 раза в неделю в течение 8 недель. Период наблюдения составил 12 недель.
Эффективность и безопасность лечения оценивалась по следующим критериям:
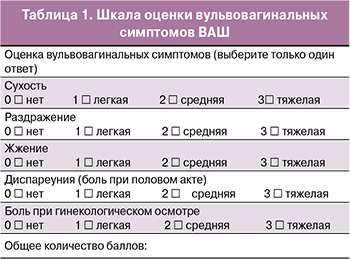
1. Адаптированная шкала для оценки вульвовагинальных симптомов (табл. 1). Участники исследования оценивали симптомы по 4-балльной шкале (0=нет; 1=легкая степень; 2=умеренная; 3=тяжелая), затем данные усреднялись для получения сводных оценок по визуально-аналоговой шкале (ВАШ). Более высокие показатели указывали на большее количество и тяжесть симптомов [20].
2. Гинекологический осмотр с определением pH влагалища. рН-метрию содержимого заднего свода влагалища проводили с помощью индикаторных полосок Кольпо-тест рН («Биосенсор АН», Россия) путем сопоставления окраски сенсорного элемента тест-полосок с соответствующими цветовыми полями шкалы. Цветовая шкала на этикетке содержит 12 цветовых полей, соответствующих значениям pH в ед.: 3,0; 3,5; 3,7; 4,0; 4,2; 4,5; 4,8; 5,0; 5,5; 6,0; 6,5 и 7,0.
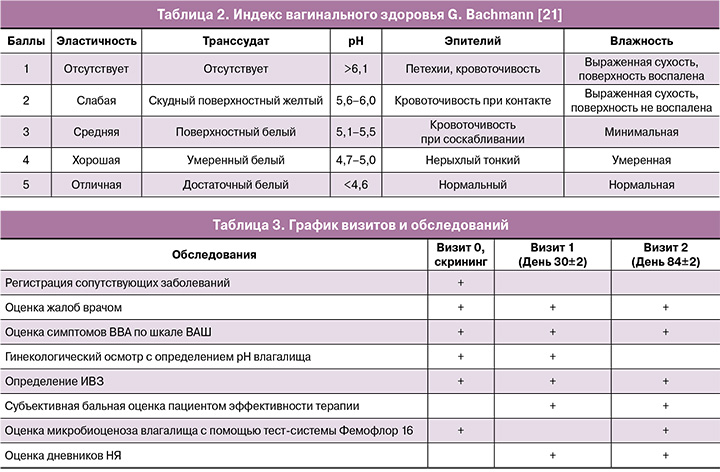
3. Определение индекса вагинального здоровья (ИВЗ) по G. Bachmann (табл. 2). Пять показателей ИВЗ оценивались по 5-балльной шкале: количество и качество отделяемого влагалища, pH, увлажненность, эластичность и толщина влагалищного эпителия. Результаты оценивались следующим образом: 20–25 баллов – норма, 15–20 баллов – незначительные атрофические изменения, менее 15 баллов – ВВА, менее 10 баллов – выраженные атрофические изменения [21].
4. Субъективная оценка пациенткой эффективности терапии кремом «Триофемин» от 0 до 10 баллов, где 0 – отсутствие эффекта от терапии, 10 баллов – максимальный эффект, т.е. полное отсутствие беспокоящих симптомов ГУМС/ВВА.
5. Оценка микробиоценоза влагалища. Для оценки микробиоценоза влагалища была использована тест-система Фемофлор-16, основанная на методе полимеразной цепной реакции (ПЦР) с детекцией результатов в режиме реального времени. В основу данного способа положена комплексная количественная оценка микрофлоры влагалища с проведением сравнительного анализа конкретных представителей нормо- и условно-патогенной микрофлоры с общим количеством микроорганизмов для выявления дисбаланса микробиоты и степени его выраженности.
6. Дневники нежелательных явлений (НЯ). Дневники НЯ выдавались на каждом визите. Пациентки указывали симптомы, время их возникновения, длительность и тяжесть.
График визитов и обследований представлен в таблице 3.
Статистический анализ
В процессе статистической обработки данных использовались: для обработки и визуализации данных – табличный процессор Microsoft Excel 2016; для построения регрессионных моделей влияния индивидуальных характеристик пациенток на динамику целевых показателей – программный пакет для эконометрического анализа gretl; для обработки данных, тестирования значимости изменения целевых показателей и визуализации данных – язык программирования Python (библиотеки pandas, scipy, matplotlib, sklearn).
Построение регрессионных моделей в gretl проводилось на основе метода наименьших квадратов. Выводы о значимости сделаны на основе теста Стьюдента. В качестве уровня значимости было принято значение в 5%.
Результаты
34 участницы из 40 завершили 12-недельный курс лечения и наблюдения. 6 пациенток исключены из исследования по следующим причинам: потеря связи, неявка на визит, нарушение режима применения исследуемого продукта, нежелательные явления в 2 случаях. Средний возраст пациенток, принявших участие в исследовании, составил 55±4 лет, средний возраст менопаузы – 6,6±3,2 лет (от 1 года до 20 лет). 28/40 женщин (70%) были замужем или имели половых партнеров и 12/40 пациенток (30%) не имели половых контактов.
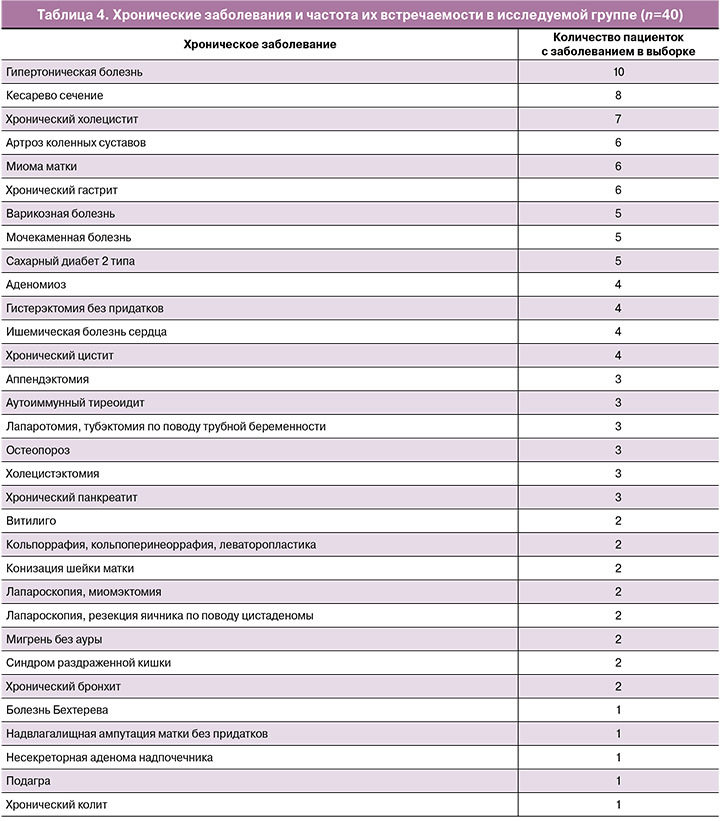
На этапе скрининга учитывался коморбидный статус пациенток с целью оценки потенциального влияния хронических заболеваний и сопутствующей терапии на эффективность применения крема «Триофемин» (табл. 4).
Согласно анкетированию, ведущей жалобой пациенток на визите скрининга являлась сухость во влагалище. Все женщины (n=34), чьи данные были включены в статистический анализ, оценили исходно этот симптом в 2–3 балла. К концу периода наблюдения 26/34 участниц (76,5%) не сообщали о наличии сухости во влагалище или отмечали значимое уменьшение симптома и оценивали его в 1 балл. 26/34 сексуально активных женщин (76,5%) отмечали боли при половом акте, а треть из них – периодические контактные кровянистые выделения. Кроме того, 22/34 (64,7%) пациентки отмечали раздражение во влагалище и в области вульвы, 18/34 (52,9%) – жжение и 20/34 участниц (58,8%) жаловались на боль при гинекологическом осмотре и предупреждали об этом врача. Анализ данных продемонстрировал значимое снижение количества баллов ВАШ по отдельным симптомам после трех месяцев терапии на 49–61%, при этом наибольший эффект был достигнут в отношении жжения, наименьший – в отношении диспареунии (рис. 1).
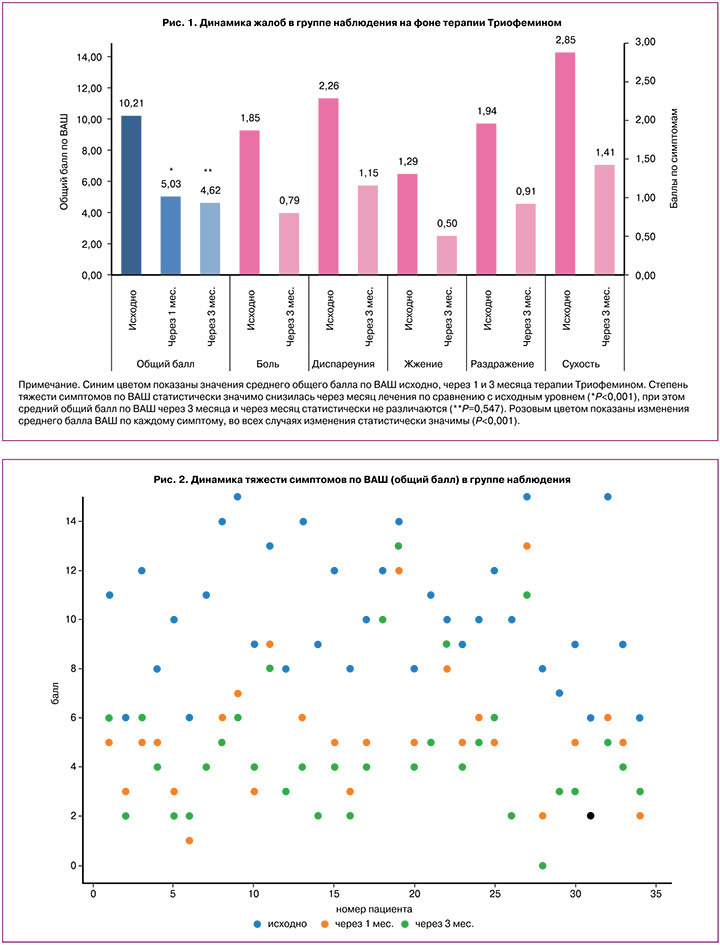
Через 1 месяц терапии кремом «Триофемин» средний общий балл по ВАШ снизился на 50,7%, а после 3 месяцев лечения – на 54,7% по сравнению с исходным уровнем (средний балл по ВАШ исходно – 10,21, через 1 месяц – 5,03, через 3 месяца – 4,62). Стоит отметить, что средняя оценка тяжести симптомов по ВАШ значимо снизилась через месяц лечения по сравнению с исходными данными (p<0,001), при этом средний общий балл по ВАШ через 1 и 3 месяца лечения статистически не различались (p=0,547). Это свидетельствует о том, что максимальный клинический эффект был достигнут к концу 1-го месяца при ежедневном использовании крема дозированного «Триофемин», а при снижении кратности введения до 3 раз в неделю в последующие 2 месяца эффективность не повышалась, но оставалась на том же уровне (рис. 1).
На точечной диаграмме (рис. 2) наглядно показано, что на визите скрининга подавляющее большинство женщин оценивало тяжесть проявлений ВВА от 8 до 15 баллов, а через 1 и 3 месяца лечения – от 0 до 6 баллов, что подтверждает значимую клиническую эффективность исследуемого продукта.
Регрессионный анализ влияния таких факторов, как возраст, длительность менопаузы, индекс массы тела, значение pH, состояние микробиоценоза влагалища на выраженность субъективных симптомов по ВАШ до начала лечения выявил, что тяжесть проявлений ВВА прямо коррелирует с уровнем pH, титром облигатно-анаэробной микрофлоры и обратно коррелирует с титром лактобактерий исходно.
Объективные признаки ГУМС/ВВА оценивались врачом на всех визитах с определением ИВЗ по G. Bachmann. Исходно показатели ИВЗ находились в диапазоне от 3 до 15 баллов; через 3 месяца применения крема «Триофемин» показатели ИВЗ у большинства пациенток значимо повысились до 15–23 баллов, причем практически половина участниц через 3 месяца наблюдения достигла нормальных значений ИВЗ (≥20), что свидетельствует об улучшении состояния слизистой оболочки вульвы и влагалища, ее эластичности и увлажненности (рис. 3).
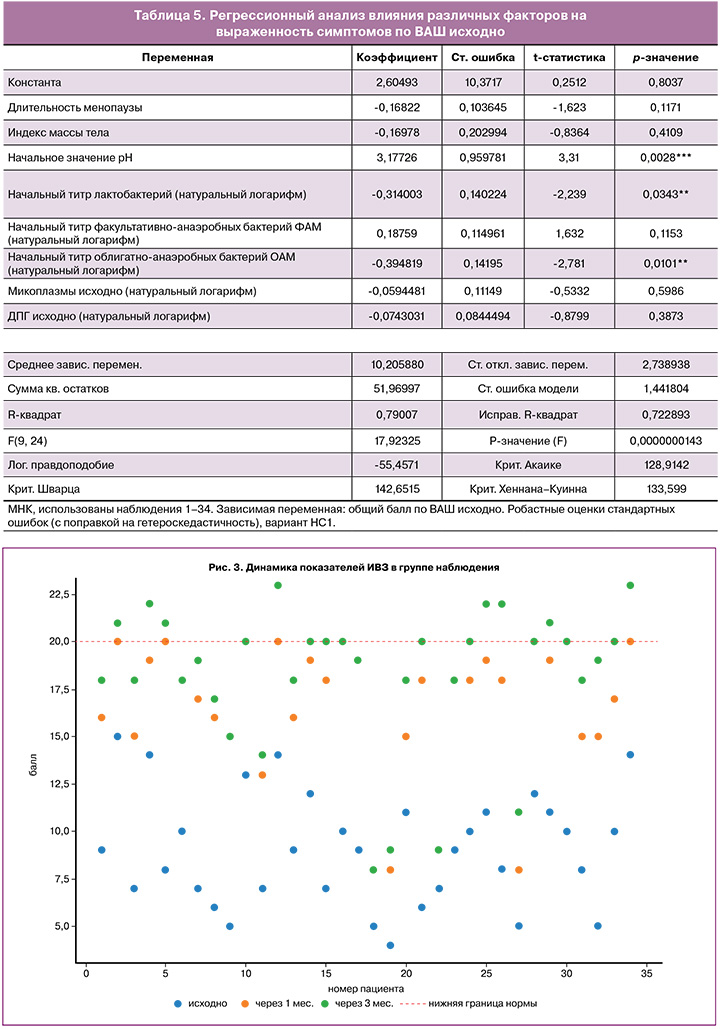
Средние значения ИВЗ в выборке статистически значимо повысились через месяц терапии по сравнению с исходным уровнем (p<0,001). Через 3 месяца лечения наблюдался дальнейший рост показателей ИВЗ, однако изменения в объективной оценке признаков ВВА к концу периода наблюдения по сравнению с 1-м месяцем терапии имели низкую статистическую значимость (p=0,082) (рис. 4).
Одним из объективных и достоверных признаков ВВА является повышение pH содержимого влагалища. Среднее значение pH через 3 месяца лечения снизилось на 9,28% по сравнению с исходным показателем, что демонстрирует статистически значимое изменение (pH исходно – 5,71, через 3 месяца терапии – 5,18, p<0,05) (рис. 5).
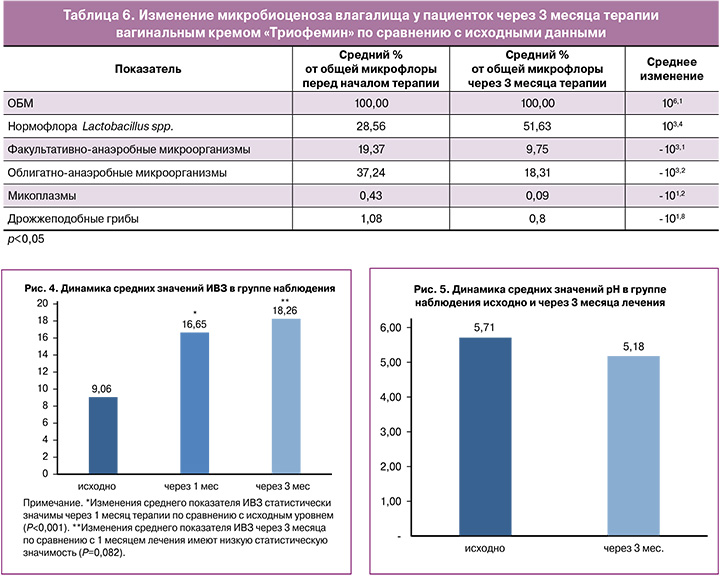
Оценка микробиоценоза влагалища методом ПЦР проводилась на визите скрининга и через 3 месяца терапии. До начала лечения у 9 (26,5%) пациенток лактобактерии (Lactobacillus spp.) отсутствовали (в абсолютных значениях –1000. копий/образец), у остальных женщин титр лактобактерий был снижен и колебался от 102,5 до 105,8 копий/образец. К концу периода наблюдения у всех 34/34 (100%) участниц определялась лактофлора в абсолютных значениях от 102,8 до 107,5 копий/образец. У 19/34 (55,9%) пациенток до начала терапии «Триофемином» преобладала облигатно-анаэробная микрофлора (Gardnerella vaginalis/Prevotella bivia/Porphyromonas spp., Eubacterium spp., Megasphaera spp./Veillonella spp./Dialister spp., Lachnobacterium spp./Clostridium, Mobiluncus spp./Corynebacterium, Peptostreptococcus spp.).
Для объективного восприятия данных был рассчитан средний % Lactobacillus spp. и представителей условно-патогенной микрофлоры от общей бактериальной массы (ОБМ) исходно и через 3 месяца терапии, а также определены средние изменения полученных значений (табл. 6).
К концу периода наблюдения отмечено статистически значимое увеличение количества Lactobacillus spp. (исходно средний % от ОБМ – 28,56, через 3 месяца терапии – 51,63, среднее изменение – 103,4), а также достоверное снижение факультативно-анаэробной (исходно средний % от ОБМ – 19,37%, через 3 месяцев лечения – 9,75%, среднее изменение – -103,1) и облигатно-анаэробной микрофлоры (исходно средний % от ОБМ – 37,24%, через 3 месяца терапии – 18,31%, среднее изменение – -103,2).
На 2-м и 3-м визитах пациентки оценивали удовлетворенность терапией кремом «Триофемин» от 0 до 10 баллов, где 0 баллов – отсутствие эффекта от терапии, 10 баллов – максимальный эффект, т.е. полное отсутствие беспокоящих симптомов ГУМС/ВВА. Среднее значение по шкале удовлетворенности лечением через 1 месяц составило 7,35, через 3 месяца – 7,59, т.е. согласно субъективной оценке участниц исследования эффект через 1 и 3 месяца терапии был одинаковым (рис. 6).
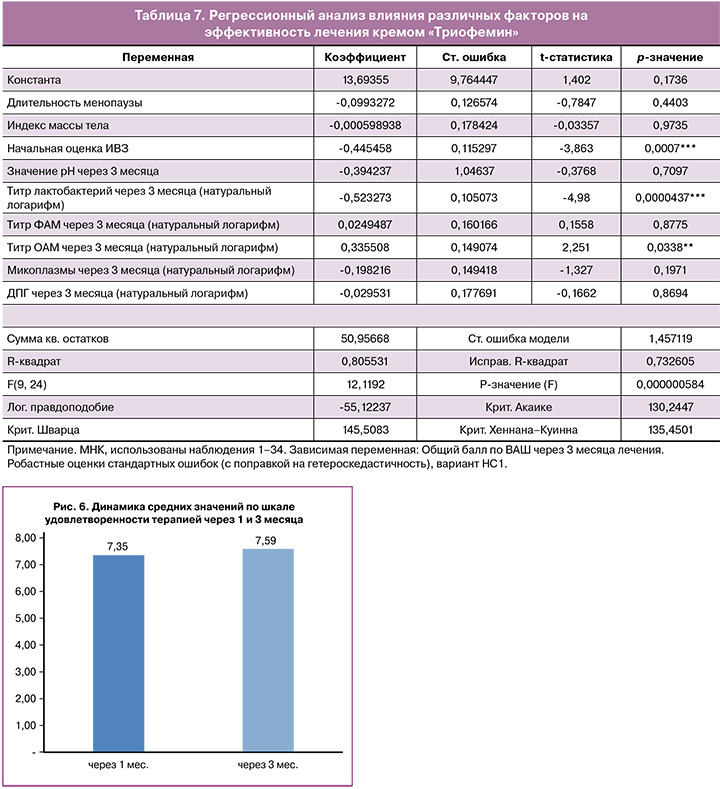
С помощью регрессионного анализа определены факторы, которые влияли на успех терапии кремом «Триофемин». Показана сильная корреляционная зависимость между эффективностью лечения и исходным уровнем ИВЗ, а также титром лактобактерий через 3 месяца наблюдения. Таким образом, чем меньше поражение слизистой влагалища на визите скрининга и чем выше титр лактобактерий через 3 месяца, тем больше был выражен клинический эффект (табл. 7).
НЯ наблюдались у 6/40 (15%) участниц в первые недели использования крема «Триофемин». 5 пациенток предъявляли жалобы на жжение во влагалище легкой или умеренной степени после введения крема. Только одна участница самостоятельно прекратила лечение из-за жжения и была исключена из исследования. Остальные 4 пациентки продолжали терапию и отметили, что данный симптом проходил в течение 10–14 дней без применения дополнительных лечебных средств. У одной пациентки наблюдалась местная аллергическая реакция в виде зуда и отека слизистой, терапия «Триофемином» отменена и участница также исключена из исследования.
Заключение
Таким образом, комбинированный крем дозированный «Триофемин» с гиалуроновой кислотой, фитокомплексом и лактобактериями эффективно редуцирует симптомы и объективные признаки ВВА, снижает рН влагалища и способствует нормализации локального микробиоценоза. «Триофемин» обладает хорошей переносимостью и имеет безопасный состав по критериям ВОЗ, что обеспечивает возможность его длительного применения.
Максимальный клинический эффект был достигнут к концу 1-го месяца при ежедневном использовании крема «Триофемин», а при снижении кратности введения до 3 раз в неделю в последующие 2 месяца эффективность не повышалась, но поддерживалась на том же уровне. Успех терапии «Триофемином» зависел от степени поражения слизистой влагалища исходно и титра лактобактерий через 3 месяца лечения.
Крем дозированный с гиалуроновой кислотой, фитокоплексом и лактобактериями «Триофемин» может быть рекомендован пациенткам с симптомами ГУМС в пери- и постменопаузе в качестве стартового средства для облегчения симптомов и дискомфорта, связанных с эстрогенодефицитом, в том числе у тех групп пациенток, которые имеют противопоказания или ограничения к применению локальных эстрогенов.



