Врастание плаценты является одной из наиболее тяжелых аномалий ее прикрепления, обусловленной избыточной инвазией ворсин в подлежащие тканевые структуры. Выделяют три морфологических варианта нарушения инвазии ворсин хориона: их приращение к миометрию – placenta accreta, прорастание мышечной оболочки – placenta increta, а при достижении ворсинами серозного слоя и/или соседних органов – placenta percreta. Аномалии прикрепления плаценты являются серьезной акушерской проблемой, сопровождающейся высоким риском массивной кровопотери, а также утратой репродуктивной функции [1]. По данным ВОЗ, в структуре причин материнской смертности кровотечения составляют от 19,9 до 36,2%, по данным FIGO – 27,1%, при этом непосредственная доля врастания плаценты составляет 7% [2].
В последние годы отмечается прогрессивное увеличение числа случаев врастания плаценты (от 1:30 000 до 1:533 родов) [3], что напрямую связано с увеличением частоты оперативных родоразрешений. В настоящее время ведущая роль в возникновении данной патологии отводится повреждению эндометрия, нарушению кровоснабжения и архитектоники стенки матки, что характерно для области рубца на матке после оперативных вмешательств. Кроме того, к подобным изменениям могут приводить высокий паритет родов, частый кюретаж матки, хронический эндометрит, синдром Ашермана. Известны случаи врастания плаценты у пациенток после перенесенной эмболизации маточных артерий (ЭМА) по поводу миомы матки [4]. С другой стороны, возможна неадекватная реакция трофобласта, протеолитическая активность которого определяется плацентарными специфическими белками, роль которых активно изучается с помощью определения их внеклеточных мРНК в крови: плацентарного лактогена (hPL), белка KISS-1, плацентоспецифического белка 1 (PLAC1), микроРНК-34а [5–7].
Врастание плаценты, по данным мировой литературы, является лидирующей причиной массивных акушерских кровотечений (3000–47 000 мл) [8]. Такой объем кровопотери обусловлен анатомическими особенностями кровоснабжения беременной матки: близость магистральных сосудов, богатая сеть коллатералей и анастомозов, возникновение артериовенозных мальформаций вследствие предыдущих оперативных вмешательств, неоангиогенез в области placenta increta, а также частым сочетанием с предлежанием плаценты. Практически во всех странах мира, в том числе в Российской Федерации, массивная кровопотеря становится показанием к гистерэктомии (ГЭ). На сегодняшний день в развитых странах врастание плаценты является ведущей причиной ГЭ при родоразрешении и составляет до 47%.
Избежать ГЭ и сохранить репродуктивную функцию пациенток с врастанием плаценты – важная задача современного акушерства.
Весомый вклад в успешное лечение врастания плаценты вносит своевременная диагностика этой патологии. Достаточно чувствительным методом является ультразвуковое исследование (УЗИ) с допплерометрией. Частота, с которой обнаруживается патология прикрепления плаценты при выполнении УЗИ, по данным литературы, составляет от 33 до 100%, при использовании цветового и энергетического допплерометрического исследования чувствительность и специфичность антенатальной диагностики повышается, и ее частота варьирует от 82,4 до 100% и от 92 до 96,8% соответственно [9, 10].
 Ультразвуковые маркеры врастания плаценты включают в себя потерю гипоэхогенной ретроплацентарной зоны миометрия, наличие плацентарных лакун, нарушение границы задней стенки мочевого пузыря и матки, и, в случае placenta percreta, определяются локальные экзофитные массы [11]. При допплерометрическом исследовании регистрируется картина турбулентного кровотока, распространяющегося от плаценты в окружающие ткани, сосуды, пересекающие границу плаценты и мочевого пузыря, плацентарный лакунарный поток, гиперваскуляризация границ плаценты и субплацентарная васкуляризация.
Ультразвуковые маркеры врастания плаценты включают в себя потерю гипоэхогенной ретроплацентарной зоны миометрия, наличие плацентарных лакун, нарушение границы задней стенки мочевого пузыря и матки, и, в случае placenta percreta, определяются локальные экзофитные массы [11]. При допплерометрическом исследовании регистрируется картина турбулентного кровотока, распространяющегося от плаценты в окружающие ткани, сосуды, пересекающие границу плаценты и мочевого пузыря, плацентарный лакунарный поток, гиперваскуляризация границ плаценты и субплацентарная васкуляризация.
Магнитно-резонансная томография (МРТ) более информативна, когда плацента плохо визуализируется при УЗИ, например, при ее расположении по задней стенке матки. Чувствительность МРТ составляет от 80 до 85%, специфичность от 65 до 100%. Заподозрить врастание плаценты позволяют следующие изменения при МРТ: гипоинтенсивные внутриплацентарные участки в виде округлых или линейных структур, выбухание стенки матки в виде ограниченного выпячивания стенки матки, гетерогенность сигнала от плацентарной ткани, патологическая извитость плацентарных сосудов, нечеткость границы миометрия в виде его отсутствия на ограниченных участках, деформация контура мочевого пузыря [12, 13].
В современном мире следует отдавать предпочтение оперативному родоразрешению с одномоментной метропластикой у пациенток с патологией прикрепления плаценты. Разработаны различные методики оперативного вмешательства, позволяющие снизить объем кровопотери и избежать ГЭ. Наиболее безопасно проведение оперативного вмешательства при сроках гестации 32–36 недель. Проведение донного или корпорального разреза на матке позволяет более бережно извлечь плод из полости матки с меньшим объемом кровопотери и меньшей травматизацией области нижнего сегмента матки и мочевого пузыря. Применение современных гемостатических методов (временная окклюзия магистральных сосудов с использованием турникетов [14], ЭМА, баллонная тампонада общих подвздошных артерий, баллонная окклюзия внутренних подвздошных артерий, баллонная окклюзия аорты [15–19]) создает временную ишемию тканей, что значительно снижает интраоперационную кровопотерю, обеспечивает хорошую визуализацию тканей и условия для выполнения реконструктивной операции на матке. Немалый вклад вносит применение технологии Cell-Saver, позволяя снизить частоту гемотрансфузии донорских эритроцитов.
Успешное выполнение органосохраняющей операции у беременной с врастанием плаценты демонстрирует следующий клинический случай.
 Клиническое наблюдение
Клиническое наблюдение
Пациентка Б., 43 лет, поступила в клинику акушерства и гинекологии ФГБОУ ВО «Первый Санкт-Петербургский государственный медицинский университет им. акад. И.П. Павлова» при сроке беременности 35–36 недель.
Диагноз: основной – неполное предлежание плаценты. Placenta increta. Умеренная преэклампсия (ПЭ). Осложнение – хроническая плацентарная недостаточность. Нарушение гемодинамики в системе мать–плацента–плод I степени. Синдром задержки внутриутробного роста плода. Сопутствующий: рубец на матке после операций кесарева сечения. Отягощенный акушерско-гинекологический анамнез (2 неразвивающиеся беременности в 2002, 2014 гг., кесарево сечение (КС) 2002 и 2015 гг.). Носитель генов, ассоциированных с патологией системы гемостаза (ген интегрина a2 GPIa, ген фибриногена FGB, PLAT, MTHFR, MTRR).
В анамнезе у пациентки 5 беременностей: 2 неразвивающиеся беременности при сроке 8–9 недель с последующим кюретажем стенок полости матки в 2010 г. и 2014 г., 2 операции КС (в 2002 г. плановое КС в связи с ножным предлежанием плода, 3200 г/50 см, в 2015 г. экстренное КС в родах в связи с острой гипоксией плода, 3200 г/50 см), а также срочные роды с рубцом на матке per vias naturalis в 2012 г., 2650 г/49 см, послеродовый период осложнился кровотечением.
Данная беременность протекала на фоне симптомов умеренной ПЭ, дебют подъема артериального давления (АД) наблюдался при сроке гестации 30 недель. Максимальные цифры АД за время беременности – до 165/110 мм рт. ст., суточная протеинурия 0,7 г/л, в разовой порции мочи 0,3 г/л. Получала магнезиальную, гипотензивную терапию.
Впервые врастание плаценты заподозрено при сроке гестации 34 недели при проведении ультразвукового скрининга (аппарат Voluson Е8 General Electric), по данным которого плацента располагалась по передней стенке матки в области нижнего сегмента, толщина плаценты в нижнем сегменте до 75 мм с грыжевидным выпячиванием в область задней стенки мочевого пузыря. Миометрий в нижнем сегменте тонкий, линейный, не подлежит измерению, имеет грыжевидное выбухание на всем протяжении в область задней стенки мочевого пузыря.
Для уточнения диагноза была выполнена МРТ (AsteionMulti 4 Toshiba), по данным которой (рис. 1) плацента представлена единым диском, располагается по передней стенке матки, доходит до края внутреннего зева. В нижней трети тела матки и в области перешейка миометрий истончен, стенка матки выпячивается книзу, плацентарная ткань утолщена до 79 мм, неоднородна, в области рубца толщина плаценты локально 46–48 мм, миометрий истончен, оценить толщину миометрия в области послеоперационного рубца не представляется возможным, неоднородность структуры плаценты, с расширением и извитостью варикозно расширенных сосудов, с локальной неровностью, нечеткостью границы между миометрием и плацентой. Нельзя исключить участок инвазии. Мочевой пузырь малого наполнения, верхняя стенка вогнута, компримирована маткой.
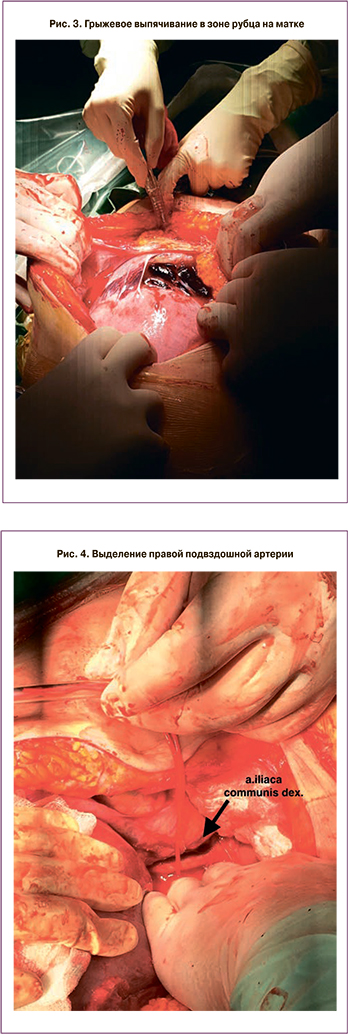
 При сроке гестации 37 недель запланировано и выполнено оперативное родоразрешение. В ходе операции обнаружено: по передней стенке матки, в области нижнего сегмента определяется грыжевое выпячивание размерами 15,0×8,0×6,0 см (рис. 2–3).
При сроке гестации 37 недель запланировано и выполнено оперативное родоразрешение. В ходе операции обнаружено: по передней стенке матки, в области нижнего сегмента определяется грыжевое выпячивание размерами 15,0×8,0×6,0 см (рис. 2–3).
Выполнено корпоральное КС. За ножки извлечен мальчик массой 2220 г, длиной 46 см. Оценка по шкале Апгар составила 8/8 баллов. На пуповину наложена лигатура и погружена в матку. Рана матки ушита однорядным непрерывным швом (Викрил 1,0).
С целью профилактики тромбоэмболических осложнений внутривенно струйно введено 2500 Ед гепарина. Произведено наложение турникетов на общие подвздошные артерии (рис. 4). При контроле пульсоксиметрии на нижних конечностях зафиксирован удовлетворительный блок кровотока (Sat 0%).
 Вскрыта брюшина в области пузырно-маточной складки, мочевой пузырь низведен, обнажен нижний сегмент матки с участком врастания. Плацента по передней стенке, край ее доходит до области внутреннего зева, не перекрывая его. Произведено иссечение участка врастания плаценты размерами 15,0×8,0×6,0 см в пределах интактной ткани миометрия по передней стенке матки. Целостность стенки матки восстановлена двухрядным непрерывным мышечно-мышечным (Викрил 1.0).
Вскрыта брюшина в области пузырно-маточной складки, мочевой пузырь низведен, обнажен нижний сегмент матки с участком врастания. Плацента по передней стенке, край ее доходит до области внутреннего зева, не перекрывая его. Произведено иссечение участка врастания плаценты размерами 15,0×8,0×6,0 см в пределах интактной ткани миометрия по передней стенке матки. Целостность стенки матки восстановлена двухрядным непрерывным мышечно-мышечным (Викрил 1.0).
Турникеты с подвздошных сосудов сняты на 20-й минуте, кровоснабжение восстановлено в полном объеме (Sat 98%).
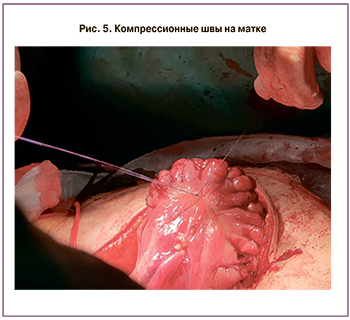
Выполнена комбинированная фармако-механическая профилактика гипотонического кровотечения: внутривенно струйно введен 1,0 мл карбетоцина, наложены компрессионные швы на матку по B-Lynch (рис. 5). Гемостаз в области раны матки удовлетворительный.
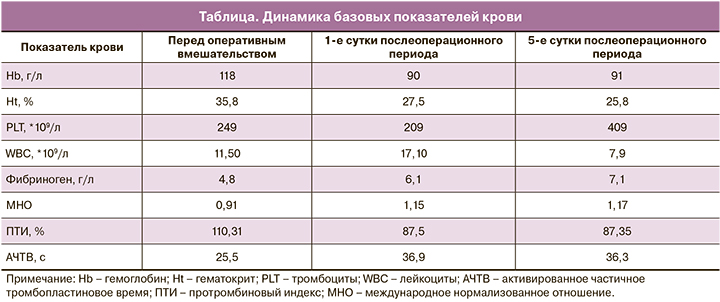
Продолжительность оперативного вмешательства составила 105 минут. Общая кровопотеря составила 1500 мл. Выполнена реинфузия 552 мл отмытых эритроцитов (Ht 76,5 %) с применением аппарата Cell Saver 5. Послеоперационный период протекал без осложнений (таблица).
По данным контрольного УЗИ на 2-е сутки послеоперационного периода размеры матки составили в длину – 128 мм; толщину – 65 мм; ширину – 120 мм. Полость матки расширена: в верхней трети до 6 мм, в средней трети – до 5 мм, в нижней трети – до 10 мм, содержит эхоплотные включения размерами до 2–3 мм. Контуры полости матки визуализируются отчетливо. Стенки полости матки гладкие.
Пациентка выписана на 6-е сутки послеоперационного периода в удовлетворительном состоянии.
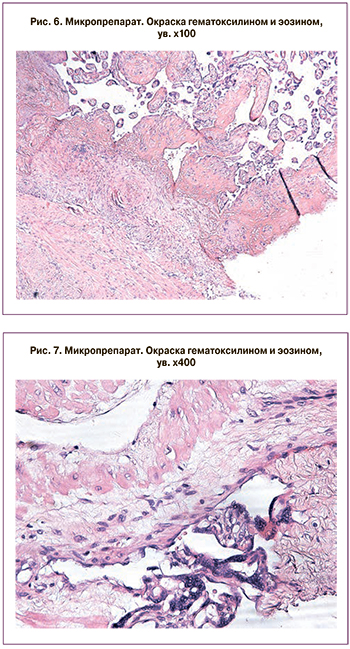
Гистологическое исследование препарата представлено на рис. 6–8.
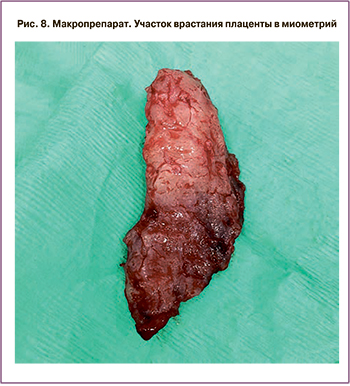 В материале плацента с фрагментом миометрия. Плацента зрелая, соответствует сроку гестации с умеренно выраженными признаками физиологического старения. Отмечается преимущественное малокровие межворсинчатого пространства с немногочисленными фокусами коллапса ворсин, неравномерное кровенаполнение ворсин всех генераций. Оболочки отечные с инволютивно-дистрофическими изменениями. Пуповина содержит три сосуда, обычного гистологического строения, отмечается минимальный отек вартонова студня. Плацента плотно приращена к миометрию, с инвазией ворсин хориона во внутренний циркулярный мышечный слой. Миометрий с гипертрофией мышечных волокон.
В материале плацента с фрагментом миометрия. Плацента зрелая, соответствует сроку гестации с умеренно выраженными признаками физиологического старения. Отмечается преимущественное малокровие межворсинчатого пространства с немногочисленными фокусами коллапса ворсин, неравномерное кровенаполнение ворсин всех генераций. Оболочки отечные с инволютивно-дистрофическими изменениями. Пуповина содержит три сосуда, обычного гистологического строения, отмечается минимальный отек вартонова студня. Плацента плотно приращена к миометрию, с инвазией ворсин хориона во внутренний циркулярный мышечный слой. Миометрий с гипертрофией мышечных волокон.
Заключение
Основными методами диагностики врастания плаценты являются УЗИ с допплерометрической оценкой кровотока и магнитно-резонансное исследование. Данную патологию необходимо выявлять на догоспитальном этапе. Это позволит направлять пациенток в соответствующий многопрофильный стационар, где будет реализован весь объем современных технологий и обеспечен мультидисциплинарный подход к их ведению с участием акушера-гинеколога, анестезиолога, трансфузиолога и, при необходимости, сосудистого хирурга, уролога.
Корпоральное (донное) КС с разрезом на матке вне плацентарной площадки и временная окклюзия подвздошных сосудов значимо уменьшают объем кровопотери, длительность оперативного вмешательства и анестезиологического пособия, а также создают условия для выполнения метропластики и сохранения репродуктивной функции у пациентки.



