Системы поддержки принятия врачебных решений (англ. Clinical Decision Support System, CDSS) – это программные продукты, которые объединяют и структурируют медицинские знания и, благодаря этому, позволяют улучшать качество оказания медицинской помощи. Активное развитие компьютеризированных систем, возможности интеграции и обработки данных о пациенте с последующим их параллельным анализом с течением того или иного заболевания создали объективные предпосылки для разработки новых подходов к диагностике и терапии в рамках создания «искусственного интеллекта» – СППР.
Область применения СППР включает задачи диагностики, контроля состояния пациента, подбора терапии, контроля назначения и приема препаратов и многие другие, которые реализуются при помощи веб-приложений либо приложений для мобильных устройств или стационарных компьютеров, и может, в том числе, обеспечивать более эффективное взаимодействие врача и пациента.
К преимуществам СППР следует отнести:
- возможность оценки совместимости и безопасности при назначении лекарственной терапии;
- выбор правильного вектора диагностического поиска;
- возможность установки «фильтров» для получения только таргетной информации.
Отметим, что точность предлагаемых системой решений зависит от содержания текущих данных и постоянного их обновления в соответствии с меняющимися клиническими практиками.
По мнению авторов обзора, правильно спроектированная СППР должна быть самообучаемой. По мере анализа корректности принятых решений и выбора наиболее рационального пути алгоритмы принятия решений системы совершенствуются, становясь «живой системой».
К преимуществам СППР относится и возможность обратной связи пациента с врачом. Дистанционный мониторинг позволяет своевременно менять врачебную тактику и максимально избегать тяжелых осложнений. В акушерстве проблемы, связанные с ведением пациенток с отягощенным соматическим анамнезом и осложненным течением беременности, также могут быть решены с помощью СППР. Алгоритмы ведения таких пациенток внедряются в программное обеспечение, где врачам дается информация о необходимости назначения клинико-лабораторного дообследования, консультаций профильных специалистов. Лекарственный мониторинг во время беременности также имеет свои особенности с точки зрения безопасности и эффективности применения в различные сроки беременности.
Вместе с тем внедрение СППР в клиническую практику сопряжено с рядом трудностей: финансовыми затратами, необходимостью обучения персонала, сложностью интеграции с другими компьютерными системами (например, ЭМК – электронной медицинской картой и МИС – медицинской информационной системой, используемой в медицинской организации). В Российской Федерации СППР в настоящее время не распространены, тогда как в некоторых странах Европы и в США внедрение таких систем в работу медицинских учреждений уже активно началось [1–7].
Стратегия и результаты поиска
Поиск статей, опубликованных в 2008–2019 гг., был проведен в базе данных Scopus по названию, тексту и ключевым словам с использованием следующих запросов: clinical decision support system AND medicine (1101 статья), decision AND support AND system AND obstetrics (206 статей), clinical decision support system AND obstetrics (35 статей) (рисунок).
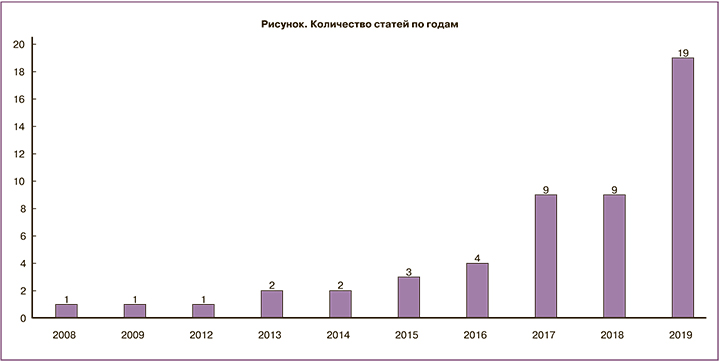
Из 1342 уникальных статей были отобраны 23, вошедшие в данный обзор, так как бо́льшая часть содержала термины поиска только в ключевых словах и содержательно не относилась к медицине, в частности, к акушерству/смежным специальностям (гинекология, перинатология, онкология, хирургия, кардиология, реаниматология). Для более полной оценки развития исследуемого направления рассматривались не только полноценные СППР, но и отдельные компоненты: алгоритмы, визуализация, взаимодействие с пациентом, онтология.
Так как работы разнородны по применяемым методам, для унификации описания полученных авторами результатов в качестве меры будет приводиться точность как доля верно классифицированных случаев к общему количеству случаев. Данная мера приводится в большинстве статей и применима в случае как бинарной, так и многоклассовой переменной отклика.
Обзор используемых алгоритмов принятия решений
В основе СППР могут быть использованы различные методы работы с информацией, математического моделирования и алгоритмов принятия решений. Все методы можно разделить по следующим критериям: интерпретируемость (доступность, почему система предлагает такое решение), гибкость при необходимости внесения изменений в систему медицинских знаний, доступность (возможность интеграции с МИС или ЭМК), полнота охвата патологий/методов исследования (насколько система будет полезна конечному пользователю – врачу) и возможность преобразования или обобщения информации.
Алгоритмы принятия решений, основанные на соответствии условиям
Наиболее часто встречаются системы, принимающие решения на основе существующих клинических рекомендаций и протоколов ведения пациентов.
Это один из базовых алгоритмов, при использовании которого процесс принятия решений становится автоматизированным, и врачу не нужно тратить время на поиск и чтение информации в рекомендациях. Следует отметить, что такие системы обладают высокой интерпретируемостью, так как возможно непосредственно указать источник информации, ограниченной гибкостью (из-за зависимости от сторонних источников информации), доступностью, полнотой. Но данный тип СППР не способен генерировать новое знание путем обобщения информации, и этот процесс происходит вне системы, неавтоматизированно, что требует вложения значительных ресурсов в постоянное обновление базы знаний. Такие системы могут быть включены в состав МИС в акушерстве [1, 2] и в других областях медицины [3–5, 8].
Графовые методы [6, 9–19]
Данные методы включают в себя модели принятия решений и организации знаний, основанные на графах – совокупности узлов и соединяющих их ребер. Использование графов целесообразно в тех разделах знания, где предполагается либо иерархическая структура, либо нелинейное взаимодействие между фрагментами знаний. Так, для иерархической структуры характерны графы типа «дерево», когда из родительского узла выбирается та или иная ветвь, которая либо затем разветвляется, либо система находит решение. Такой способ представления знаний широко распространен в медицине, и большинство алгоритмов, составленных для упрощения принятия решений человеком, является деревом принятия решений. Для сложных структур знаний используются графы, отражающие взаимодействие между элементами знаний – корреляцию, причинно-следственную связь либо иные отношения и позволяющие, переходя из одного узла в другой, давать более сложные решения. Примерами таких методов являются байесовские сети доверия, нечеткие когнитивные карты, марковские сети. Методы, основанные на графах, как правило, легко интерпретируемые, умеренно гибкие, умеренно доступные и позволяют составлять и отображать более сложные решения.
Методы, основанные на искусственных нейронных сетях [9, 17, 20–24]
Данные методы применяются, как правило, в тех областях медицины, где генерируется большое количество информации, обычно визуальной. Это методы лучевой диагностики, патологоанатомические изображения, сложные биоэлектрические сигналы. Искусственные нейронные сети позволяют проводить свертку (компактное и обобщенное отображение больших объемов входных данных) для задач по распознаванию образов и автоматизированно находить связи между различными фрагментами знаний.
Однако нейронные сети не интерпретируемы, недостаточно гибкие, сложны в интеграции, требуют большого объема данных для обучения сети. Они отлично выполняют функцию обобщения либо преобразования сложно структурированных данных.
Примеры систем поддержки принятия врачебных решений
Ниже приводятся примеры различных моделей СППР в акушерстве, которые могут как решать одну [25, 26] или несколько задач в области акушерства и гинекологии, так и иметь более универсальный характер и распространяться, в том числе, на смежные дисциплины.
Moreira M.W.L. et al. [16] определяют риски и проводят диагностику гипертензивных расстройств у беременных с помощью алгоритма NBTree (Naive Bayes Tree) [25]. Полученные результаты показывают достаточно высокую ценность использования СППР, но ограниченную несколькими патологиями. В своей работе D’Souza R. et al. [13] подбирают оптимальный антикоагулянт беременным с механическими клапанами сердца. Авторы указывают, что при оценке рисков учитывают состояние и матери, и плода одновременно. Douali N. et al. [18] анализируют вероятность развития гестационного сахарного диабета. Lam J. et al. [26] разработана база знаний для беременности высокого риска. Использовалась обратная связь от клиницистов и проведено анкетирование среди врачей и акушерок для оценки базы знаний по шести критериям: понятность, полнота, правильность, гибкость, простота и целостность. Система оказалась полезной и удобной в практике акушерок, но недостаточно эффективной для врачей. Авторы не указывают на возможные причины полученных результатов.
Роды
Bourgani E. et al. [17] используют СППР для объективизации показаний для проведения кесарева сечения. Система определяет угрожающие состояния для матери и плода. Авторы использовали модель, учитывающую изменение параметров во времени. Точность полученного решения в статье не указана.
Другие системы, поддерживающие принятие врачебных решений при конкретных ситуациях в родах [1, 21, 24, 27–29], также не имеют потенции к объединению акушерских ситуаций и самообучению.
Оценка состояния плода
Akbulut A. et al. [6] прогнозируют вероятность развития врожденных аномалий развития у плода. Авторы обобщили 9 бинарных классификаторов и создали модель, основанную на совокупности большого ансамбля деревьев решений (Decision forest). Точность, достигнутая на обучающих данных, составила 89,5%, при валидации – 87,5%.
Заслуживает внимания использование данных кардиотокографии для оценки и классификации различных состояний плода [20, 30, 31].
Узкоспециализированные системы поддержки принятия врачебных решений
Van Calster B. et al. [32] используют СППР для диагностики внематочной беременности. В основе системы лежат модели логистической регрессии, достигнутая точность составила 92,4% на выборке 856 человек. Van Belle V.M.C.A. et al. [7] с помощью математической модели решают задачу предикции степени злокачественности опухолей яичника, а также прогнозируют вероятность выкидыша в I триместре беременности. Исследование выполнено на больших выборках (3511 и 1435 пациентов), точность метода составила 96% и 92% соответственно.
Системы общего назначения
Seitinger A. et al. [2] спроектировали систему, результатом которой являются сообщения-напоминания для конкретного пациента в виде списка дел для каждой фазы: беременность, роды, послеродовый период. Система была основана на клинических рекомендациях. Horner V. et al. [33] провели оценку результатов внедрения СППР в Южной Африке. На основе информации о дородовых визитах пациенток программа определяет перинатальные риски. Несмотря на слабую компьютерную грамотность, введение СППР позволило снизить частоту ошибок ввода данных, которые могут привести к принятию неверных клинических решений. Одной из сильных сторон программы является то, что ее данные предназначены для медсестер и не требуют участия высококвалифицированных специалистов.
Gorthi A. et al. [15] применяют СППР для определения беременности высокого риска. Авторы построили бинарное дерево с помощью алгоритма CART (Classification and Regression Tree). Точность оценки составила 82,5%.
Merriel A. et al. [34] провели исследование внедрения СППР в акушерском отделении больницы в Зимбабве. Система дает оценку вероятности возникновения осложнений во время родов и в послеродовом периоде. На успешность исследования в большей степени повлияла степень участия команды специалистов в адаптации системы и осуществлении плана реализации. Для проверки системы в условиях нехватки времени и ресурсов требуются дальнейшие исследования.
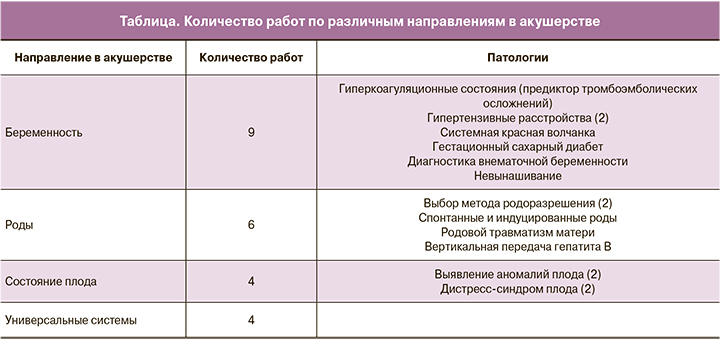
В настоящее время большинство опубликованных работ, описывающих использование СППР в акушерстве, направлено на решение какой-либо узкоспециализированной задачи (таблица); используемые методы не предполагают возможности масштабирования на большие акушерские синдромы, что не соответствует глобальным запросам клинических специалистов.
Системы поддержки принятия врачебных решений в России
При поиске публикаций в изданиях, рецензируемых Scopus, не было обнаружено отечественных статей по описанию или внедрению СППР в акушерстве. В смежных областях было обнаружено малое количество таких исследований. Bolgova K. et al. [35] тестировали СППР по сердечно-сосудистым нарушениям, интегрированную в электронную медицинскую карту, и отметили снижение количества ошибок пользователей в данных. Клейменова Е.Б. и соавт. [36] исследовали эффективность СППР на основе клинических рекомендаций в профилактике внутригоспитальных венозных тромбоэмболических осложнений. Авторы отмечают снижение частоты дефектов фармакологической профилактики и повышение адекватности применения антикоагулянтов. Abuhay T. et al. [37] предлагают СППР на основе мониторинга состояния пациентов с острым коронарным синдромом.
Заключение
Рассмотренные работы описывают системы, алгоритмы и результаты, полученные, как правило, на небольших выборках. Основные препятствия в продвижении СППР возникают на этапе их внедрения и валидации в клинической практике; многие модели так и не доходят до финального этапа. Также у врачей могут возникать объективные и субъективные трудности при использовании СППР. Отметим, что многие из клинических рекомендаций и протоколов – это стандартизованный подход, основанный на анализе «идеального» пациента с точки зрения построения диагноза. СППР индивидуализируют подход, переходя к персонализированной медицине, учитывая особенности конкретного пациента, что делает разработку и внедрение этой системы неотъемлемой частью современной медицины.



