Несмотря на обилие контрацептивных средств, проблема контрацепции до сих пор не теряет своей актуальности. Согласно официальным статистическим данным в 2015 г. в России частота абортов на 1 тыс. женщин фертильного возраста составила 20,9 [1, 2]. По данным различных исследований подавляющее большинство женщин избегающих гормональной контрацепции опасаются побочных эффектов, увеличения рисков для здоровья [3]. При этом немногие женщины знают о лечебно-профилактических эффектах комбинированных оральных контрацептивов (КОК). Помимо надежной профилактики беременности, при длительном использовании КОК снижают риск рака эндометрия [4], рака яичников [5], рака ободочной кишки [6], а также комбинированных оральных контрацептивов (КОК) с антиандрогенным эффектом могут успешно использоваться для лечения андроген-зависимых дермопатий (гирсутизма, акне, алопеции) [7]. К сожалению, страхи, связанные с гормональными контрацептивами, распространены не только среди пациенток, но и среди врачей. Для повышения приверженности врачей к гормональной контрацепции необходимо проведение большего числа исследований, посвященных изучению эффективности и безопасности КОК, а также оценивающих их возможные лечебные эффекты, а для повышения приверженности пациенток требуется грамотное консультирование по гормональной контрацепции врачами.
В настоящей публикации приводятся данные изучения лечебных свойств КОК содержащего этинилэстрадиол (ЭЭ) и хлормадинона ацетат (ХМА) (белара, Гедеон Рихтер, Венгрия), полученные в рамках фармако-эпидемиологического исследования среди женщин, представляющих репрезентативную типичную популяцию принимающую КОК в Российской Федерации.
Материал и методы исследования
Дизайн исследования: многоцентровое открытое наблюдательное исследование в 20 центрах из 13 городов России (Москва, Пермь, Ставрополь, Санкт-Петербург, Краснодар, Казань, Екатеринбург, Верхняя Пышма, Волгоград, Самара, Томск, Воронеж, Нижний Новгород). В исследование была включена 161 пациентка, нуждающаяся в контрацепции, в репродуктивном возрасте от 18 до 37 лет и с подписанным информированным согласием. В исследование не включались женщины имеющие противопоказания к приему КОК или имеющие состояния при которых КОК следует использовать с осторожностью (согласно инструкции к препарату).
 С целью контрацепции пациенткам был назначен КОК представляющий комбинацию ЭЭ с ХМА в циклическом режиме 21/7. Все женщины использовали данный препарат впервые. Минимум за 3 месяца до приема препарата не использовали какие-либо другие гормональные препараты. За время исследования было проведено 3 визита: на этапе включения в исследование (визит 1) проводился сбор жалоб, оценка соматического, гинекологического и семейного анамнеза, гинекологический осмотр, ультразвуковое исследование (УЗИ) органов малого таза, измерение индекса массы тела (ИМТ) по формуле Brey, ИМТ=масса тела (кг/рост, м)2, окружности талии (ОТ), окружности бедер (ОБ), измерение артериального давления (АД), субъективная и объективная оценка состояния кожи (жирность, наличие угревой сыпи), анализ крови на Д-димер, АЧТВ, фибриноген, протромбин. Также проводилась оценка эмоционального состояния пациенток с помощью специального опросника САН, предназначенного для оперативной оценки самочувствия, активности и настроения (по первым буквам этих функциональных состояний и назван опросник). Пациенток просили оценить свое самочувствие по шкале, которая состоит из индексов (3 2 1 0 1 2 3) и расположена между тридцатью парами слов противоположного значения, отражающих подвижность, скорость и темп протекания функций (активность), силу, здоровье, утомление (самочувствие), а также характеристики эмоционального состояния (настроение). Для определения средних контрольных значений был проведен опрос выборки студентов из Москвы, который показал, что самочувствие здорового человека в среднем оценивается на 5,4 балла, активность – на 5 баллов, а настроение – 5,1 балла [8]. Через 3 месяца приема препарата (визит 2) и через 6 месяцев после приема препарата (визит 3) повторно проводились сбор жалоб, УЗИ органов малого таза, измерение ИМТ, ОТ, ОБ, АД, оценка состояния кожи (жирность, наличие угревой сыпи), оценка комплаентности, эффективности, побочных эффектов.
С целью контрацепции пациенткам был назначен КОК представляющий комбинацию ЭЭ с ХМА в циклическом режиме 21/7. Все женщины использовали данный препарат впервые. Минимум за 3 месяца до приема препарата не использовали какие-либо другие гормональные препараты. За время исследования было проведено 3 визита: на этапе включения в исследование (визит 1) проводился сбор жалоб, оценка соматического, гинекологического и семейного анамнеза, гинекологический осмотр, ультразвуковое исследование (УЗИ) органов малого таза, измерение индекса массы тела (ИМТ) по формуле Brey, ИМТ=масса тела (кг/рост, м)2, окружности талии (ОТ), окружности бедер (ОБ), измерение артериального давления (АД), субъективная и объективная оценка состояния кожи (жирность, наличие угревой сыпи), анализ крови на Д-димер, АЧТВ, фибриноген, протромбин. Также проводилась оценка эмоционального состояния пациенток с помощью специального опросника САН, предназначенного для оперативной оценки самочувствия, активности и настроения (по первым буквам этих функциональных состояний и назван опросник). Пациенток просили оценить свое самочувствие по шкале, которая состоит из индексов (3 2 1 0 1 2 3) и расположена между тридцатью парами слов противоположного значения, отражающих подвижность, скорость и темп протекания функций (активность), силу, здоровье, утомление (самочувствие), а также характеристики эмоционального состояния (настроение). Для определения средних контрольных значений был проведен опрос выборки студентов из Москвы, который показал, что самочувствие здорового человека в среднем оценивается на 5,4 балла, активность – на 5 баллов, а настроение – 5,1 балла [8]. Через 3 месяца приема препарата (визит 2) и через 6 месяцев после приема препарата (визит 3) повторно проводились сбор жалоб, УЗИ органов малого таза, измерение ИМТ, ОТ, ОБ, АД, оценка состояния кожи (жирность, наличие угревой сыпи), оценка комплаентности, эффективности, побочных эффектов.
Статистическая обработка проведена с помощью программы Statisica v.6. Данные проверяли на соответствие нормальному закону распределения с помощью тестов Kolmogorov-Smirnov&Lillefors. Cравнение проводили с помощью дисперсионного анализа ANOVA, использовали Т-тесты Стьюдента для зависимых и независимых переменных; использовали χ2 и M-L-χ2 для работы с таблицами сопряженных значений, графические возможности Excel. В исследовании уровень значимости различий был принят для р<0,05.
Результаты исследования и обсуждение
Средний возраст женщин составил 29,3±4,1 года. Большинство пациенток находилось в возрастной группе 25–35 лет.
Изучение соматического и акушерско-гинекологического анамнеза также выявило, что лишь 94 (58,4%) женщин были практически здоровы (I группа), у остальных 67 пациенток (41,6%, II группа) присутствовали те или иные гинекологические заболевания (синдром поликистозных яичников, дисфункция яичников репродуктивного периода, аденомиоз, наружный генитальный эндометриоз, миома матки малых размеров, функциональные кисты яичников, синдром предменструального напряжения).

Средний возраст на момент первой менструации у участниц исследования составил 12,8±1,18 года. Длительность менструации равнялась в среднем 5,2±1,1 дня. Менструальный цикл был регулярный у большинства пациенток, межменструальный период составлял 29,6±5,5 дня. Статистических различий по возрасту начала менструации между группами выявлено не было, но длительность менструации была больше в группе II.
Во II группе отмечался статистически значимо более длинный межменструальный период: 30,9±7,5 дня в группе II и 28,6±3,1 дня в I группе, (p<0,05).
У большинства пациенток обеих групп менструация была умеренной (74,5%), обильная менструация отмечалась у 26,6% пациенток I группы и у 13,4% пациенток II группы, скудная менструация наблюдалась редко (5,3% и 4,5% соответственно).
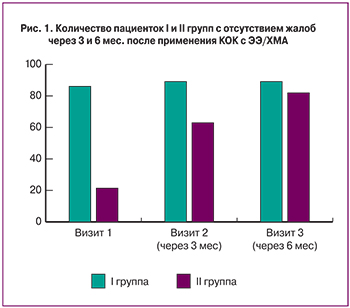
До начала приема ЭЭ/ХМА большинство пациенток из I группы не предъявляли никаких жалоб, 1 пациентка (1%) отмечала боли в молочных железах в предменструальном периоде и еще у одной (1%) были болезненные менструации. Во II группе лишь 14 женщин (20,9%) не предъявляли никаких жалоб, остальные пациентки отмечали болезненные менструации – 17 пациенток (25,4%), нерегулярные менструации – 12 (17,9%), обильные менструации – 2 (3%), мажущие менструальные выделения – 4 (5,9%), боли в молочных железах в предменструальном периоде – 2 (3%), а также 16 пациенток жаловались на акне (23,9%). Через 3 мес приема ЭЭ/ХМА количество жалоб во II группе снизилось на 42% и еще на 18,9% через 6 мес. Таким образом, 55 (82,1%) пациенток II группы не предъявляли никаких жалоб через полгода приема ЭЭ/ХМА (p<0,05). В группе практически здоровых пациенток количество жалоб также уменьшилось, однако различия носили незначимый характер, так как исходное количество жалоб было небольшим (рис. 1).
Наиболее выраженные изменения касались характера менструаций. Так, в группе II через 6 мес приема ЭЭ/ХМА наблюдалось значимое снижение обильности менструаций (p<0,05). Характер менструации по группам и в динамике на фоне приема контрацептива представлены в табл. 1.
Девять женщин (9,6%) из I группы и 16 (26,9%) из II группы жаловались на акне. Проводилась как субъективная, так и объективная оценка угревой сыпи до и на фоне приема контрацептива. Для оценки субъективных ощущений использовалась шкала от 0 до 100%. Во время каждого визита пациентки указывали процент выраженности акне на текущий момент времени.

По мнению пациенток из II группы степень выраженности угревых высыпаний через 3 месяца приема контрацептива уменьшилась на 7,23% (p<0,05), а через 6 мес снизилась с 28 до 10,49% (p<0,01) (рис. 2). В группе практически здоровых женщин также наблюдалось значимое снижение выраженности акне – с 20,39 до 11,05% через 6 месяцев приема препарата (p<0,01) (рис. 2).
Что касается повышенной жирности кожи, то в обеих группах также наблюдалось статистически значимое различие на всех временных срезах в обеих группах. С увеличением продолжительности приема динамика становилась более выраженной. До начала приема контрацептива повышенная жирность кожи лица наблюдалась у 24,2% пациенток из I группы и у 34,4% во II группе. Через 3 месяца выраженность жирности кожи лица статистически значимо снизилась до 14,2 и 23,0% соответственно (р<0,001), а через 6 месяцев приема – до 12,3 и 11,3% соответственно (р<0,001) (рис. 3).
Для объективной оценки степени тяжести течения угревой болезни использовали дерматологический индекс акне (ДИА). ДИА – это сумма баллов, которая количественно выражает каждый из основных симптомов угревой болезни – комедоны, папулы, пустулы, узлы. Числовые значения индекса представлены в табл. 2.

Значение ДИА определяет степень тяжести угревой болезни: легкая степень – от 1 до 5 баллов; средняя степень – от 6 до 10 баллов; тяжелая степень – от 11 до 15 баллов. До начала приема ЭЭ/ХМА угревая сыпь отсутствовала у 28 (29,79%) пациенток из I группы и у 7 (10,45%) пациенток из II группы. На фоне приема ЭЭ/ХМА уже через 3 месяца у 51 (54,26%) пациенток из I группы и у 19 (28,36%) пациенток из II группы отсутствовала угревая сыпь (различия с исходными данными статистически значимы, p<0,05). Данная положительная динамика еще в большей степени увеличилась через 6 месяцев от начала приема препарата, угревая сыпь отсутствовала у 60 (63,83%) женщин из I группы и у 32 (47,76%) из II группы (p<0,05). Уменьшилась и степень тяжести акне в обеих группах (рис. 4).
УЗИ органов малого таза проводилось на 5–7-й день менструального цикла или менструальноподобной реакции. До начала приема контрацептива у всех пациенток из I группы при УЗИ не было выявлено каких-либо особенностей. Во II группе УЗ-картина соответствовала клиническому диагнозу. Отрицательной динамики ни в одном случае выявлено не было, у пациенток с поликистозной морфологией яичников наблюдалось снижение объема яичников к шестому месяцу использования КОК.
Заключение
В течение 6 месяцев приема ЭЭ/ХМА ни одной беременности не наступило, что свидетельствует о высокой (100%) эффективности препарата.
Лечебный эффект КОК с ХМА проявлялся в общем снижении количества жалоб. Наиболее выраженные изменения касались характера менструации и симптомов, связанных с ней (снижалась болезненность менструаций, уменьшалось количество мажущих межменструальных выделений, значимо снижалась обильность менструации), а также улучшалось состояние кожи. Уменьшались частота и степень тяжести проявлений угревой болезни, кожа становилась менее жирной.
Антиандрогенные свойства ХМА, обусловленные снижением синтеза андрогенов, повышением синтеза половых стероидсвязывающих глобулинов и усиливающиеся за счет снижения экспрессии андрогеновых рецепторов и блокады 5α-редуктазы, позволяют активно использовать ЭЭ/ХМА для лечения акне. На фоне приема через 3–6 месяцев уменьшилась степень выраженности акне и жирность кожи как косвенные проявления антиандрогенного эффекта.
Необходимо отметить, что многочисленные дополнительные лечебные эффекты ЭЭ/ХМА позволяют использовать его в качестве высокоэффективного и безопасного контрацептива, обладающего дополнительными позитивными эффектами, такими как снижение выраженности акне, уменьшение обильности менструации, улучшение настроения женщины.



