1 N.I. Pirogov Russian National Research Medical University, Moscow, Russia;
2 Stavropol State Medical University, Stavropol, Russia;
3 Kuban State Medical University, Krasnodar, Russia;
4 Krasnoyarsk State Medical University named after prof. V.F. Voyno-Yasenetskii, Krasnoyarsk, Russia;
5 Ural Research Institute of Maternal and Infant Care, Yekaterinburg, Russia;
6 Nizhny Novgorod State Medical Academy, Nizhny Novgorod, Russia;
7 South-Ural State Medical University, Chelyabinsk, Russia;
8 Rostov State Medical University, Rostov-on-Don, Russia;
9 Tula State Medical Institute, Tula, Russia;
10 Yaroslavl State Medical Academy, Yaroslavl, Russia;
11 Siberian State Medical University, Tomsk, Russia;
12 Orenburg State Medical Academy, Orenburg, Russia;
13 Voronezh State Medical University, Voronezh, Russia;
14 Omsk State Medical University, Omsk, Russia;
15 Irkutsk State Medical University, Irkutsk, Russia;
16 Novosibirsk State Medical University, Novosibirsk, Russia;
17 Kazan State Medical Academy, Kazan, Russia;
18 Moscow State University of Medicine and Dentistry named after A.I. Evdokimov, Moscow, Russia;
19 Regional Perinatal Center, Yekaterinburg, Russia;
20 Perm State Medical University named after acad. E.A. Vagner, Perm, Russia;
21 Baltic State University named after Immanuel Kant, Kaliningrad, Russia;
22 Saratov State Medical University, Saratov, Russia;
23 Bashkir State Medical University, Ufa, Russia;
24 Volgograd State Medical University, Volgograd, Russia;
25 Moscow Regional Perinatal Center, Balashikha, Russia;
26 Astrakhan State Medical University, Astrakhan, Russia;
27 St. Petersburg State Pediatric Medical University, St. Petersburg, Russia
Objective. To assess obstetric and neonatal outcomes of the second half of pregnancy (after 22 weeks) in women with a habitual miscarriage who received or did not receive periconceptional care and therapy with micronized progesterone (a pharmaceutical product of Utrogestan) in the framework of TRISTAN-2 multicenter study.
Materials and methods. A total of 743 women who are 22–24 weeks pregnant and diagnosed with habitual miscarriage (2 or more consecutive interruptions of pregnancy in anamnesis) took part in the study. All patients included in TRISTAN-2 study, previously participated in TRISTAN-1 study (TRISTAN-2 study is a continuation of TRISTAN-1 patients’ observation). Of these, 369 patients in Group 1 received periconceptional care with micronized progesterone before conception in the luteal phase of their menstrual cycle and during the first half of pregnancy (intravaginally 200–400 mg / day), 374 patients in Group 2 started taking micronized progesterone only after the clinical confirmation of pregnancy and during the first half of pregnancy (intravaginally 200–400 mg / day). All patients underwent micronized progesterone therapy in the second half of pregnancy (intravaginally 200–400 mg / day) with the appropriate indications described in the instructions for the medical use of Utrogestan). The monitoring of patients in both groups was carried out in late pregnancy (starting from 22 weeks 0 days before discharge from the hospital after delivery). The study collected data on the course of the current pregnancy and its outcomes: gestational age at the time of delivery, neonatal outcomes, use of additional medications, complications and hospitalizations during pregnancy, adverse events on the part of the mother and/or fetus/child during the whole period of observation. All medical procedures performed as part of the study were routine and used in everyday clinical practice. Statistical analysis of the collected data was carried out using IBM SPSS 23 software.
Results. The main criterion for the therapy effectiveness was the frequency of preterm delivery before 34 full weeks of pregnancy. In Group 1 (patients who underwent periconceptional therapy with micronized progesterone), the incidence of preterm delivery was 8.9% (2.0% of preterm deliveries in the period of ≤33+6 weeks), in Group 2 (patients who started taking micronized progesterone only after the clinical confirmation of pregnancy) the incidence was 9.6% (1.7% of preterm deliveries in the period of ≤33+6 weeks) p> 0,05, which corresponds to the general population level in the world. Very early (before 28 weeks) and early
(28-30+6 weeks) premature births in the groups were not observed. On this basis, it can be concluded that the use of micronized progesterone in accordance with approved indications is an effective tool for the prevention of preterm delivery in patients at risk of a habitual miscarriage, regardless of previous periconceptional therapy. The frequency and nature of adverse events were statistically comparable in the groups (p> 0.05).
Conclusion. The presented results of the study prove the efficacy and safety of the use of micronized progesterone (the pharmaceutical product of Utrogestan) in accordance with the recorded indications in late pregnancy with a habitual miscarriage.
habitual abortion
habitual miscarriage
micronized progesterone
preterm delivery
Utrogestan
periconceptional care
Одной из актуальных проблем современного здравоохранения является охрана здоровья матери и ребен-ка [1]. При этом, несмотря на значительные достижения репродуктивной медицины в лечении невынашивания беременности, привычный выкидыш продолжает оставаться серьезной социальной проблемой [2]. Привычный выкидыш составляет до 20% в структуре невынашивания беременности в целом. После двух предшествующих самопроизвольных прерываний риск потери желанной беременности существенно возрастает по сравнению с риском потери первой беременности и составляет 36–38%. Таким образом, учитывая возрастающий с увеличением числа неудач риск потери беременности, большинство специалистов, занимающихся проблемой невынашивания, в настоящее время приходят к выводу, что достаточно двух последовательных выкидышей, чтобы отнести супружескую пару к категории привычного выкидыша с последующим обязательным обследованием и комплексом мер по подготовке к беременности [3]. У больных с привычным выкидышем недостаточность лютеиновой фазы выявляют до 60% случаев. Этот факт обуславливает необходимость назначения прогестерона таким пациентам с прегравидарного этапа, что подтверждено рядом зарубежных и российских исследований [4, 5], в частности исследованием ТРИСТАН-1, где была доказана эффективность и безопасность применения микронизированного прогестерона (препарата утрожестан) при привычном выкидыше во время прегравидарной подготовки и в течение беременности до 22 недель 0 дней гестации [6].
 Применение же прогестерона после клинического подтверждения беременности (после 8 недель 0 дней беременности), к сожалению, менее эффективно, что также подтверждают результаты международного исследования PROMISE [7].
Применение же прогестерона после клинического подтверждения беременности (после 8 недель 0 дней беременности), к сожалению, менее эффективно, что также подтверждают результаты международного исследования PROMISE [7].
Большинство научных работ по привычному выкидышу в настоящее время сосредоточены на причинах, прогнозах и лечении данного заболевания на прегравидарном этапе и ранних сроках беременности. Однако эта группа пациентов также подвержена более высокому риску возникновения акушерских осложнений в течение второй половины гестации таких, как преждевременные роды, преэклампсия, задержка и аномалии развития плода, placenta accrete [8]. Следовательно, дородовая медицинская помощь таким пациентам должна осуществляться с целью предотвращения этих осложнений. До сих пор остается неясным, связаны ли эти поздние акушерские осложнения со специфическими патологическими состояниями, такими как антифосфолипидный синдром или наследственные тромбофилии, часто являющиеся причиной привычного выкидыша.
Безусловно, пациентки с привычным выкидышем находятся в группе риска по преждевременным родам и требуют особого медицинского внимания. Анализ результатов ряда исследований показал, что относительный риск преждевременных родов возрастает почти в 2 раза в группе женщин с привычным выкидышем, ОР=1,74 (95% ДИ 1,38–2,19) [8]. Была выявлена статистически значимая корреляция между этими двумя патологическими состояниями [9–11]. Это, конечно же, является причиной увеличения риска перинатальной заболеваемости и смертности в популяции таких пациентов, ОР=1,22 (95% ДИ 1,02–1,46) [9, 10, 12]. Таким образом, имеющиеся в настоящее время научные данные свидетельствуют о достоверно худшем акушерском и неонатальном исходе беременности у женщин с привычным выкидышем [8].
Преждевременные роды являются существенной комплексной медико-социальной проблемой в России и мире, связанной с решением задач по улучшению качества последующей жизни детей, родившихся недоношенными, и сопряженными материально-экономическими затратами. Тяжесть осложнений, связанных с недоношенностью, обратно пропорциональна гестационному сроку преждевременных родов [13]. В связи с этим в настоящее время наиболее актуальными становятся вопросы медикаментозной профилактики преждевременных родов, особенно очень ранних (до 28 недель) и ранних (28–30+6 недель) преждевременных родов. Очевидно, что ее эффективность зависит в первую очередь от корректного выбора контингента беременных. Таким образом, беременные женщины с привычным выкидышем, составляют группу повышенного риска по преждевременным родам, требуют повышенной диагностической настороженности со стороны врача и своевременного применения эффективных терапевтических мер. Данный вопрос является одним из наиболее обсуждаемых в научном мире и представляет собой огромный интерес.
Для получения новых данных в отношении применения микронизированного прогестерона в рутинной клинической практике с целью профилактики преждевременных родов в группе пациентов с привычным выкидышем было проведено многоцентровое наблюдательное исследование ТРИСТАН-2 (наблюдение за пациентками во второй половине беременности, с 22 недель), что является непосредственным продолжением наблюдения за пациентами исследования ТРИСТАН-1 (наблюдение в первой половине беременности).
Цель данного исследования – оценить акушерские и неонатальные исходы второй половины беременности (с 22 недель) у женщин с привычным выкидышем, получавших и не получавших прегравидарную подготовку и терапию микронизированным прогестероном (лекарственным препаратом утрожестан) в рамках многоцентрового исследования ТРИСТАН-2.
Материал и методы исследования
В рамках многоцентрового наблюдательного исследования ТРИСТАН-2 были включены 743 беременные женщины 30,6±0,1 года на сроке беременности 22–24 недели с диагнозом привычный выкидыш (2 и более последовательных прерываний беременности в анамнезе). Все пациентки, включенные в данное исследование ТРИСТАН-2, принимали до этого участие в исследовании ТРИСТАН-1 (исследование ТРИСТАН-2 является продолжением наблюдения за пациентками исследования ТРИСТАН-1). Из них 369 пациенток группы 1 получали прегравидарную подготовку микронизированным прогестероном до зачатия в лютеиновой фазе менструального цикла и в течение первой половины беременности (интравагинально 200–400 мг/ сут), 374 беременных группы 2 начали прием препарата микронизированного прогестерона только после клинического подтверждения наступления беременности и в течение первой половины беременности (интравагинально 200–400 мг/сут). Все пациентки исследования получали терапию микронизированным прогестероном во второй половине беременности (интравагинально 200–400 мг/сут) при наличии соответствующих показаний, описанных в инструкции по медицинскому применению лекарственного препарата утрожестан. Наблюдение за пациентами велось в 31 исследовательском центре России.

Критериями включения в исследование служили: пациентки, завершившие участие в исследовании ТРИСТАН-1, с диагнозом привычный выкидыш (имеющие в анамнезе 2 и более самопроизвольных выкидыша), в возрасте от 18 до 35 лет (включительно), с прогрессирующей маточной беременностью на момент включения в исследование (с 22 недель 0 дней до 24 недель 0 дней беременности) наступившей на фоне или без прегравидарной подготовки препаратом микронизированного прогестерона спонтанно; информированное согласие пациентки на участие в исследовании. Решение врача о необходимости назначения пациентке препарата микронизированного прогестерона согласно утвержденной инструкции, а также о тактике дальнейшего ведения беременности принималось до включения пациентки в исследование и независимо от него.
Критерии исключения были следующими: применение любых гестагенов (за исключением препарата утрожестан) во время настоящей беременности; пациентки, ранее включенные в данное исследование, но выбывшие из исследования по какой-либо причине; любые клинические состояния, которые, по мнению врача-исследователя, затруднят трактовку результатов наблюдения; противопоказания к применению препарата утрожестан, перечисленные в инструкции.
Наблюдение за пациентками обеих групп проводилось во второй половине беременности с 22–24 недель до выписки из стационара после родов. Каждая пациентка проходила 3 последовательных визита исследования: Визит 1 (включение в исследование ТРИСТАН-2), Визит 2 (в 32–33 полных недель беременности) и Визит 3 (в день выписки из стационара после родов). В ходе исследования оценивались данные относительно течения текущей беременности и ее исходов: срок беременности на момент родов, неонатальные исходы, применение дополнительных лекарственных средств, осложнения и госпитализации в течение беременности, нежелательные явления со стороны матери и/или плода/ребенка, возникающие в течение всего периода наблюдения. Все выполняемые медицинские процедуры в рамках проведения исследования являлись рутинными, используемыми в повседневной клинической практике, что определило неинтервенционный (наблюдательный) характер исследования.
 Первичной конечной точкой (на основании которой оценивалась эффективность проводимой терапии) была частота преждевременных родов до 34 полных недель беременности. Безопасность оценивалась по анализу всех нежелательных явлений (НЯ) и серьезных нежелательных явлений (СНЯ), начиная с момента подписания участницей исследования информированного согласия до момента окончания участия в исследовании.
Первичной конечной точкой (на основании которой оценивалась эффективность проводимой терапии) была частота преждевременных родов до 34 полных недель беременности. Безопасность оценивалась по анализу всех нежелательных явлений (НЯ) и серьезных нежелательных явлений (СНЯ), начиная с момента подписания участницей исследования информированного согласия до момента окончания участия в исследовании.
Статистический анализ данных выполнялся с использованием программ IBM SPSS 23 и MS Excel 2016. Демографические данные, данные исходного состояния рассчитывались в виде частот или процентного отношения, или при помощи среднего значения (стандартного отклонения), медианы (межквартильного размаха), минимума и максимума, в зависимости от типа переменной. Для проверки гипотезы об исходной однородности групп исследования было проведено тестирование нулевых гипотез при помощи t-критерия Стьюдента (для количественных показателей между независимыми выборками с нормальным распределением в исследуемой популяции), критерия Манна–Уитни (для ординальных показателей или для интервальных показателей с распределением, отличающимся от нормального) или критерия χ2 (для качественных признаков). Если предпосылки применения критерия χ2 не выполнялись, применялся точный двусторонний критерий Фишера.
Для сравнительного анализа данных о нежелательных явлениях были подвергнуты анализу следующие параметры: количество, выраженность и длительность НЯ/СНЯ на фоне применения препаратов исследования, в группах исследования (на основании случаев НЯ, зафиксированных в формах отчета о НЯ в ИРК). Для сравнения частоты возникновения НЯ в группах исследования применялся критерий χ2, для сравнения степени выраженности (а также возможной причинно-следственной связи между препаратом и НЯ) применялся критерий Манна–Уитни.
Результаты исследования и обсуждение
Пациентки обеих групп были однородны по ряду клинико-анамнестических и социально-экономических характеристик, которые подробно описаны в статье «Терапия привычного выкидыша микронизированным прогестероном (результаты многоцентрового исследования ТРИСТАН-1)» [6].
Анализ эффективности проведенной терапии показал, что частота преждевременных родов у женщин с привычным выкидышем в группе 1 (прошедших прегравидарную подготовку микронизированным прогестероном) составила 8,9% (2,0% преждевременных родов на сроке ≤33+6 недель), в группе 2 (начавших прием микронизированного прогестерона только после клинического подтверждения наступления беременности) – 9,6% (1,7% преждевременных родов на сроке ≤33+6 недель) p>0,05, что соответствует общепопуляционному уровню в мире. При этом очень ранние (до 28 недель) и ранние (28–30+6 недель) преждевременные роды в группах не наблюдались (рис. 1). Таким образом, полученные данные демонстрируют лучшую динамику течения второй половины беременности, особенно до 28 недель, по сравнению с результатами проведенных ранее исследований, где частота преждевременных родов до 28 недель в группе пациенток с привычным невынашиванием достигала 28% [8, 14].
На этом основании можно сделать вывод, что применение микронизированного прогестерона в соответствии с утвержденными показаниями, является эффективным средством для профилактики преждевременных родов у пациенток группы риска с привычным выкидышем независимо от проведенной ранее прегравидарной подготовки. На настоящий момент микронизированный прогестерон является общепризнанным и хорошо изученным препаратом, используемым для профилактики преждевременных родов [15].
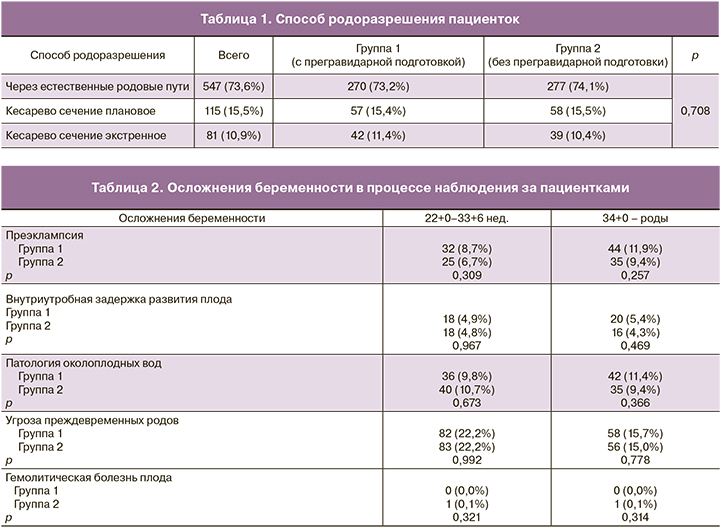
В большинстве наблюдений роды у пациенток велись через естественные родовые пути. Однако в ряде случаев применялось оперативное плановое и экстренное родоразрешение (табл. 1).
Статистический обзор осложнений беременности, возникших в процессе наблюдения за пациентками, показал, что обе группы были однородны по данным показателям (табл. 2).
Довольно высокий процент угрозы преждевременных родов, делает эту патологию существенным фактором риска у пациентов с привычным выкидышем.
Процент применения сопутствующей медикаментозной и хирургической терапии в группах пациентов не имел статистически значимых различий как в течение беременности, так и в процессе родов (табл. 3).
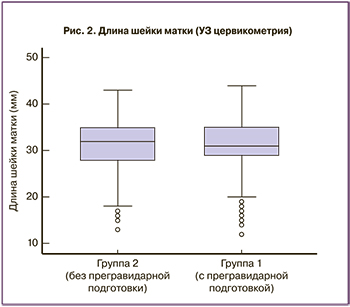
Проведение трансвагинальной ультразвуковой цервикометрии пациенткам при включении в исследование не выявило статистически значимых различий в длине шейки матки у пациенток обоих групп (p=0,679), среднее значение в группах составило 31,4±0,3 мм (рис. 2).
По количеству госпитализаций и их продолжительности обе группы были статистически сопоставимы (табл. 4).
При анализе состояния новорожденных, оцениваемого по шкале Апгар, статистически значимых различий выявлено в группах не было: Апгар 1-я минута – 7,59±0,04 и 7,64±0,04 балла, Апгар 5-я минута – 8,42±0,04 и 8,47±0,04 балла в первой и второй группах соответственно.
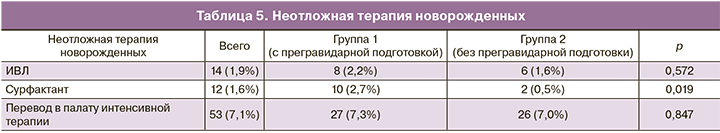
В ряде случаев потребовалось применение неотложной терапии новорожденных (табл. 5).
Оценка безопасности терапии, проводимая по анализу всех нежелательных явлений (НЯ) и серьезных нежелательных явлений (СНЯ) начиная с момента подписания участницей исследования информированного согласия до момента окончания участия в исследовании показала, что две группы пациентов статистически однородны по изучаемым признакам (p>0,05).
Заключение
Представленные результаты исследования демонстрируют эффективность и безопасность применения микронизированного прогестерона (препарата утрожестан) для профилактики преждевременных родов у пациенток группы риска с привычным выкидышем в соответствии с утвержденными показаниями препарата, независимо от проведенной ранее прегравидарной подготовки. Таким образом, возможно стоит рассматривать таких пациентов в качестве целевой популяции для рутинного назначения микронизированного прогестерона во второй половине беременности.
1. Манухин И.Б., Силаев К.А., Вученович Ю.Д. Влияние современной методики дородовой психопрофилактической подготовки беременных и альтернативных способов вагинального родоразрешения на течение и исход родов. Акушерство и гинекология. 2018; 2: 115-9. [Manukhin I.B., Silaev K.A., Vuchenovich U.D. Influence of modern methods of prenatal psychoprophylactic preparation of pregnant women and alternative methods of vaginal delivery on the course and outcome of labor. Akusherstvo i Ginekologiya/Obstetrics and Gynecology. 2018; (2): 115-9. (in Russian)] https://dx.doi.org/10.18565/aig.2018.2.115-119
2. Practice Committee of American Society for Reproductive Medicine. Definitions of infertility and recurrent pregnancy loss: a committee opinion. Fertil. Steril. 2013; 99(1): 63.
3. Савельева Г.М., Сухих Г.Т., Серов В.Н., Радзинский В.Е., ред. Акушерство. Национальное руководство. 2-е изд. М.: ГЭОТАР-Медиа; 2015: 189-98. [Savelyeva G.M., Sukhikh G.T., Serov V.N., Radzinsky V.E., ed. Obstetrics. National guideline. 2nd ed. Moscow: GEOTAR-Media; 2015: 189-98. (in Russian)]
4. Ismail A.M., Abbas A.M., Ali M.K., Amin A.F. Peri-conceptional progesterone treatment in women with unexplained recurrent miscarriage: a randomized double-blind placebo-controlled trial. J. Matern. Fetal Neonatal Med. 2018; 31(3): 388-94.
5. Stephenson M.D., McQueen D., Winter M., Kliman H.J. Luteal start vaginal micronized progesterone improves pregnancy success in women with recurrent pregnancy loss. Fertil. Steril. 2016; 107(3): 684-90.
6. Савельева Г.М., Аксененко В.А., Андреева М.Д., Базина М.И., Башмакова Н.В., Боровкова Л.В., Брюхина Е.В., Буштырева И.О., Волков В.Г., Гурьев Д.Л., Данькова И.В., Доброхотова Ю.Э., Егорова А.Т., Иванова Т.В., Константинова О.Д., Коротких И.Н., Кравченко Е.Н., Крамарский В.А., Кулешов В.М., Лебеденко Е.Ю., Мальцева Л.И., Манухин И.Б., Мартиросян С.В., Михельсон А.Ф., Олина А.А., Пашов А.И., Рогожина Е.И., Сахаутдинова И.В., Селихова М.С., Серова О.Ф., Синчихин С.П., Сичинава Л.Г., Тапильская Н.И., Цхай В.Б., Ярмолинская М.И. Терапия привычного выкидыша микронизированым прогестероном (результаты многоцентрового исследования ТРИСТАН-1). Акушерство и гинекология. 2017; 11: 44-55. [Saveleva G.M., Aksenenko V.A., Andreeva M.D., Bazina M.I., Bashmakova N.V., Borovkova I.V., Bryuhina E.V., Bushtyireva I.O., Volkov V.G., Gurev D.L., Dankova I.V., Dobrohotova Yu.E., Egorova A.T., Ivanova T.V., Konstantinova O.D., Korotkih I.N., Kravchenko E.N., Kramarskiy V.A., Kuleshov V.M., Lebedenko E.Yu., Maltseva L.I., Manuhin I.B., Martirosyan S.V., Mihelson A.F., Olina A.A., Pashov A.I., Rogozhina I.E., Sahautdinova I.V., Selihova M.S., Serova O.F., Sinchihin S.P., Sichinava L.G., Tapilskaya N.I., Tshay V.B., Yarmolinskaya M.I. Micronized progesterone therapy of recurrent pregnancy loss (results of multicenter Tristan-1 study). Akusherstvo i ginekologiya/Obstetrics and Gynecology. 2017; (11): 44-55. (in Russian)] https://dx.doi.org/10.18565/aig.2017.11.44-55
7. Coomarasamy A., Williams H., Truchanowicz E., Seed P.T., Small R., Quenby S. et al. A Randomized trial of progesterone in women with recurrent miscarriages. N. Engl. J. Med. 2015; 373(22): 2141-8.
8. Howard J.A. Carp, ed. Recurrent pregnancy loss: causes, controversies, and treatment. 2nd ed. CRC Press; 2014: 339-49.
9. Hughes N., Hamilton E.F., Tulandi T. Obstetric outcome in women after multiple spontaneous abortions. J. Reprod. Med. 1991; 36(3): 165-6.
10. Jivraj S., Anstie B., Cheong Y.C., Fairlie F.M., Laird S.M., Li T.C. Obstetric and neonatal outcome in women with a history of recurrent miscarriage: A cohort study. Hum. Reprod. 2001; 16(1): 102-6.
11. Thom D.H., Nelson L.M., Vaughan T.L. Spontaneous miscarriage and subsequent adverse birth outcomes. Am. J. Obstet. Gynecol. 1992; 166(1, Pt1): 111-6.
12. Sheiner E., Levy A., Katz M., Mazor M. Pregnancy outcome following recurrent spontaneous abortions. Eur. J. Obstet. Gynecol. Reprod. Biol. 2005;118(1): 61-5.
13. Ходжаева З.С., Дембовская С.В., Доброхотова Ю.Э., Сичинава Л.Г., Юзько А.М., Мальцева Л.И., Серова О.Ф., Макаров И.О., Ахмадеева Э.Н., Башмакова Н.В., Шмаков Р.Г., Клименченко Н.И., Муминова К.Т., Талибов О.Б., Сухих Г.Т. Медикаментозная профилактика преждевременных родов (результаты международного многоцентрового открытого исследования МИСТЕРИ). Акушерство и гинекология. 2016; 8: 37-43. [Khodzhaeva Z.S., Dembovskaya S.V., Dobrokhotova Yu.E., Sichinava L.G., Yuzko A.M., Maltseva L.I., Serova O.F., Makarov I.O., Akhmadeeva E.N., Bashmakova N.V., Shmakov R.G., Klimenchenko N.I., Muminova K.T., Talibov O.B., Sukhikh G.T.. Drug therapy for preterm birth: Results of the international multicenter open-label Mystery study. Akusherstvo i ginekologiya/Obstetrics and Gynecology. 2016; (8): 37-43. (in Russian)] http://dx.doi.org/10.18565/aig.2016.8.37-43
14. Reginald P.W., Beard R.W., Chapple J., Forbes P.B., Liddell H.S., Mowbray J.F., Underwood J.L. Outcome of pregnancies progressing beyond 28 weeks gestation in women with a history of recurrent miscarriage. Br. J. Obstet. Gynaecol. 1987; 94(7): 643-8.
15. Romero R., Nicolaides K.H., Conde-Agudelo A., O’Brien J.M., Cetingoz E., Da Fonseca E. et al. Vaginal progesterone decreases preterm birth ≤ 34 weeks of gestation in women with a singleton pregnancy and a short cervix: an updated meta-analysis including data from the OPPTIMUM study. Ultrasound Obstet. Gynecol. 2016; 48(3): 308-17.
Received 08.06.2018
Accepted 22.06.2018
Savelyeva, Galina M., Doctor of Medicine, Professor, academician of the Russian Academy of Sciences, Department of Obstetrics and Gynecology, N.I. Pirogov
Russian National Research Medical University. 117997, Russia, Moscow, Ostrovityanova str. 1 Tel.: +74954329897. E-mail:
agpf-gms@rambler.ru
Aksenenko, Viktor A., Doctor of Medicine, professor, Department of Obstetrics and Gynecology, Stavropol State Medical University.
355017, Russia, Stavropol, Mira str. 310. Tel.: +79624026899. E-mail:
aksenenko.vic@yandex.ru
Andreeva, Margarita D., Doctor of Medicine, Professor, department of obstetrics, gynecology and perinatology, Faculty of advanced training and professional retraining
of specialists. Kuban state medical university. 350063, Russia, Krasnodar, Sedina St., 4. E‑mail:
andreeva_md@mail.ru.
Bazina, Marina I., Doctor of Medicine, Professor, Department of Obstetrics and Gynecology, Krasnoyarsk State Medical University named after prof. V.F. Voyno-Yasenetskii. 660034, Russia, Krasnoyarsk, Krasnoyarskiy rabochiy pr. 170
Bashmakova, Nadezda V,, Doctor of Medicine, Professor, Director of Ural Research Institute of Maternity and Child Care, Ministry of Health of Russia.
620028, Russia, Ekaterinburg, Repina str. 1. Tel.: +73433718768. E-mail:
dr@niiomm.ru
Borovkova, Lyudmila V., Doctor of Medicine, Professor, Department of Obstetrics and Gynecology, Nizhniy Novgorod State Medical Academy.
603950, Russia, Nizhniy Novgorod, Minin and Pozharskiy Square, 10/1. Tel. +79519137727. E-mail:
BorovcovaLV@yandex.ru
Bryukhina, Elena V., Doctor of Medicine, Professor, Department of Obstetrics and Gynecology South-Ural State Medical University.
454080, Russia, Chelyabinsk, Vorovskogo str. 64. E-mail:
elena-bruhina@rambler.ru
Bushtyreva, Irina O., Doctor of Medicine, Professor, the Head of the Department of Obstetrics, Gynecology and Reproduction № 4, Rostov State Medical University,
Ministry of Health of Russia; leading researcher, Research Center of Obstetrics, Gynecology and Perinatology, Ministry of Health of Russia.
344022, Russia, Rostov-on-Don, Nakhichevan lane 29. Tel.: +7928770972. E-mail:
kio4@mail.ru
Volkov, Valeriy G., Doctor of Medicine, Professor, Department of Obstetrics and Gynecology, Tula State Medical Institute.
300012, Russia, Tula, pr. Lenina, 92. E-mail:
valvol@yandex.ru
Gurev, Dmitriy L., assistant professor, Department of Obstetrics and Gynecology Yaroslavl State Medical Academy, Yaroslavl, Russia, Chief Obstetrician-Gynecologist
of the Department of Health and Pharmacy of the Yaroslavl Region. 150003, Yaroslavl, Z. Kosmodemyanskoy, 9. Tel. +74852729279. E-mail:
d_guriev@mail.ru
Dankova, Irina, candidate of medical science, senior researcher, Research Department of Preservation of Reproductive Function, Ural Research Institute
for Maternity and Infancy. 620028, Russia, Yekaterinburg, Repina str. 1
Dobrokhotova, Yuliya E., Doctor of Medicine, Professor, Department of Obstetrics and Gynecology, N.I. Pirogov Russian National Research Medical University,
Ministry of Health of Russia. 117997, Russia, Moscow, Ostrovityanova str. 1. Tel.: +74952374033. E-mail:
pr.dobrohotova@mail.ru
Egorova, Antonina T., Doctor of Medicine, Professor, Department of Obstetrics and Gynecology, Krasnoyarsk State Medical University named
after prof. V.F. Voyno-Yasenetskii. 660034, Russia, Krasnoyarsk, Krasnoyarskiy rabochiy pr. 170
Ivanova, Tatyana V., assistant professor Department of Obstetrics and Gynecology, Siberian State Medical University.
634050, Russia, Tomsk, Moskovskiy trakt, 2. Tel.: +73822530423. E-mail:
office@ssmu.ru
Konstantinova, Olga D., Doctor of Medicine, Professor, Department of Obstetrics and Gynecology, Orenburg State Medical University.
460000, Russia, Orenburg, Sovetskaya str. 6. Tel.: +73532520612. E-mail:
const55@mail.ru
Korotkih, Irina N., Doctor of Medicine, Professor, Department of Obstetrics and Gynecology, Voronezh State Medical University.
394036, Russia, Voronezh, Studencheskaya str. 10. E-mail:
korotkikh_1950@mail.ru
Kravchenko, Elena N., Doctor of Medicine, Professor, Department of Obstetrics and Gynecology, Omsk State Medical University.
644099, Russia, Omsk, Lenina str. 12. E-mail:
kravchenko.en@mail.ru
Kramarskiy, Vladimir A., Doctor of Medicine, Professor, Department of Obstetrics and Gynecology, Irkutsk State Medical University.
664000, Russia, Irkutsk, Krasnogo Vosstaniya, 1. E-mail:
kramarskye@mail.ru
Kuleshov, Vitaliy M., Doctor of Medicine, Professor of the Department of Obstetrics and Gynecology, Novosibirsk State Medical University.
630091, Russia, Novosibirsk, Krasnyiy prospekt, 52. Tel.: +73833410436. E-mail:
kuleshov_vm@mail.ru
Lebedenko, Elizaveta Yu., Doctor of Medicine, Professor of the Department of Obstetrics and Gynecology, Rostov State Medical University.
344022, Russia, Rostov-on-Don, per. Nahichevanskiy, 29. Tel.: 8 (863) 252-24-65. E-mail:
Lebedenko08@mail.ru
Maltseva, Larisa I., Doctor of Medicine, Professor, Department of obstetrics and gynecology № 1, Kazan State Medical Academy.
420012, Russia, Kazan, Mushtari str. 11. Tel.: +78432333487. E-mail:
laramalc@mail.ru
Manukhin, Igor B., Honored Doctor of Russia, Doctor of Medicine, Professor, Department of Obstetrics and Gynecology, Medical Faculty, Moscow State University
of Medicine and Dentistry, Ministry of Health of Russia. 127473, Russia, Moscow, Delegatskaya str. 20, bld. 1. Tel.: +74991782831. E-mail:
mgmsugyn@mail.ru
Martirosyan, Sergey V., candidate of medical science, chief doctor of the regional perinatal center.
620000, Russia, Ekaterinburg, Serafimyi Deryabinoy, 32k2. E-mail:
smart.75@list.ru
Mihelson, Aleksandr F., Doctor of Medicine, Professor, Department of Obstetrics and Gynecology, Rostov State Medical University.
344022, Russia, Rostov-on-Don, per. Nahichevanskiy, 29. Tel: +78632522465
Olina, Anna A., Doctor of Medicine, Professor of the Department of Obstetrics and Gynecology, Academician E.A. Wagner Perm State Medical University,
Ministry of Health of Russia. 614000, Russia, Perm, Petropavlovskaya str. 26. Tel.: +73422364472. E-mail:
olina29@mail.ru
Pashov, Aleksandr I., Doctor of Medicine, Professor of the Department of Obstetrics and Gynecology, Baltic State University named after Immanuel Kant.
236000, Russia, Kaliningrad, Aleksandra Nevskogo, 14. E-mail:
pachov@mail.ru
Rogozhina, Irina E., Doctor of Medicine, Professor, Department of Obstetrics and Gynecology, Saratov State Medical University.
410012, Russia, Saratov, Bolshaya Kazachya, 112. E-mail:
itg.r@yandex.ru
Sahautdinova, Indira V., Doctor of Medicine, Professor, Department of Obstetrics and Gynecology, Bashkir State Medical University.
450000, Russia, Ufa, Lenina str. 3. Tel.: +73472721160. E-mail:
bgmu.ag@yandex.ru
Selikhova, Marina, Doctor of Medicine, professor of the department of obstetrics and gynecology, Volgograd State Medical University.
400131, Russia, Volgograd, Pavshih boytsov sq. 1. Tel.: +78442417002. E-mail:
selichovamarina@yandex.ru
Serova, Olga F., Doctor of Medicine, professor, chief physician of the Moscow Regional Perinatal Center. 143900, Russia, Moscow Region, Balashikha, sh. Enthusiasts, 12
Sinchihin, Sergey., Doctor of Medicine, Professor, Department of Obstetrics and Gynecology, Astrakhan State Medical University.
414000, Russia, Astrakhan, Bakinskaya, 121. E-mail:
Doc_sinchihin@rambler.ru
Sichinava, Lali G., Doctor of Medicine, Professor, Department of Obstetrics and Gynecology, N.I. Pirogov Russian National Research Medical University.
117997, Russia, Moscow, Ostrovityanova str. 1
Tapilskaya, Natalia I., Doctor of Medicine, Professor of the Department of Obstetrics and Gynecology, St Petersburg State Pediatric Medical University; leading scientific member ART department, D.O. Ott Scientific Research Institute of Obstetrics, Gynecology and Reproduction. Russia, St. Petersburg, Mendeleevskaya line, 3
Tskhay, Vitaliy B., Doctor of Medicine, Professor, Department of Perinatology, Obstetrics and Gynecology Medical Faculty, V.F. Voyno-Yasenetsky Krasnoyarsk State Medical University. 660022, Russia, Krasnoyarsk, P. Geleznyaka str. 1. Tel.: +79232872134. E-mail:
tchai@yandex.ru
Yarmolinskaya, Maria, Doctor of Medicine, Leading researcher of the Department of Reproduction Endocrinology, D.O. Ott Research Institute of Obstetrics, Gynecology, and Reproductology; Professor in the Department of obstetrics and gynecology № 2, North-Western Federal Medical Research Center, Ministry of Health of Russia.
199034, Russia, Saint-Petersburg, Mendeleevskaya line 154. Tel.: +78123289849. E-mail:
m.yarmolinskaya@gmail.com
For citations: Saveleva G.M., Aksenenko V.A., Andreeva M.D., Bazina M.I., Bashmakova N.V., Borovkova I.V., Bryuhina E.V., Bushtyireva I.O., Volkov V.G., Gurev D.L., Dankova I.V., Dobrohotova Yu.E., Egorova A.T., Ivanova T.V., Konstantinova O.D., Korotkih I.N., Kravchenko E.N., Kramarskiy V.A., Kuleshov V.M., Lebedenko E.Yu., Maltseva L.I., Manuhin I.B., Martirosyan S.V., Mihelson A.F., Olina A.A., Pashov A.I., Rogozhina I.E., Sahautdinova I.V., Selihova M.S., Serova O.F., Sinchihin S.P., Sichinava L.G., Tapilskaya N.I., Tshay V.B., Yarmolinskaya M.I. Outcomes of the second half of pregnancy in patients with recurrent pregnancy loss (results of multicenter study of TRISTAN-2). Akusherstvo i Ginekologiya/Obstetrics and Gynecology. 2018; (8): 111-21. (in Russian)
https://dx.doi.org/10.18565/aig.2018.8.111-121
 Применение же прогестерона после клинического подтверждения беременности (после 8 недель 0 дней беременности), к сожалению, менее эффективно, что также подтверждают результаты международного исследования PROMISE [7].
Применение же прогестерона после клинического подтверждения беременности (после 8 недель 0 дней беременности), к сожалению, менее эффективно, что также подтверждают результаты международного исследования PROMISE [7].


 Первичной конечной точкой (на основании которой оценивалась эффективность проводимой терапии) была частота преждевременных родов до 34 полных недель беременности. Безопасность оценивалась по анализу всех нежелательных явлений (НЯ) и серьезных нежелательных явлений (СНЯ), начиная с момента подписания участницей исследования информированного согласия до момента окончания участия в исследовании.
Первичной конечной точкой (на основании которой оценивалась эффективность проводимой терапии) была частота преждевременных родов до 34 полных недель беременности. Безопасность оценивалась по анализу всех нежелательных явлений (НЯ) и серьезных нежелательных явлений (СНЯ), начиная с момента подписания участницей исследования информированного согласия до момента окончания участия в исследовании.


