Трансформирующий фактор роста бета (Transforming growth factor beta, TGFβs) – белок, который контролирует пролиферацию, клеточную дифференцировку и другие функции в большинстве клеток; выделяемый клетками во внеклеточную среду, существует в трех изоформах: TGFβ1, TGFβ2 и TGFβ3 (TGFβs) [1]. TGFβs инициирует апоптоз в большинстве типов клеток и действует как антипролиферативный фактор в нормальных эпителиальных клетках и на ранних стадиях онкогенеза [2]. Некоторые клетки, секретирующие TGFβs, также имеют рецепторы для него; подобный механизм известен как аутокринная индукция [3].
В последнее десятилетие достигнут значительный прогресс как в идентификации генов, нарушения функции которых ведут к развитию злокачественных новообразований, так и в выяснении роли кодируемых ими белковых продуктов. Гены, вовлеченные в регуляцию процессов клеточного цикла, дифференцировки, морфогенетических реакций и апоптоза, могут быть объединены в несколько сигнальных каскадов, изменения в которых в конечном итоге приводят к возникновению злокачественных новообразований; к числу таких факторов относится фактор роста семейства TGFβ [1]. TGFβ инициирует апоптоз в большинстве типов клеток и действует как антипролиферативный фактор в нормальных эпителиальных клетках и на ранних стадиях онкогенеза [2]. Тем не менее, прогрессия цервикальной интраэпителиальной неоплазии (CIN) в цервикальную карциному сопровождается снижением восприимчивости трансформированных клеток к антипролиферативному действию цитокинов семейства TGFβ [4]. Также все три изоформы TGFβ способствуют индукции синтеза провоспалительных цитокинов в эпителиальных клетках шейки матки [5]. В связи с этим анализ экспрессии TGFβ в эпителии шейки матки при предраковых процессах представляет определенный интерес.
Цель работы – исследование регуляции клеточного цикла в эпителии эктоцервикса при инфицировании вирусом папилломы человека (ВПЧ) и формировании CIN путем изучения экспрессии в эпителиальных клетках изоформы TGFβs.
Материал и методы исследования
Наблюдаемые пациентки амбулаторно-поликлинического приема в количестве 105 человек были выявлены при обследовании в ООО «Центр эстетической гинекологии», г. Пермь. Протокол исследования был одобрен локальным этическим комитетом ГБОУ ВПО ПГМУ имени академика Е.А. Вагнера Минздрава России. Каждая пациентка получала подробную информацию о проводимом исследовании и давала информированное согласие на участие в исследовании и публикацию его результатов в открытой печати. Критериями включения пациенток в исследование было: наличие аномальных кольпоскопических картин, а именно пунктуации и мозаики; неравномерная реакция на нанесение раствора уксусной кислоты и различный ее уровень; визуализация ацетобелого эпителия; визуализация атипических сосудов; обнаружение нетипичной ткани шейки матки, особенно легко ранимой; неровная поверхность ткани шейки матки (плюс ткань); наличие папиллярных разрастаний или изъязвлений; наличие лейкоплакии шейки матки.
Критерии исключения пациенток из исследования: наличие на момент обследования острых воспалительных заболеваний репродуктивных органов, беременность; хламидийная, цитомегаловирусная и герпесвирусная инфекции урогенительного тракта в стадии обострения; экстрагенитальные заболевания в стадии декомпенсации; инфекционный, аллергический, аутоиммунный и лимфопролиферативный синдромы; онкологические заболевания; прием антибактериальных, противовирусных и иммунотропных препаратов на протяжении последних 3 месяцев. При постановке диагноза руководствовались Инструкцией по применению «Алгоритмы ранней диагностики предрака и рака шейки матки» Министерства здравоохранения республики Беларусь от 27.04.2007 № 150-1106 (Минск, 2007), а также Приказом Министерства здравоохранения и социального развития Российской Федерации от 2 октября 2009 г. № 808н «Об утверждении порядка оказания акушерско-гинекологической помощи».
Все исследования проведены в соответствие с Хельсинской декларацией Всемирной медицинской ассоциации (ВМА) «Этические принципы медицинских исследований с участием людей в качестве субъектов», принятой на 18-й Генеральной Ассамблее ВМА, Хельсинки, Финляндия, июнь 1964, с изменениями, внесенными на 64-й Генеральной Ассамблее ВМА, Форталеза, Бразилия, октябрь 2013, Основами Законодательства Российской Федерации «Об охране здоровья граждан», Приказом МЗ РФ № 266 от 19.07.03 г. «Об утверждении правил клинической практики в Российской Федерации», Национальным стандартом Российской Федерации «Надлежащая клиническая практика», 2005 г. Диагностика цервикальных интраэпителиальных неоплазий проводилась в соответствии МКБ-Х (1995).
Формирование групп пациентов при проведении гистологической оценки биоптатов осуществлялось с соблюдением принципов рандомизации. В исследуемой выборке пациентки с CIN I составили 39 человек, с CIN II – 24, с CIN III – 12 человек. Группу сравнения составляли 30 пациенток без CIN, но с доказанной ВПЧ-инфекцией методом полимеразной цепной реакции, для проведения которой использовали реагенты «АмплиСенс» («Интерлабсервис», Москва, Россия). Первоначально проводили качественный анализ с использованием набора реагентов «АмплиСенс», затем количественный – при помощи набора реагентов для выявления и количественного определения ДНК вирусов папилломы человека высокого канцерогенного риска «АмплиСенс ВПЧ ВКР скрин-титр-FL» (Метод детекции: FRT; генотипы 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59, 66 и 68 (суммарно) и генотипов 16, 18 и 45 – с дифференциацией), а также набора реагентов «АмплиСенс ВПЧ ВКР генотип-титр-FL» (Метод детекции: FRT; генотипы 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59, 66 и 68).

 Группы пациенток были сопоставимы по возрасту. Анализ клинико-анамнестического материала проводился по историям болезни пациенток и при проведении их клинического обследования. Кольпоскопии предшествовало проведение ПАП-теста и обследование пациенток на ВПЧ, а также цитологическое исследование. При этом для разделения пациенток на группы использовали гистологическую классификацию CIN. Биопсию проводили в условиях асептики и антисептики амбулаторно (на гинекологическом приеме). Иммуногистохимические исследования выполнены по стандартным протоколам с использованием реагентов Diagnostic BioSystems (USA). Для объективизации полученных данных вычисляли средний цитохимический коэффициент (СЦК), характеризуя динамику изменения интенсивности иммуногистохимического окрашивания в исследуемых группах. Оценка интенсивности пероксидазной метки и определение индекса пролиферации Ki-67 (ИП) проводились полуколичественным методом. Учитывалось число позитивных результатов на 100 учтенных ядер (при учете 500–1000 клеток) [6]. При определении экспрессии Ki-67 ядерная реакция любой интенсивности фиксировалась как позитивная [7]. Уровень пролиферации расценивался как низкий, если <15% клеток имели позитивную реакцию, умеренный, если 15–30% ядер были позитивны на Ki-67, и высокий – при позитивной реакции более 30% клеток.
Группы пациенток были сопоставимы по возрасту. Анализ клинико-анамнестического материала проводился по историям болезни пациенток и при проведении их клинического обследования. Кольпоскопии предшествовало проведение ПАП-теста и обследование пациенток на ВПЧ, а также цитологическое исследование. При этом для разделения пациенток на группы использовали гистологическую классификацию CIN. Биопсию проводили в условиях асептики и антисептики амбулаторно (на гинекологическом приеме). Иммуногистохимические исследования выполнены по стандартным протоколам с использованием реагентов Diagnostic BioSystems (USA). Для объективизации полученных данных вычисляли средний цитохимический коэффициент (СЦК), характеризуя динамику изменения интенсивности иммуногистохимического окрашивания в исследуемых группах. Оценка интенсивности пероксидазной метки и определение индекса пролиферации Ki-67 (ИП) проводились полуколичественным методом. Учитывалось число позитивных результатов на 100 учтенных ядер (при учете 500–1000 клеток) [6]. При определении экспрессии Ki-67 ядерная реакция любой интенсивности фиксировалась как позитивная [7]. Уровень пролиферации расценивался как низкий, если <15% клеток имели позитивную реакцию, умеренный, если 15–30% ядер были позитивны на Ki-67, и высокий – при позитивной реакции более 30% клеток.
Результаты исследований подвергали статистической обработке с применением программного пакета Biostat и приложения Microsoft Excel полнофункционального офисного пакета Microsoft Office 2007. При проведении статистической обработки результатов вычисляли выборочные средние, ошибку среднего и стандартное отклонение. Сравнение между собой двух выборок проводили при помощи критерия Стьюдента.
Результаты исследования и обсуждение
Женщины в изучаемой выборке были инфицированы следующими типами ВПЧ: 6, 16, 18, 31, 33, 35, 39, 45, 51, 56. Наиболее часто выявлялось инфицирование ВПЧ 16-го типа – 16 пациенток, что составило 44,44%, и инфицирование ВПЧ 51-го типа (8 человек – 22,22%). При проведении кольпоскопии просвет шейки матки имел вид узкого канала светло-красного цвета с древовидными сосудами стромы и прозрачными эпителиальными слоями. Отмечали наличие зон гиперемии, лейкоплакии, патологических сосудов, потерявших свою гибкость и древовидность, сосочковые образования, представляющие собой возвышения эпителия. При проведении пробы с уксусной кислотой у всех наблюдаемых пациенток мы наблюдали появление ацидофилии эпителия. Визуальные изображения пунктации и мозаики, образованные соединительнотканно-сосудистыми возвышениями и соответствующие клеточной интраэпителиальной пролиферации, встречались у 76 пациенток (72,38%). Ободки вокруг устьев выводных протоков желез встречались у 100% больных. При проведении пробы с раствором Люголя наличие йод-негативных зон было выявлено у 100% женщин; наличие неоднородных зон йода, косвенно свидетельствующее об инфицировании ВПЧ, также выявлено у 100% больных. У 68,57% пациенток всей анализируемой выборки отмечались проявления цервицита в виде отека и гиперемии слизистой оболочки, полнокровия ее сосудов, наличия выделений слизисто-гнойного характера. Но, как известно, аналогичные кольпоскопические изображения могут иметь место при различных патофизиологических процессах, в связи с чем следующим этапом нашей работы явилось проведение гистологического исследования.
В соответствие с МКБ-10, рубрикой N87, различали: N87.0 Слабовыраженную дисплазию шейки матки (CIN I); N87.1 Умеренную дисплазию шейки матки (CIN II); N87.2 Резко выраженную дисплазию шейки матки (CIN III). Легкую дисплазию определяли при наличии гиперплазии клеток базального и парабазального слоев многослойного плоского эпителия (МПЭ), клеточного и ядерного полиморфизма, повышения митотической активности в них [8]. Среднюю степень дисплазии устанавливали при наличия поражения 1/2-1/3 толщи МПЭ; наличии клеточного полиморфизма (вытянутые, овальные, тесно прилегающие друг к другу клетки, визуализация митозов, в том числе и патологических); незначительного ядерно-цитоплазматического сдвига (ядра крупные, грубая структура хроматина, в ядрах определяются небольшие ядрышки). При выраженной дисплазии эпителия шейки матки гиперплазированные клетки базального и парабазального слоев обнаруживали по всей толщине эпителиального пласта; ядра визуально крупные, овальные или вытянутые, гиперхромные, с митозами, выраженным ядерным полиморфизмом, выраженным ядерно-цитоплазматическим сдвигом, двуядерные клетки. Вместе с тем, клетки сохраняли четкие границы, и их можно дифференцировать на принадлежность к тому или иному слою МПЭ.
В группе сравнения (отсутствие CIN на фоне имеющейся ВПЧ-инфекции) строение эпителиального пласта типичное без признаков дисплазии, но часто – с гипер- и паракератозом. Под слоями МПЭ визуализируется собственная пластинка слизистой оболочки, представленная слоем оформленной соединительной ткани, в которой видны кровеносные сосуды. В группе пациенток с CIN I отмечалась дисплазия базальных слоев плоского эпителия – не более одной трети (нижней) эпителиального пласта. Клетки верхних двух третей остаются зрелыми, хотя в них и обнаруживаются дистрофические изменения. В группе с CIN II мы находили более выраженные диспластические изменения МПЭ эктоцервикса, выражающиеся в гиперхромии ядер, их неправильной форме, нарушении стратификации эпителиального пласта и созревания эпителиальных клеток – появление клеток, подобным базальным, в вышележащих слоях эктоцервикса. Патологически измененные клетки занимали у пациенток этой группы до двух третей эпителиального пласта. В группе пациенток с CIN III диспластические изменения плоского эпителия занимали в более двух третей эпителиального пласта; дифференциация слоев практически не прослеживается. Параллельно отмечалось нарастание выраженности атипии – повышение ядерно-цитоплазматического отношения, гиперхроматоз и полиморфизм ядер с неравномерным распределением хроматина.
Анализируя экспрессию TGFβs, мы наблюдали ее в клетках базального слоя эктоцервикса у пациенток группы сравнения (рис. 1) в 60% случаев, базального и парабазального – в 30%, базального, парабазального и промежуточного – в 10% случаев; у всех пациенток – отсутствие экспрессии в однослойном столбчатом эпителии в зоне трансформации.
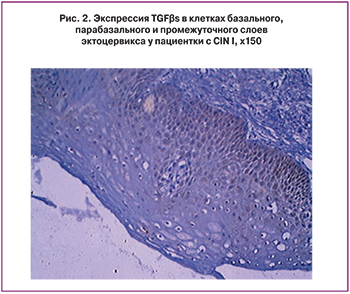
В группе с CIN I экспрессия TGFβs определялась в клетках базального слоя у 48,72% пациенток, базального и парабазального – у 30,77% пациенток данной группы, базального, парабазального и промежуточного – у 12,82% (рис. 2); у 7,6% больных экспрессия этого маркера выявлена не была. Также выявлено отсутствие экспрессии TGFβs в призматическом эпителии в зоне трансформации и наботовых желез в собственной пластинке слизистой оболочки шейки матки.
В группе с CIN II экспрессия TGFβs определялась в базальном и парабазальном слоях эктоцервикса – у 20,83% пациенток или только в базальном слое – у 50% женщин этой группы, у части пациенток (29,17%) не определялась. Также экспрессия этого маркера отсутствовала в призматическом эпителии зоны трансформации и наботовых желез.
В группе с CIN III у большинства пациенток (83,33%) экспрессия TGFβs отсутствовала – как в плоском эпителии эктоцервикса (рис. 3), так и в призматическом эпителии наботовых желез и в зоне трансформации.
При проведении количественной оценки экспрессии TGFβs (определение СЦК) в эпителии шейки матки у наблюдаемых пациенток установлено, что в базальном, парабазальном и промежуточном слоях экстоцервикса экспрессия TGFβs статистически значимо более выражена в группах ВПЧ-инфекция без CIN, с CIN I, с CIN II, чем в группе с CIN III (таблица).
В группе сравнения (отсутствие CIN на фоне имеющейся ВПЧ-инфекции) экспрессия Ki-67 определялась исключительно в базальном и парабазальном слоях, ИП=15,23±2,57%. В группе с CIN I экспрессия Ki-67 также определялась исключительно в базальном и парабазальном слоях, ИП=21,44±2,69%. В группе с CIN II экспрессия Ki-67 определялась в базальном и парабазальном слоях, ИП=49,12±3,52%, а также в промежуточном слое, ИП=33,64±4,93%. В группе с CIN III экспрессия Ki-67 определялась в базальном, парабазальном и поверхностном слоях, ИП=63,28±4,31%.
В современных литературных источниках приводятся разноречивые данные, касающиеся уровня экспрессии белков семейства TGFβ в эпителии эктоцервикса у пациенток с CIN и ВПЧ. Так, одни авторы отмечают увеличение уровня TGFβ в цервикальной слизи при дисплазии шейки матки и цервикальном раке [9]. Другие исследования также указывают на нарастание интенсивности экспрессии и увеличение слоев эпителия, экспрессирующих TGFβ в ряду CIN I – CIN III, но, тем не менее, уменьшение экспрессии при переходе в cancer in situ [10]. С другой стороны, на сегодняшний день также известно, что в процессе прогрессирования карциномы шейки матки экспрессия белков семейства TGFβ уменьшается [4]. Кроме того, при этом прогрессия CIN в цервикальную карциному сопровождается снижением восприимчивости трансформированных клеток к антипролиферативному действию цитокинов этого семейства [11].
TGFβ является мощным ингибитором роста эпителиальных клеток; тип 16 ВПЧ оказывает существенное влияние на рост и дифференцировку эпителия эктоцервикса. В этих условиях TGFβ1 участвует в ремоделировании эпителия в качестве важного паракринного/аутокринного фактора, действие которого направлено на ограничение распространения ВПЧ-инфекции путем стимуляции апоптоза [12] и ингибирования пролиферации эпителиальных клеток, инфицированных ВПЧ [10]. Кроме того, известно, что все три изоформы TGFβ способствуют индукции синтеза провоспалительных цитокинов в эпителиальных клетках шейки матки [5].
Заключение
Таким образом, учитывая полученные результаты, можно утверждать, что экспрессии TGFβs в эпителии эктоцервикса по мере прогрессирования CIN уменьшается, вплоть до полного исчезновения, что, по-видимому, свидетельствует о снижении антипролиферативной активности эпителия посредством аутокринной регуляции.



