Маточные кровотечения стабильно занимают 2-е место среди причин госпитализаций в гинекологические стационары. При отсутствии поддерживающей терапии после остановки кровотечения частота рецидивов может достигать 70–80%. При этом следует учитывать, что более 60% гистерэктомий выполняются в связи с заболеваниями, проявляющимися рецидивирующими маточными кровотечениями [1].
В качестве хирургического гемостаза при аномальных маточных кровотечениях (АМК) почти всегда выполняется выскабливание стенок полости матки, которое останавливает кровотечение, но не профилактирует рецидивы. Подобное вмешательство сопровождается неизбежной травматизацией шейки матки и эндометрия, что может быть фактором риска осложнений последующих беременностей (невынашивания беременности, плацентарной недостаточности, задержки роста плода, преждевременных родов) [1, 2]. Несмотря на высокий процент рецидивов, в настоящее время в Российской Федерации гормональную терапию при АМК получают только 19% пациентов из числа женщин, которым она показана [2, 3].
Согласно актуальным клиническим рекомендациям РОАГ «Аномальные маточные кровотечения» (2021), рекомендуется проведение хирургического лечения у пациенток с АМК при неэффективности медикаментозной терапии, противопоказаниях к ней [4]. Таким образом, еще раз подчеркивается, что необходимым компонентом лечения АМК после исключения злокачественных новообразований является медикаментозная терапия, направленная на достижение длительной ремиссии заболевания.
Назначение гормональной терапии с противорецидивной целью и объяснение ее важности должны происходить еще на этапе госпитализации. Далее, по окончании стационарного лечения, с пациенткой еще раз необходимо обсудить, что операция не является заключительным этапом лечения, и ей необходима длительная (более 6 месяцев) терапия. Далее, на амбулаторном этапе, повторно проводится беседа с пациенткой о необходимости поддерживающей лечебной, а затем противорецидивной терапии. Важны преемственность всех уровней лечебно-профилактических учреждений на каждом этапе лечения АМК и организационные меры в стандартизации ведения пациенток с АМК [5].
Этиология и эпидемиология
АМК могут быть классифицированы как острые или хронические. Острое АМК – эпизод сильного кровотечения, который, как правило, требует немедленного вмешательства и принятия мер для предотвращения гиповолемии. Хроническое АМК может быть определено как кровотечение, чрезмерное по продолжительности, объему и/или частоте, повторяющееся более 3 месяцев [6, 7].
В репродуктивном возрасте особое внимание уделяется не только нормализации менструального цикла, но и наличию регулярной и своевременной овуляции. Международной федерацией акушеров и гинекологов (International Federation of Gynecology and Obstetrics, FIGO) в 2022 г. разработана новая классификация нарушений овуляции, которая позволяет врачу определить уровень поражения, лежащего в основе механизма развития овуляторной дисфункции, и назначить необходимое обследование и лечение. Также в работе подчеркивается, что у здоровой женщины в репродуктивном возрасте (если она не беременна, не кормит грудью, не принимает комбинированные оральные контрацептивы (КОК)) овуляция предсказуема и циклична. Овуляторная дисфункция (от редкого отсутствия овуляции до хронической ановуляции) приводит к различным нарушениям менструального цикла и бесплодию [8].
Некоторые виды медикаментозной терапии АМК обладают контрацептивными свойствами (могут подавлять овуляцию). Эти особенности необходимо учитывать для пациенток молодого возраста, заинтересованных в реализации репродуктивной функции [8].
В подростковом возрасте АМК чаще встречаются из-за незрелости гипоталамо-гипофизарно-яичниковой системы. Такие кровотечения (в подростковом или раннем репродуктивном периодах) чаще являются ановуляторными. Время, необходимое для достижения зрелости гипоталамо-гипофизарно-яичниковой оси, обеспечивающей овуляторные циклы и последующие регулярные менструации, варьирует от шести месяцев до трех лет после менархе. Поэтому первое время менструальные циклы могут быть нерегулярными и непредсказуемыми по объему и продолжительности кровотечения [6].
Среди всех обращений к врачу по поводу АМК примерно 70% приходится на период менопаузального перехода. В этот период изменяется длительность менструальных циклов; они зачастую становятся ановуляторными, что оказывает негативное влияние на эндометрий, увеличивая риск гиперплазии эндометрия и АМК. Отсутствие противодействия эффектам эстрогенов (дефицит прогестерона) приводит к непрерывной пролиферации эндометрия. Соответственно, эпизоды кровотечений становятся нерегулярными, пролонгированными и/или чрезмерными.
Клиническое и анатомическое разнообразие патологических состояний, которые могут встречаться при АМК, диктует необходимость определения индивидуальной стратегии лечения, которая будет во многом зависеть от возраста, выявленного заболевания и индивидуальных данных на момент обращения.
Учитывая высокую частоту рецидивов, необходимо принятие дополнительных мер по повышению взаимодействия между врачами амбулаторного и стационарного звеньев в рамках оказания квалифицированной и комплексной помощи данной группе пациенток, повышению информированности пациенток о необходимости длительной гормональной терапии для профилактики рецидива АМК.
Оценка и диагностика аномального маточного кровотечения
Первоначальная оценка АМК должна включать подробный анамнез пациентки и данные объективного обследования. Необходимо как уточнение семейного анамнеза, так и анамнеза, направленного на выявление факторов риска гематологических заболеваний и рака эндометрия [9, 10].
В рамках первичного консультирования следует провести физикальное обследование, сосредоточив внимание на проявлениях синдрома поликистозных яичников, на признаках инсулинорезистентности или нарушений функции щитовидной железы, симптомах коагулопатий и геморрагических заболеваний в виде петехий, синяков, а также осмотр на наличие поражений во влагалище или шейке матки и определение объема матки [10]. Для того чтобы оценить количество или объем кровопотери во время менструации и влияние, которое оно оказывает на пациентку, используются общедоступные графики, анкеты и результаты измерений, сообщаемых каждой пациенткой [8].
У пациенток репродуктивного возраста с маточным кровотечением в первую очередь необходимо исключить беременность, поэтому определение уровня β-субъединицы хорионического гонадотропина является обязательным. Пациентки с АМК, как с острыми, так и хроническими, должны быть обследованы на дефицит железа, уровень ферритина в сыворотке и вторичную анемию. Показано также проведение клинического анализа крови и коагулограммы.
Впоследствии врач проводит поиск причины АМК по каждому из компонентов классификации FIGO PALM-COEIN [11].
Аббревиатура PALM отражает структурные изменения:
- Polyp (полип);
- Adenomyosis (аденомиоз);
- Leiomyoma (лейомиома);
- Malignancy and hyperplasia (малигнизация и гиперплазия).
- Аббревиатура COEIN – функциональные нарушения:
- Coagulopathy (коагулопатия);
- Ovulatory dysfunction (овуляторная дисфункция);
- Endometrial (эндометриальное);
- Iatrogenic (ятрогенное);
- Not identified (не классифицированное).
Оценка PALM
При обследовании пациенток в первую очередь исключаются структурные поражения: вагинальные, цервикальные, маточные. Часть из них могут быть выявлены при рутинном гинекологическом обследовании. Ультразвуковое исследование (УЗИ) органов малого таза должно выполняться в качестве дополнения к гинекологическому осмотру для диагностики причин АМК. Этот метод имеет хорошую чувствительность, однако в ряде случаев – низкую специфичность [12].
По этой причине для достижения точной диагностики структурных нарушений полости матки показано проведение гистероскопии, которая позволяет выполнить биопсию поражений; фактически она обладает большей чувствительностью (94,4%) и специфичностью (99,6%) для определения злокачественности выявленных поражений [12]. Этих исследований обычно достаточно для постановки диагноза полипа, лейомиомы, гиперплазии или злокачественных поражений эндометрия.
Оценка COEIN
Полезным и эффективным инструментом скрининга для выявления коагулопатий является хорошо структурированный анамнез. FIGO рекомендует использование опросников для пациента, которые имеют чувствительность до 90% для выявления этих нарушений. Данная таблица включает историю кровотечений или наследственно-семейную историю коагулопатий в дополнение к анамнезу послеоперационных кровотечений и обильных менструаций с момента менархе. Пациентов с положительным результатом скрининга необходимо направить на консультацию к гематологу. При выявлении коагулопатии данный тип нарушения будет классифицирован как АМК-С (коагулопатии) [11–13].
Предсказуемые циклические менструации каждые 24–38 дней обычно ассоциируются с сохраненной овуляцией. При этом кровотечения, связанные с нарушением овуляции, обычно нерегулярны как по времени, так и по продолжительности и часто чередуются с периодами аменореи. Если какая-либо структурная патология уже исключена и у пациентки обнаружено АМК, связанное с ановуляторными циклами, данный тип нарушения классифицируется как АМК-О (связанное с дисфункцией яичников) [11, 12].
АМК-I (ятрогенные) включают использование системных препаратов, прогестагенов/КОК (в том числе и в виде внутриматочных спиралей). В этом разделе учитывается не только использование половых стероидов, но и препаратов, которые могут влиять на их выработку или функцию.
К АМК-E (эндометриальные) относят АМК после исключения структурных причин, как правило, на фоне регулярного ритма менструаций. К этой категории можно отнести кровотечения, связанные, например, с хроническим эндометритом [11, 12].
Категория АМК-N (неклассифицированные) была создана для включения еще не классифицированных или редко встречающихся расстройств. Они могут включать, но не ограничиваются, такими состояниями, как артериовенозные мальформации, истмоцеле, и другими патологиями [11, 12].
Лечение
Цели лечения женщин с АМК – остановка кровотечения, поддержание нормального объема циркулирующей крови, лечение и профилактика анемии, нормализация менструального цикла и улучшение качества жизни пациенток. В первую очередь должна быть установлена причина АМК. Необходимо также исключить сопутствующие заболевания, которые могут быть причиной АМК, – например, гипотиреоз.
В настоящее время существует множество эффективных вариантов лечения острого АМК [14]. В зависимости от клинической ситуации применяются и комбинируются различные методы лечения нарушений менструального цикла – негормональные, хирургические и гормональные. Выбор схемы лечения в каждом клиническом случае должен проводиться совместно с пациенткой в зависимости от клинической картины, показаний/противопоказаний, индивидуальных предпочтений пациентки, наличия репродуктивных планов и т.д. [4]. Одним из важных аспектов является своевременное назначение антианемической терапии при ее выявлении или коррекция латентного дефицита железа.
После купирования картины острого АМК необходимо продолжить прием противорецидивной терапии, направленной на профилактику рецидивов заболевания [14].
Острое событие
Первоначальная оценка пациентов с острым АМК должна включать быструю первичную оценку признаков гиповолемии и гемодинамической нестабильности. Основными целями лечения острого AМК являются:
1) остановка текущего эпизода кровотечения;
2) коррекция сопутствующих состояний (анемии, гиповолемии);
3) выявление причины АМК и профилактика рецидива.
Варианты терапии острого АМК включают негормональные и гормональные методы остановки кровотечения, хирургическое лечение и их комбинации.
Гормональная терапия и применение транексамовой кислоты, как правило, являются первой линией медикаментозной терапии для остановки острого АМК у пациенток без известных или предполагаемых нарушений свертываемости крови. При неэффективности медикаментозной терапии в остановке кровотечения показано хирургическое вмешательство.
Хирургическое лечение
Хирургические варианты терапии включают выскабливание стенок полости матки, резекцию или аблацию эндометрия, гистерэктомию. Хирургическое лечение рассматривается при неэффективности консервативной терапии или в неотложных случаях, угрожающих жизни пациента. Сохранение фертильности всегда должно рассматриваться как приоритет при выборе тактики лечения [10, 14–16].
У женщин репродуктивного возраста выскабливание стенок полости матки оказалось не столь эффективным при лечении обильного маточного кровотечения. Более того, исследования показали, что абляция эндометрия посредством различных методов успешно уменьшает кровотечение у женщин в постменопаузе, однако она не рекомендуется для лечения подростков и молодых женщин из-за негативного влияния на фертильность и высокой частоты терапевтических неудач.
Гистерэктомия для лечения заболеваний, проявляющихся АМК, по-прежнему рассматривается как крайняя мера. Наиболее часто такой вариант лечения рассматривается при неэффективности других методов или при наличии жизнеугрожающих состояний [10, 14, 17].
Гормональная терапия
Рекомендуется проводить гормональный гемостаз, в т.ч. в комбинации с негормональными методами терапии, как метод остановки острого АМК, не связанного с органической патологией органов малого таза или нарушениями свертываемости крови.
Допустимо назначение гестагенов или КОК для пациенток, нуждающихся в контрацепции [4].
Для проведения гормонального гемостаза в случаях острых АМК используют монофазные КОК в дозе не более 100 мкг/сут до остановки кровотечения по 1 таблетке с равными интервалами, с последующим снижением дозы до 1 таблетки в сутки. Продолжительность терапии – 21 день от начала лечения [4].
Как альтернатива КОК для лечения АМК пациенткам может быть рекомендовано применение прогестагенов в пролонгированном циклическом режиме, в том числе и дидрогестерона по 10 мг 2 раза в сутки. При этом отмечено, что эффективность 21-дневной схемы прогестагенов сопоставима с приемом КОК [4]. Для профилактики АМК прием дидрогестерона может быть продолжен в схеме с 11-го по 25-й дни менструального цикла по инструкции, или пациентке может быть рекомендована установка левоноргестрел-выделяющей внутриматочной системы (ЛНГ-ВМС) (52 мг) [4].
Негормональные методы терапии
Негормональным вариантом лечения острых состояний являются нестероидные противовоспалительные препараты (НПВП) и транексамовая кислота: НПВП снижают уровень простагландинов путем ингибирования циклооксигеназы, что способствует сужению сосудов. Снижение кровопотери при применении НПВП составляет 30–40% [4]. Данный вид терапии может уменьшить обильные менструальные кровотечения и полезен для пациенток, которые предпочитают избегать или имеют противопоказания к гормональной терапии [18]. Как гемостатическое средство может быть использована транексамовая кислота в дозировке 500 мг по 2 таблетки 3 раза в день до 4 дней. Такая терапия обычно оказывается эффективной в остановке/уменьшении кровотечения, но не профилактирует повторные эпизоды АМК.
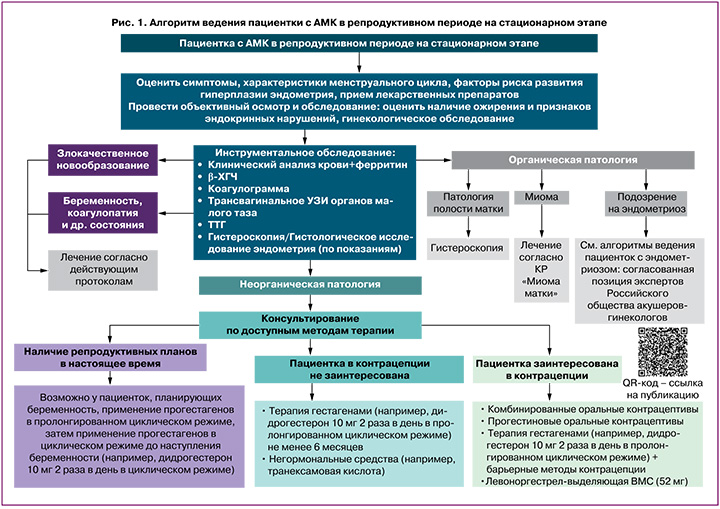
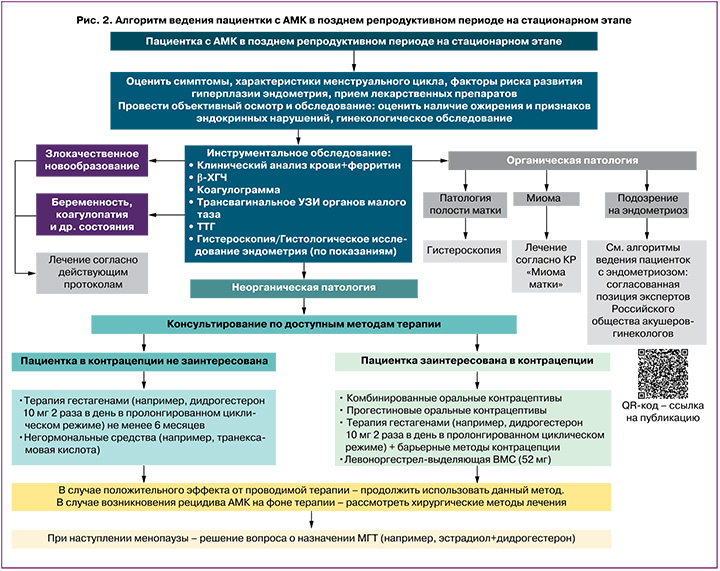
На рисунках 1 и 2 представлены алгоритмы ведения пациенток с АМК в репродуктивном периоде и пациенток в позднем репродуктивном периоде на стационарном этапе.
Терапия хронического аномального маточного кровотечения
Целями лечения хронического AМК являются:
1) остановка текущего эпизода кровотечения;
2) профилактика последующих эпизодов АМК;
3) восстановление нормального менструального цикла, уменьшение менструальной кровопотери в последующих циклах;
4) при наличии репродуктивных планов – восстановление и сохранение фертильности.
На стационарном этапе с пациенткой необходимо обсудить этапы лечения АМК, так как пациентки нуждаются в патогенетически обоснованной терапии АМК в любом возрасте.
Учитывая длительность терапии, обязательным является акцент на индивидуальных потребностях пациентки. Так, при наличии репродуктивных планов терапия не должна нарушать синтез гонадотропных и половых гормонов и подавлять овуляцию [8].
В большинстве случаев лечение хронического АМК проводится амбулаторно. При выборе тактики лечения определяющее значение имеют наличие репродуктивных планов или потребности в контрацепции, наличие сопутствующих заболеваний и личные предпочтения [18].
Гормональная терапия
Для гормональной терапии АМК могут быть использованы различные группы препаратов в зависимости от нужд конкретной пациентки. Согласно данным Кокрейновского обзора и сетевого метаанализа 2022 г., к терапии первой линии, эффективно уменьшающей объем кровопотери у пациенток с АМК, относятся ЛНГ-ВМС, антифибринолитики и прогестагены в пролонгированном циклическом режиме [19].
При отсутствии запроса со стороны пациентки на гормональную контрацепцию следует отдать предпочтение гормональной терапии с использованием гестагенов. Гестагены различаются по своей способности децидуализировать эндометрий, и это определяет их успех в уменьшении или прекращении эндометриального кровотечения. Как известно, наличие эстрогенной стимуляции в отсутствие прогестерона может привести к гиперплазии эндометрия [1].
Гестагены прекращают индуцированный эстрогенами рост эндометрия, стабилизируют сосудистую сеть эндометрия и блокируют неограниченный рост сосудов, запускают каскад свертывания крови, обеспечивают гемостатическое и антифибринолитическое действие (через PAI-1) и снижают активность матриксных металлопротеиназ.
Дидрогестерон имеет зарегистрированные показания для лечения АМК, оказывает патогенетическое действие через поддержание уровня прогестерона, что влечет за собой полноценную секреторную трансформацию эндометрия без подавления овуляции [20, 21].
Учитывая возможную длительность терапии более года, необходимо оценить риски назначения гормональных препаратов. Дидрогестерон оказывает действие только через рецепторы прогестерона, имеет большую биодоступность при пероральном приеме при высоком профиле безопасности и переносимости, благодаря чему может подходить для длительного применения [22].
Агонисты гонадотропин-рилизинг-гормона применяются в наиболее тяжелых случаях хронического АМК, особенно при наличии сочетанной патологии, миомы матки или эндометриоза, и при неэффективности других медикаментозных препаратов. Следует учитывать спектр побочных эффектов через 3–4 недели терапии агонистами: аменорея и атрофия эндометрия, перепады настроения, вазомоторные симптомы. Длительный прием агонистов ассоциирован со снижением минеральной плотности костной ткани, что требует назначения «add-back терапии» [14].
Если пациентка нуждается в контрацепции, целесообразно провести полное консультирование о доступных методах контрацепции. Определение метода контрацепции должно основываться на наличии медицинских показаний и критериях приемлемости, предпочтениях пациентки, эффективности, безопасности, простоте использования и периоде, в течение которого необходима контрацепция [23].
Применение барьерных методов контрацепции в комбинации с гестагенами может быть предпочтительным при наличии противопоказаний к другим методам контрацепции, а также при нерегулярной половой жизни.
Согласно данным Кокрейновского обзора и сетевого метаанализа 2022 г., ЛНГ-ВМС (52 мг) является первой линией терапии для снижения объема менструальной кровопотери у пациенток с АМК, не заинтересованных в беременности. При выборе данного метода следует учитывать возможные технические сложности при установке ВМС [21, 24–26].
Согласно результатам исследования 2023 г., оценивающего влияние ЛНГ-ВМС и дидрогестерона в пролонгированном циклическом режиме на качество жизни и сексуальную функцию у пациенток с АМК, существенной разницы в эффективности обнаружено не было. Единственное значительное улучшение наблюдалось с позиции восстановления сексуальной функции в группе применения дидрогестерона в пролонгированном циклическом режиме [27].
В исследование Подзолковой Н.М. и соавт. (2018), представивших анализ данных в подгруппе пациенток из России по применению дидрогестерона с 11-го по 25-й дни для нормализации менструального цикла, были включены 40 пациенток с АМК (длительность менструального цикла менее 21 дня). На фоне применения дидрогестерона в циклическом режиме среднее изменение продолжительности менструального цикла на момент окончания лечения у пациенток с АМК составило +7,8±4,4 дня. Было установлено, что длительность терапии дидрогестероном связана с количеством последующих нормальных менструальных циклов. Анализ показал положительную статистически значимую корреляцию, что говорит в пользу большей эффективности терапии при ее продолжительности не менее 6 месяцев. Помимо нормализации менструального цикла, терапия дидрогестероном была эффективной с точки зрения значимого снижения интенсивности менструальных болей и тревоги как в ходе лечения, так и в течение 6 месяцев последующего наблюдения. Поскольку АМК оказывает существенное влияние на качество жизни женщин, данные результаты особенно значимы [28].
Применение гормональных контрацептивов при АМК возможно с контрацептивной целью у пациенток, не имеющих репродуктивных планов. Известно, что монофазные КОК снижают объем менструальной кровопотери на 40–50%, а КОК, в состав которого входят эстрадиола валерат и диеногест с динамическим режимом дозирования, – до 88% [29]. При применении КОК формируется искусственный менструальный цикл, в котором уровень гормонов (эстрогенов и прогестерона) сохраняется низким в течение всего цикла за счет подавления синтеза эндогенных гормонов, а отторжение эндометрия проявляется менструальноподобной реакцией. Однако ряд нежелательных лекарственных реакций в виде снижения либидо, изменения веса, перепадов настроения могут снижать приверженность пациенток к лечению.
Было показано, что используемые гормональные варианты терапии эффективны в уменьшении частоты АМК [15]. Кроме того, улучшение качества жизни во многом зависит от уровня ферритина [17].
Негормональная терапия
НПВП, которые можно использовать при хроническом АМК, уменьшают количество кровотечений у женщин, однако они не так эффективны, как другие медикаментозные методы лечения. Женщинам с подозрением на нарушение свертываемости крови следует избегать использования НПВП, так как у этих больных, наоборот, кровотечения могут усиливаться.
Транексамовая кислота – антифибринолитическое средство; она показала высокую эффективность во многих исследованиях у взрослых женщин для уменьшения кровотечения по сравнению с плацебо [21].
Фактически пероральная транексамовая кислота так же эффективна для этой цели, как и терапия КОК, в том числе с целью улучшения качества жизни этих пациенток, что является привлекательным вариантом у пациенток с коагулопатией. Данный вид терапии не является патогенетическим и имеет ограничения по длительности приема. Пациенток с нарушением свертываемости крови следует вести совместно с гематологом [14].
АМК, особенно обильные кровотечения, часто приводят к дефициту железа и анемии. В случаях развития железодефицитной анемии показано назначение препаратов железа [10, 14–16].
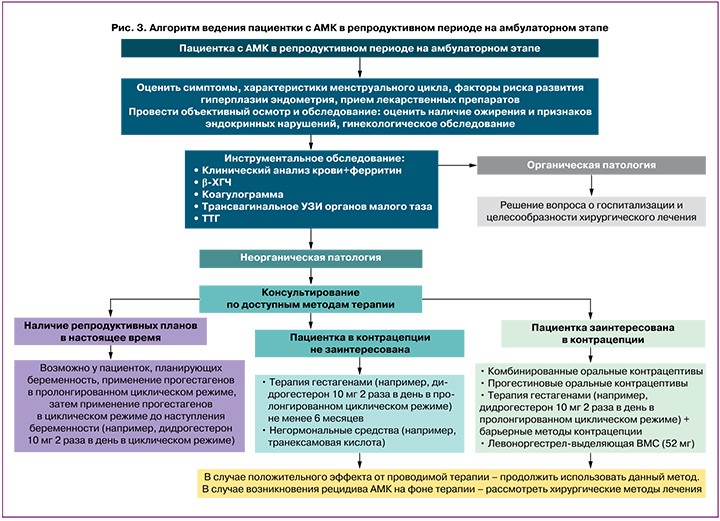
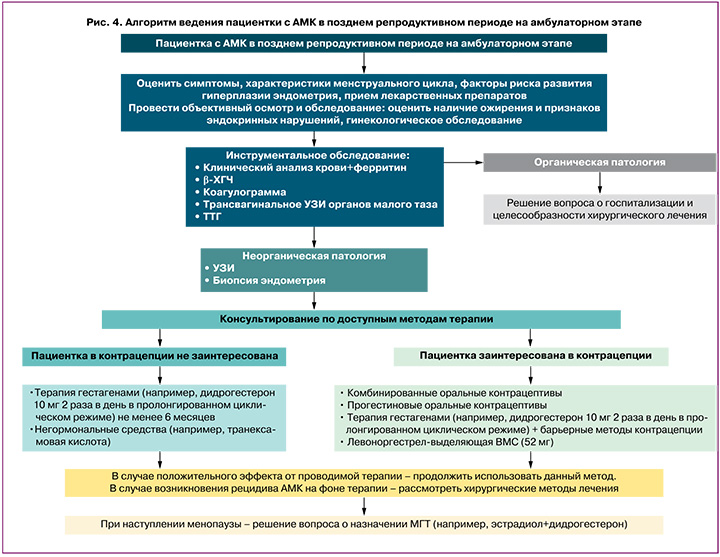
На рисунках 3 и 4 представлены алгоритмы ведения пациенток с АМК в репродуктивном периоде и пациенток в позднем репродуктивном периоде на амбулаторном этапе.
Консультирование пациенток
Высокая частота встречаемости АМК и рецидивов кровотечений в отсутствие поддерживающей терапии после остановки кровотечения диктует необходимость принятия организационных мер. Среди этих мер: информирование женщин, обучение врачей, активное выявление пациентов, своевременная диагностика и назначение лечения, контроль за назначениями, составление регистров женщин, нуждающихся в терапии [3].
Правильное консультирование, а именно – полное информирование пациентки, максимальное вовлечение ее в обсуждение и поддержка в правильности выбора, являются ключевыми факторами, определяющими будущую приверженность конкретному методу терапии. В рамках консультирования врач должен уточнить наличие репродуктивных планов у пациентки, использование контрацептивных средств в настоящее время и ранее, наличие финансовых ограничений.
По результатам консультирования следует принять взвешенное решение совместно с пациенткой, необходима ли контрацепция (и на какой срок) с учетом конкретной клинической ситуации [18]. При необходимости контрацепции адекватная информация от профессионалов об обязательной патогенетической терапии гестагенами перед назначением гормональных методов контрацепции или использованием барьерных методов контрацепции уменьшает частоту обращений и необходимость повторного консультирования в связи с развитием нежелательных явлений на фоне приема КОК [30–32]. Для улучшения качества медицинских услуг по репродуктивному выбору ВОЗ разработала комплекс признанных на международном уровне критериев приемлемости методов контрацепции для мужчин и женщин с учетом медицинских противопоказаний. В 2023 г. в Российской Федерации опубликованы национальные «Медицинские критерии приемлемости методов контрацепции», которые являются актуальным документом при подборе средств предупреждения нежеланной беременности [23].
Еще на этапе стационарного лечения необходимо проговорить с пациенткой, что операция не является заключительным этапом лечения и во избежание рецидивов терапию следует продолжить на амбулаторном этапе на срок не менее 6 месяцев.
С пациенткой необходимо обсудить:
Проблемы и жалобы пациентки. Влияние заболевания на ее социальную жизнь и социально-ролевое функционирование.
Необходимость или желание пациентки сохранить менструальный цикл.
Предшествующий опыт приема гормональных препаратов, иные принимаемые в настоящий момент препараты и наличие сопутствующих заболеваний.
Цели пациентки на конкретном этапе лечения.
Необходимость сохранения фертильности для пациенток, не реализовавших репродуктивные планы.
Возможность индивидуального ведения пациентки на этапе менопаузального перехода и далее в постменопаузе с использованием комбинированной гормональной менопаузальной терапии (в т.ч. и без смены гестагенного компонента).
Длительность терапии. Терапия гестагенами может быть назначена на срок 6 месяцев и более; при этом необходимо оценивать различные профили безопасности гестагенов [1, 22, 33].
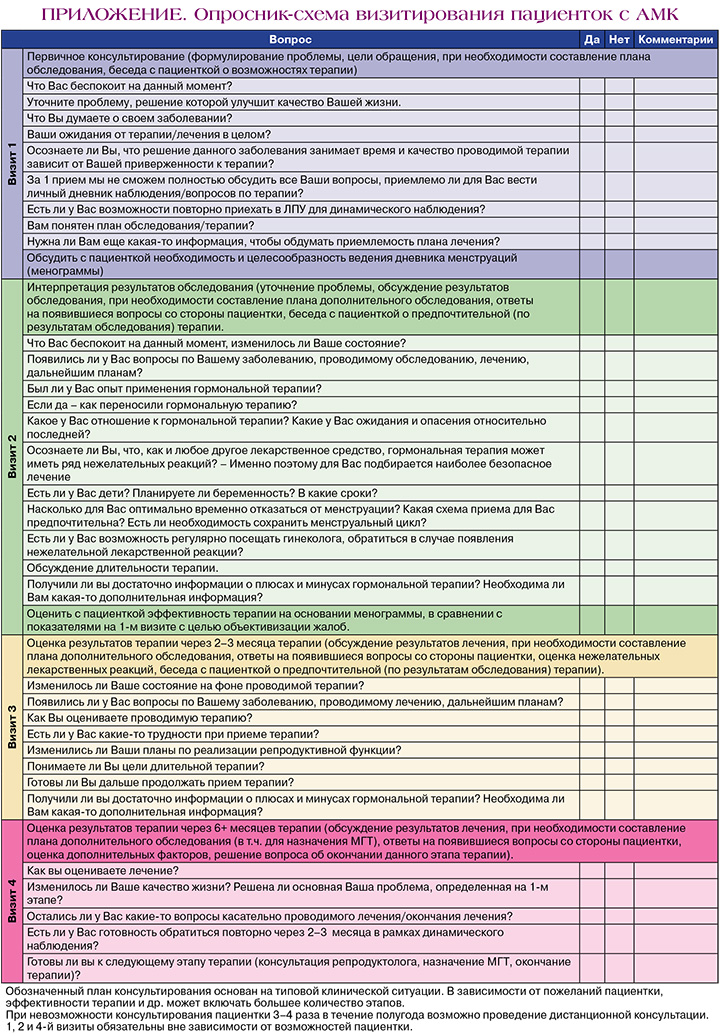
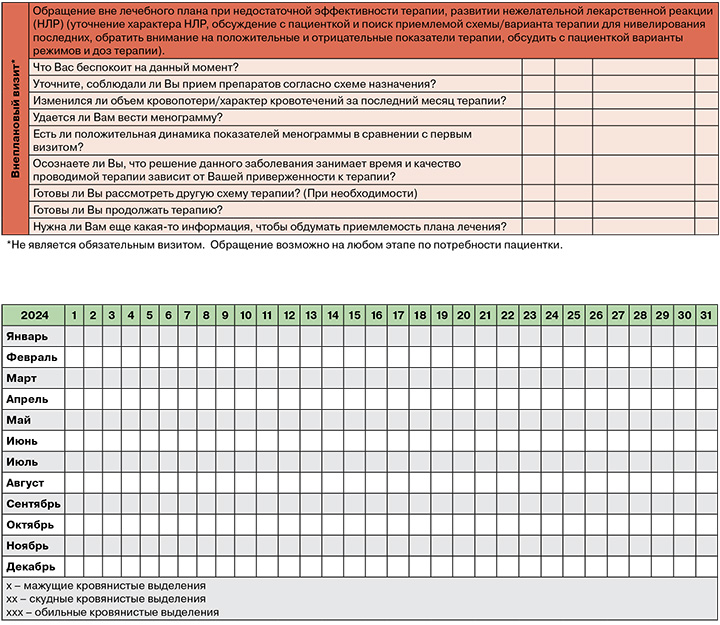
С этой целью был разработан опросник-схема визитирования (Приложение) для обеспечения индивидуального ведения пациенток с АМК, полного консультирования пациенток с данной нозологией и обеспечения высокого уровня приверженности к терапии АМК. Данный аспект является необходимым на пути преодоления высокой частоты рецидивирования АМК.
Заключение
АМК является распространенной жалобой среди женщин, которая затрагивает все возрастные группы и влияет на их состояние как с медицинской точки зрения, так и с точки зрения качества жизни. Таким образом, правильный подход в системе PALM-COEIN важен для постановки точного диагноза; использование в качестве основы физикального обследования, а также применение УЗИ органов малого таза позволяют подтвердить или исключить большинство структурных патологий. Гистероскопия с гистологическим исследованием эндометрия остается наиболее эффективным методом в диагностике и лечении внутриматочной патологии. При исключении органической патологии следующим этапом проводится исключение коагулопатий, эндокринных расстройств и ятрогенных нарушений, которые могут являться причинами АМК.
Необходимым компонентом лечения после исключения злокачественных новообразований является медикаментозная терапия, направленная на достижение длительной ремиссии заболевания.
При назначении гормональной терапии с противорецидивной целью целесообразно во время консультирования пациенток объяснять важность и необходимость выполнения назначений, постоянства приема в течение всего периода лечения и соблюдения режима терапии. Как в диагностике, так и последующей терапии обязательна ориентация на индивидуальные потребности пациентки и ее репродуктивные планы.
В качестве гормональной терапии АМК могут быть рекомендованы гестагенные препараты, способствующие восстановлению физиологического менструального цикла. Среди гестагенов особое место занимает дидрогестерон в силу высокой селективности, хорошего профиля безопасности и возможности персонализации терапии c учетом индивидуальных потребностей пациентки.