Список сокращений
АГ артериальная гипертония
АД артериальное давление
АСБ атеросклеротическая бляшка
ВВА вульвовагинальная атрофия
ВМС внутриматочная система
ВТЭО венозные тромбоэмболические осложнения, включающие ТГВ и/или ТЭЛА
Г гестагены
ГТ гормональная терапия
ГУМС генитоуринарный менопаузальный синдром
ДАД диастолическое артериальное давление
ДГЭА дегидроэпиандростерон (прастерон)
ДИД дидрогестерон
ДРСП дроспиренон
ЖКТ желудочно-кишечный тракт
ЗПА заболевания периферических артерий
Е эстрадиол
ИБС ишемическая болезнь сердца
ИМ инфаркт миокарда
ИМТ индекс массы тела
КОК комбинированные оральные контрацептивы
КЭЭ конъюгированные эквин эстрогены
КС климактерический синдром
ЛНГ левоноргестрел
Лп(а) липопротеин а
ЛС лекарственное средство
МГТ менопаузальная гормональная терапия
МП микронизированный прогестерон
MПA медроксипрогестерона ацетат
МС метаболический синдром
НП неприменимо
НПВП нестероидные противовоспалительные препараты
ОКС острый коронарный синдром
ОНМК острое нарушение мозгового кровообращения
ОР относительный риск
ОХС общий холестерин
ПНЯ преждевременная недостаточность яичников
ПО пероральное введение
ПОАК пероральные антикоагулянты прямого действия
РКИ рандомизированное контролируемое исследование
РМЖ рак молочной железы
САД систолическое артериальное давление
СД сахарный диабет
СПЯ синдром поликистозных яичников
ССЗ сердечно-сосудистые заболевания
СЭ системные эмболии
ТГ триглицериды
ТГВ тромбоз глубоких вен
ТД трансдермальное введение
ТИА транзиторная ишемическая атака
ТПВ тромбоз поверхностных вен (тромбофлебит),
включает тромбоз варикозных и неварикозных поверхностных вен
ТЭЛА тромбоэмболия легочной артерии
ФВ ЛЖ фракция выброса левого желудочка
ФП фибрилляция предсердий
ХБП хроническая болезнь почек
ХС-ЛПВП холестерин липопротеинов высокой плотности
ХС-ЛПНП холестерин липопротеинов низкой плотности
ХСН хроническая сердечная недостаточность
Э эстрогены
НОМА-IR (Homeostasis Model Assessment of Insulin Resistance) индекс инсулинорезистентости
MAGE (mean amplitude of glycemic excursions) средняя амплитуда гликемических экскурсий
Введение
Распоряжением Правительства РФ от 29.12.2022 г. № 4356-р утверждена Национальная стратегия действий в интересах женщин на 2023–2030 гг. Одними из важных задач государственной политики становятся сохранение здоровья женщин всех возрастов, улучшение качества жизни и увеличение периода активного долголетия [1]. Для реализации этой стратегии в здравоохранении крайне важен междисциплинарный подход. Врачам-интернистам совместно с врачами акушерами-гинекологами необходимо выявлять женщин, вступивших в период менопаузального перехода, для своевременного оказания им необходимой помощи.
Климактерические симптомы могут нарушать ход жизни женщин на пике карьеры и семейной жизни: 75% женщин в возрастном периоде 45–55 лет предъявляют жалобы на приливы; в 28,5% случаев это приливы средней или тяжелой степени выраженности; продолжительность симптомов может составлять 3–15 лет [2].
Согласно данным ведущих международных обществ, а также российским клиническим рекомендациям, самым эффективным методом лечения этих проявлений является МГТ [3, 4]. 22 сентября 2025 г. были утверждены и размещены на Рубрикаторе МЗ РФ разработанные РОАГ клинические рекомендации «Менопауза и климактерическое состояние у женщины» [4]. В настоящее время данные клинические рекомендации являются основополагающим документом для врачей всех специальностей, определяющим стратегию ведения пациенток.
Наличие сердечно-сосудистых и метаболических заболеваний само по себе не исключает возможность назначения МГТ с целью купирования климактерических симптомов и улучшения качества жизни. Однако нередко препятствием для использования этого вида гормональной терапии являются опасения врачей, боящихся принести пациенткам больше вреда, чем пользы.
Осторожность особенно важна, когда речь идет о женщинах, страдающих сопутствующими заболеваниями. Более того, следует признать, что качественных исследований относительно безопасности МГТ при основных хронических неинфекционных заболеваниях и часто встречаемых коморбидных состояниях недостаточно.
Таким образом, цель согласительного документа: провести анализ всех доступных в настоящее время данных, полученных в ходе клинических исследований различного дизайна, и создать свод критериев приемлемости назначения МГТ женщинам с сопутствующими сердечно-сосудистыми и метаболическими заболеваниями.
Опираясь на представленный документ, врачи различных специальностей, консультирующие женщин в климактерии, получат доступный алгоритм, позволяющий избегать потенциально опасных ситуаций и обоснованно назначать МГТ в реальной практике.
Раздел 1. Основные определения, симптомы и классификация менопаузы
Менструальный цикл является одним из важнейших показателей здоровья женщины, и его регулярность может меняться в зависимости от стадии репродуктивного старения.
Рабочая группа по изучению стадий старения репродуктивной системы женщин (Stages of Reproductive Aging Workshop, STRAW) [5] выделяет три стадии репродуктивного старения: репродуктивная стадия, менопаузальный переход и постменопауза. Классификация этапов старения репродуктивной системы женщин STRAW+10 представлена на рисунке 1.1.
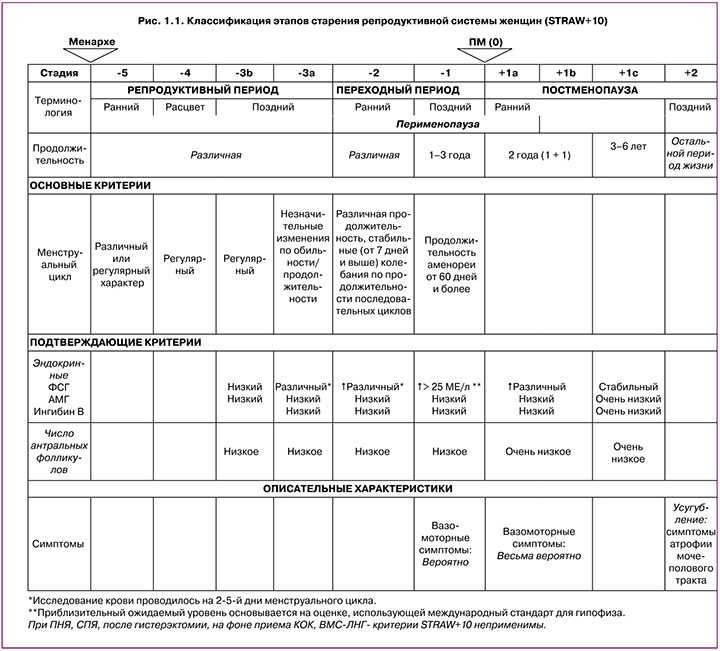
Менопаузальный переход характеризуется нарушением регулярности менструальных циклов, являющимся отражением вариабельности гормональной секреции и овуляторной функции.
Менопауза – стойкое прекращение менструаций, это последняя самостоятельная менструация, обусловленная возрастным снижением гормональной активности и «выключением» репродуктивной функции яичников. Дата наступления менопаузы оценивается ретроспективно: спустя 12 месяцев отсутствия менструации [6, 7].
Перименопауза включает период менопаузального перехода + 1 год после последней менструации.
Перименопауза начинается с нарушения регулярности менструального цикла («фаза менопаузального перехода») и длится до 1 года после полного прекращения менструаций. Эта фаза репродуктивного старения может наступать в широком возрастном диапазоне (от 42 до 58 лет) и длиться до 4–8 лет [8].
Постменопауза – период жизни после последней менструации.
Климактерический синдром – комплекс вегетативно-сосудистых, психических и обменно-эндокринных нарушений, возникающих у женщин на фоне угасания (или резкой потери) гормональной функции яичников и общего старения организма [9].
Средний возраст наступления менопаузы во всем мире составляет 48,8 года (95% ДИ 48,3–49,2) со значительными колебаниями этого показателя в зависимости от географического региона проживания женщин [10], в РФ он находится в диапазоне от 49 до 51 года [9]. Распространенность климактерических симптомов вариативна и зависит от ряда обстоятельств.
Вазомоторные симптомы чаще возникают в позднем периоде менопаузального перехода и особенно выражены в перименопаузе и первые годы постменопаузы [11, 12]. Вазомоторными симптомами страдают до 80% женщин в перименопаузе [13]. Нарушения сна встречаются у 39–47% женщин в перименопаузе и у 35–60% женщин в постменопаузе [14]. Приливы умеренной или тяжелой степени являются дополнительным, специфическим для лиц женского пола маркером риска метаболического и сердечно-сосудистого риска. Наиболее типичная жалоба пациенток с нарушениями сна – частые пробуждения (фрагментация сна). Другими проявлениями являются бессонница, трудности засыпания и ранние пробуждения. Нередко нарушения сна сочетаются с вазомоторными симптомами, а также с повышенной тревожностью, лабильностью настроения.
Среди лиц в возрасте 50 лет и старше в РФ остеопороз выявляется у 34% женщин, а частота остеопении составляет 43% [15].
Вазомоторные симптомы и другие проявления климактерического синдрома не только ухудшают качество жизни женщин и ограничивают их функциональные возможности, но и ассоциированы с повышением риска развития ИБС в 1,34 раза, риска любых ССЗ – в 1,48 раза [16].
У 15% женщин в перименопаузе и до 80% женщин в постменопаузе отмечаются симптомы ГУМС или ВВА [17]. Сухость влагалища, зуд и диспареуния (болезненность при половом акте) являются симптомами, связанными с ВВА. У 41% женщин в возрасте 50–79 лет есть хотя бы один из симптомов ВВА. Распространенность нарушений мочеиспускания (внезапное и непреодолимое желание помочиться, которое невозможно отсрочить, недержание мочи) у женщин зависит от длительности постменопаузы и увеличивается с 15,5% при постменопаузе до 5 лет и до 41,4% при длительности постменопаузы более 20 лет [17].
Классификация менопаузы
По времени наступления выделяют:
1. преждевременную менопаузу или преждевременную недостаточность яичников (до 40 лет);
2. раннюю (40–44 лет);
3. своевременную (45–55 лет);
4. позднюю (старше 55 лет).
По причине наступления выделяют естественную и ятрогенную (в том числе хирургическую менопаузу).
Раздел 2. Показания и противопоказания к МГТ
Показания и противопоказания к назначению МГТ определяются актуальными Клиническими рекомендациями и инструкциями к конкретным препаратам.
Показания к назначению МГТ [4]
- Лечение вазомоторных симптомов умеренной и тяжелой степени, существенно снижающих качество жизни.
- Лечение симптомов ГУМС, сексуальной дисфункции.
- Профилактика постменопаузального остеопороза.
- Восполнение дефицита эстрогенов при ПНЯ и ранней менопаузе; при двусторонней овариоэктомии.
Противопоказания к назначению МГТ [4]
- Кровотечение из половых путей неясного генеза.
- РМЖ (диагностированный, подозреваемый или в анамнезе).
- Диагностированные или подозреваемые эстрогензависимые злокачественные новообразования (эндометрия, яичников, матки).
- Острые и хронические заболевания печени в настоящее время или в анамнезе (до нормализации функциональных проб печени), в том числе злокачественные опухоли печени.
- Тромбозы (артериальные и венозные) и эмболии в настоящее время.
- ИМ.
- Ишемические или геморрагические цереброваскулярные нарушения.
- Наличие миомы матки с субмукозным расположением узла.
- Наличие полипа эндометрия.
- Аллергия к компонентам МГТ.
- Кожная порфирия (для эстрогенного компонента).
- Прогестагензависимые новообразования (например, менингиома) (для гестагенов).
Раздел 3. Виды МГТ и основные принципы ее назначения
Монотерапия гестагенами
Женщинам в периоде менопаузального перехода с целью профилактики гиперпластических процессов эндометрия и регуляции менструального цикла показано применение гестагенов в циклическом режиме на срок не менее 10–14 дней. В таблице 3.1 представлены зарегистрированные на территории РФ препараты для монотерапии гестагенами c целью регуляции менструального цикла и профилактики гиперпластических процессов эндометрия.

Системная МГТ
Системная МГТ является наиболее эффективным методом лечения вазомоторных симптомов и других климактерических проявлений. Большинство лекарственных препаратов МГТ одобрены для профилактики постменопаузального остеопороза, за исключением ультранизкодозированных форм.
В таблице 3.2 представлены зарегистрированные на территории РФ препараты для системной МГТ.
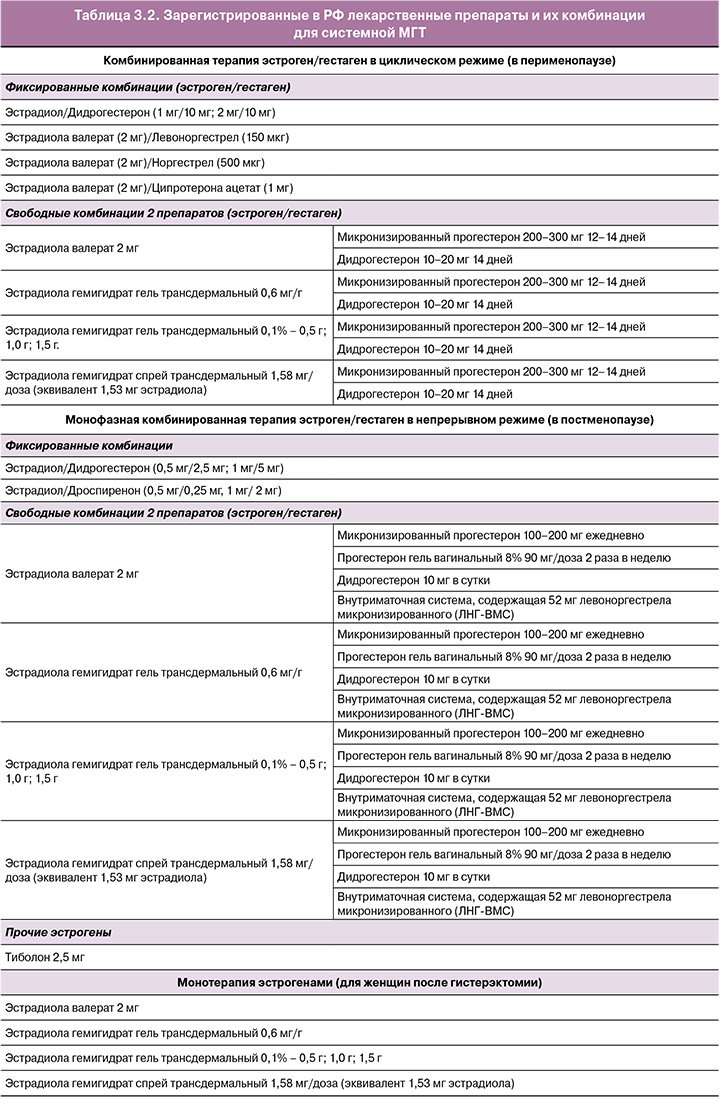
Локальная МГТ
Локальная терапия эстрогенами
Локальная терапия эстрогенами (эстриолом) используется у женщин перии постменопаузального периода с жалобами только на симптомы ГУМС: сухость влагалища, диспареунию или дискомфорт при половой жизни, мочевые симптомы (императивные и/или частые позывы на мочеиспускание, дизурия, рекуррентные инфекции мочевыводящих путей), связанные с этим состоянием [18].
При назначении локальных эстрогенов отсутствуют ограничения по возрасту и длительности постменопаузы. При недостаточном эффекте системной МГТ на симптомы ГУМС возможно дополнительное назначение локальных эстрогенов [19].
Эффективность локального эстриола 0,5 мг в лечении симптомов ГУМС/ВВА доказана в ходе РКИ и систематических обзоров [20].
Длительные наблюдения (6–24 месяцев) показывают отсутствие влияния локальных эстрогенов на эндометрий, поэтому не требуется дополнительного использования прогестагенов. Локальные эстрогены не повышают риск ВТЭО, РМЖ, ССЗ, гиперплазии и рака эндометрия по данным наблюдательных исследований [21].
В таблице 3.3 представлены зарегистрированные на территории РФ препараты для локальной МГТ.
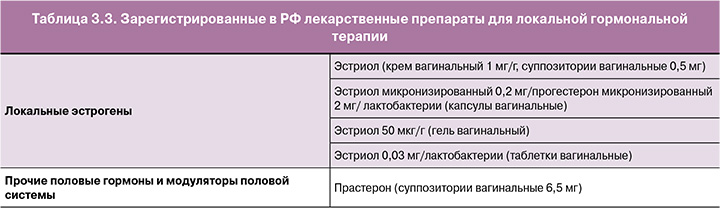
После отмены локальных эстрогенов симптомы ГУМС возобновляются, что обосновывает необходимость длительного применения [22].
Локальная терапия прастероном
Прастерон (ДГЭА) – эндогенное вещество стероидной природы, которое метаболизируется в андрогены и эстрогены только в клетках мочеполового тракта при местном применении. Прастерон имеет минимальный уровень абсорбции. При его применении сохраняются уровни эстрогенов в крови, соответствующие постменопаузальным значениям [23–27].
Основные принципы назначения МГТ
1. Начало системной МГТ необходимо рассматривать у женщин в возрасте менее 60 лет и с длительностью постменопаузы менее 10 лет. Оптимальное время для старта МГТ – период перии ранней постменопаузы. Отсутствуют возрастные ограничения при назначении локальной терапии эстрогенами (эстриолом) симптомов ГУМС.
2. Терапевтическая цель должна заключаться в использовании наиболее подходящей минимальной эффективной дозы МГТ в соответствии с целями лечения.
3. Индивидуализация МГТ проводится с учетом факторов риска РМЖ, ССЗ, остеопороза и переломов. Выбор дозы и лекарственной формы препарата, его состава, режима использования проводят с учетом возраста пациентки, стадии репродуктивного старения, гинекологических заболеваний (ПНЯ (первичная/ вторичная), СПЯ, наличие интактной матки/ гистерэктомии, эндометриоз), коморбидных состояний, ее предпочтений и потребностей.
4. Наличие показаний к назначению МГТ и отсутствие противопоказаний.
5. Применение системной МГТ требует периодической коррекции дозировок в зависимости от стадии репродуктивного старения, возраста, эффективности и переносимости лечения. По мере увеличения возраста пациентки и длительности постменопаузы целесообразно снижать дозу МГТ.
6. Мониторинг лечения и регулярная (не реже 1 раз в год) переоценка польза/риск. Длительность терапии определяется целью терапии и балансом польза/риск.
При выборе МГТ учитывается профиль безопасности составляющих компонентов. Персонифицировать дозировку МГТ с учетом факторов риска со стороны пациентки (ССЗ, риск РМЖ, риск остеопороза, коморбидные состояния и проч.) позволяет подбор минимальной эффективной дозировки и способа доставки лекарственных препаратов [14, 15].
Назначение, коррекция или отмена МГТ, а также динамический контроль за эффективностью и переносимостью лечения находятся в зоне ответственности врача акушера-гинеколога.
Раздел 4. МГТ у пациенток с ожирением, метаболическими нарушениями и нарушениями углеводного обмена
Согласно имеющимся научным данным, период естественного менопаузального перехода сопровождается постепенным формированием дефицита прогестерона, далее, в период ранней постменопаузы, уровни эстрогенов и прогестерона резко снижаются [28, 29].
Эстрогены играют важную роль в биологии жировой ткани: снижают число рецепторов к андрогенам в висцеральной жировой ткани, препятствуют распределению жировой ткани по висцеральному типу, благоприятно действуют на нейроэндокринный контроль пищевого поведения. Эстрадиол обеспечивает гомеостаз, участвует в регуляции утилизации и сохранения энергии; его дефицит постепенно приводит к развитию менопаузального метаболического синдрома (ММС) [30].
Выраженное снижение концентрации эстрогенов, сопровождающееся формированием относительной гиперандрогении у части женщин, рассматривается как основной фактор, вызывающий увеличение веса и перераспределение жира в организме у женщин в постменопаузе [31].
При этом выработка андрогенов надпочечниками не меняется, а в яичниках сохраняется продукция андрогенов тека-клетками. Вместе с тем, вслед за снижением выработки эстрогенов яичниками, снижается уровень глобулина, связывающего половые гормоны (ГСПГ), что закономерно приводит к увеличению индекса свободных андрогенов. Также у женщин в постменопаузе происходит увеличение синтеза андрогенов в периферических тканях внутри клетки в соответствии с концепцией интракринологии. Это способствует формированию физиологического сдвига в сторону относительного преобладания андрогенов над эстрогенами в ранней постменопаузе, при этом уровень тестостерона остается в пределах референсных значений [29, 32–34].
В крупном исследовании SWAN (Study of Women’s Health Across the Nation) было установлено, что изменение соотношения уровня эстрогенов и андрогенов в период менопаузального перехода, а не динамика их абсолютных значений является предиктором формирования МС у женщин в дальнейшем [35].
Относительная гиперандрогения тесно связана с метаболическими нарушениями, включая резистентность к инсулину. Инсулин стимулирует синтез андрогенов и, кроме того, способен подавлять выработку ГСПГ в печени, что приводит к повышению уровней как общего, так и свободного тестостерона. Гиперандрогения, в свою очередь, способствует развитию инсулинорезистентности и висцерального ожирения. Сформировавшийся таким образом порочный круг причинно-следственных нарушений с течением времени может усугублять клинические симптомы гиперандрогении и резистентности к инсулину [29, 36–41].
Инсулинорезистентность, дислипидемия, артериальная гипертензия и абдоминальное ожирение – основные маркеры ММС [42]. По сравнению с репродуктивным периодом женщины в период перименопаузы и ранней постменопаузы подвержены более высокому риску прогрессирования инсулинорезистентности [43].
Нарушение секреции инсулина и инсулинорезистентность признаны ключевыми патогенетическими механизмами формирования СД 2 типа (СД2). В свою очередь, СД2 и МС являются значимыми факторами риска развития атеросклеротических ССЗ и приводят к увеличению смертности от них [29, 44–46]. С возрастом риск развития МС увеличивается у женщин в 5 раз. Распространенность ССЗ повышается у женщин с нарушениями углеводного обмена в 5 раз [47].
Снижение уровня эстрогенов у женщин с наступлением менопаузы сопровождается изменением регуляции энергетического гомеостаза, что приводит к избыточному накоплению жировой ткани [48, 49]. Ожирение, особенно абдоминальное, тесно ассоциировано с МС и значительно повышает кардиометаболический риск, что отражается на прогнозе и продолжительности жизни женщин [50].
Помимо дефицита эстрогенов, относительная гиперандрогения и активация минералокортикоидных рецепторов в постменопаузе способствуют формированию висцерального ожирения, которое первоначально может носить скрытый характер в случае сохранения нормальной массы тела [29, 51]. В свою очередь, ожирение является основным фактором риска ряда других хронических заболеваний, включая СД2 и ССЗ. Женщины с ИМТ ≥24,9 кг/м2 имеют более высокий риск развития СД2, а риск смертности от ССЗ у них в 4 раза выше, чем у женщин с нормальным ИМТ [29, 37–41, 52–56].
Ожирение является независимым фактором риска развития ВТЭО. В рандомизированном исследовании «Инициатива во имя здоровья женщин» (WHI) у женщин с ожирением (ИМТ >30 кг/м2) было отмечено 3-кратное увеличение риска ВТЭО по сравнении с женщинами с нормальным ИМТ даже в группе плацебо [57].
Для практикующего врача важное значение имеет не только лечение пациентов с уже сформировавшимися метаболическими и ССЗ, но и их первичная профилактика. Важным аспектом является снижение рисков развития и обратимость ММС при своевременной модификации образа жизни, контроле/ снижении массы тела, а также вовремя начатой патогенетически обоснованной терапии.
При ожирении нежелательно назначать препараты, содержащие гестагены с остаточной андрогенной и глюкокортикоидной активностью, предпочтение отдается метаболически нейтральным прогестагенам [58]. После обнаружения связи минералокортикоидных рецепторов с дифференциацией жировой ткани установлена потенциальная роль прогестерона и прогестинов с антиминералокортикоидными свойствами в контроле массы тела и пролиферации жировой ткани [59].
На фоне снижения уровней эстрогенов у некоторых женщин возможно развитие абдоминального ожирения и повышение рисков метаболических нарушений, сердечно-сосудистых осложнений, а также относительной гиперандрогении, которая сопровождается появлением поздних акне, алопеции, гирсутизма [4, 180].
Гиперандрогения не является состоянием, требующим коррекции путем назначения МГТ [181]. Данный вид терапии не должен рассматриваться как стратегия лечения гиперандрогенных состояний. В случае развития гирсутизма или акне в период менопаузы необходимо исключить такие патологии как стромальная гиперплазия яичников, гормонпродуцирующая опухоль яичников или надпочечников, врожденная гиперплазия коры надпочечников, синдром Иценко–Кушинга, образования щитовидной железы. При выраженных признаках гиперандрогении необходимо углубленное исследование для уточнения причины и назначения патогенетической терапии. При наличии подозрений на вышеупомянутые состояния целесообразно направить пациентку к эндокринологу для дифференциальной диагностики причин гиперандрогенного состояния и назначения патогенетически обоснованной терапии [4, 181]. Изолированные акне без гирсутизма (acne tarda) могут быть не связаны с гиперандрогенией.
Частота СД2 в популяции женщин составляет: в 40–44 года – 1,2%, в 45–49 лет – 2,4%, в 50–54 года – 4,2%, в 55–59 лет – 9,4% [60].
Своевременный старт применения МГТ может отложить риск развития СД2.
По данным метаанализа 107 исследований, МГТ снижает риск развития СД2 на 30% (ОР=0,7; 95% ДИ 0,6–0,9), а при уже имеющемся СД на фоне МГТ происходит снижение гликемии и HOMA-IR, а также наблюдается улучшение липидного профиля и снижение АД, наряду со снижением степени абдоминального ожирения. На фоне монотерапии эстрогенами или комбинированной МГТ у женщин с СД2 не было отмечено увеличения риска сердечно-сосудистой смертности [61].
При СД2 может быть назначен любой вид МГТ при отсутствии противопоказаний. При назначении комбинированной МГТ важно учитывать метаболические эффекты гестагена, входящего в состав комбинированной МГТ: следует остановить выбор на прогестагенах с нейтральным воздействием на метаболические процессы (микронизированный прогестерон, дроспиренон, дидрогестерон) [62].
Благоприятный эффект МГТ на углеводный обмен прекращается при отмене терапии.
Совместимость сахароснижающей терапии с МГТ, заместительной терапией левотироксином натрия (L-T4), тиреостатической и дофаминергической терапией с учетом путей введения отражена в таблице 4.1 [63].
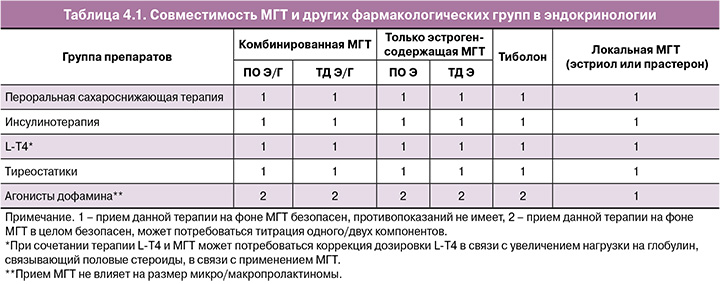
Заболевания ЖКТ, связанные с нарушением всасывания, у пациенток с метаболическим синдромом
Снижение уровней эстрогенов и прогестерона в постменопаузе может быть ассоциировано с прогрессированием заболеваний ЖКТ и усугублять риск развития мальабсорбционных состояний, особенно у пациенток с метаболическими нарушениями [64].
Синдром нарушенного всасывания (мальабсорбция) возникает вследствие дисфункции тонкого кишечника, поджелудочной железы с нарушением ее внешнесекреторной функции, заболеваний желчного пузыря [65]. При хронических воспалительных заболеваниях ЖКТ нарушаются процессы всасывания и конъюгации эстрогенов, ухудшается моторика ЖКТ, нарушается секреция желчных кислот, усиливается развитие жировой дистрофии печени, повышается риск формирования камней в желчном пузыре [66, 67].
При наличии заболеваний ЖКТ, таких как врожденный дефицит лактазы, непереносимость лактозы, глюкозо-галактозная мальабсорбция следует использовать трансдермальные формы эстрогенов [4, 68].
Ключевые положения
- На фоне дефицита прогестерона и эстрогенов в период ранней постменопаузы, при продолжающейся выработке андрогенов в яичниках и надпочечниках происходит формирование физиологического сдвига в сторону относительного преобладания андрогенов в ранней постменопаузе. При этом абсолютные значения тестостерона соответствуют референсным для стадии репродуктивного старения.
- Физиологический сдвиг в сторону относительного преобладания андрогенов в постменопаузе ассоциирован с увеличением последующего риска развития метаболических и ССЗ, СД2.
- При отсутствии гиперандрогении МГТ с антиандрогенным эффектом нецелесообразна.
- При выраженных признаках гиперандрогении необходимо направление к эндокринологу для уточнения причины и назначения патогенетической терапии. При наличии клинических признаков гиперандрогении целесообразно добиваться антиандрогенного эффекта.
- Следует учитывать, что эстрогены обладают уникальной кардиопротективной ролью и их прогрессирующее снижение ассоциировано с повышением риска сердечно-сосудистых событий.
- МГТ оказывает благоприятный эффект на композиционный состав тела за счет уменьшения висцерального ожирения.
- Совместно с применением МГТ у женщин с ожирением рекомендуется проводить образовательные беседы с целью коррекции привычного образа жизни и снижения массы тела.
- У женщин с сохраненной маткой следует остановить выбор на прогестагенах с нейтральным воздействием на метаболические процессы.
- Своевременно начатая МГТ может отсрочить развитие СД2.
- Пациенткам с СД2 может быть назначена МГТ. Выбор режима, состава и пути введения МГТ осуществляется на основе персонифицированного подхода.
- МГТ имеет положительный эффект на гликемический профиль как у женщин без СД, так и у женщин с СД2.
Раздел 5. МГТ у пациенток с тромбофилиями, заболеваниями вен, венозными эмболиями
5.1. Состав МГТ и риск венозных тромбоэмболических осложнений
Считается, что МГТ с использованием в ее составе пероральных эстрогенов повышает риск ВТЭО – ТГВ и ТЭЛА [69]. Однако этот эффект, отмеченный в РКИ и выполненных на их основе метаанализах, может быть во многом связан с назначением достаточно «тромбогенных» препаратов на основе КЭЭ и МПА, а также с несвоевременным началом МГТ [70].
Так, по данным ретроспективного анализа баз данных QResearch и CPRD, выполненного с использованием метода «случай-контроль», назначение комбинированной МГТ КЭЭ в сочетании с МПА ассоциировалось с наиболее высоким риском ВТЭО. Для перорального эстрадиола было отмечено достоверное повышение риска ВТЭО и этот эффект был дозозависимым. В то же время, для комбинации перорального эстрадиола с дидрогестероном риск ВТЭО не увеличивался вне зависимости от режима и дозы эстрадиола. Назначение трансдермального эстрадиола не было связано с увеличением риска ВТЭО как при монотерапии, так и в составе комбинированной МГТ. Вне зависимости от ИМТ назначение комбинации перорального эстрадиола с дидрогестероном, трансдермального эстрадиола как в монотерапии, так и в комбинации с гестагеном, не было связано с увеличением риска ВТЭО. В когорте женщин, имевших в анамнезе эпизоды ВТЭО и/или получающих терапию антикоагулянтами, отмечено достоверное снижение риска ВТЭО при назначении трансдермального эстрадиола в монорежиме, а также отсутствие увеличения риска ВТЭО при комбинированном использовании трансдермального эстрадиола с гестагеном и перорального эстрадиола с дидрогестероном [71].
По данным наблюдательных исследований, на фоне применения трансдермального эстрадиола как в низких (<50 мкг/сут), так и в более высоких дозах в монорежиме, а также его сочетания с любым гестагеном в циклическом или непрерывном режимах, риск ВТЭО не увеличивался [71–74].
Надлежащие РКИ или иные клинические исследования по сопоставлению этих подходов пока отсутствуют.
В наблюдательном исследовании EURAS-HRT (более 30 000 женщин) был подтвержден долгосрочный профиль безопасности дроспиренонсодержащих препаратов для МГТ в отношении ВТЭО. Риск ВТЭО на фоне МГТ с дроспиреноном был сопоставим, а риск серьезных артериальных тромбоэмболических событий (главным образом острого инфаркта миокарда и ишемического инсульта) был достоверно ниже, чем при приеме другой МГТ (детального сопоставления по составу и особенностям другой МГТ не проводилось) [75]. По имеющимся на сегодняшний день данным, применение трансдермальных эстрогенов не ассоциировано с повышенным риском ВТЭО. У женщин с факторами риска ВТЭ использование трансдермальных эстрогенов не повышало риск ВТЭ [76]. Следует отметить, что в ретроспективном исследовании Vinogradova Y. et al. (2019) авторы указали на недостаточность данных для оценки современных препаратов для МГТ (эстрадиол с дроспиреноном, эстрадиол с норгестрелом или левоноргестрелом) и их сравнения с трансдермальной терапией. Исследования, показавшие, по мнению авторов, более высокий риск ВТЭО при применении пероральных препаратов в сравнении трансдермальными, относятся к периоду до 2012 г. В последнем систематическом обзоре по данной теме Goldstajn M.S. et al. (2023) авторы отмечают, что данные, сравнивающие трансдермальный и пероральный способы введения МГТ, ограничены и имеют низкое качество, что требует проведения дополнительных исследований [72]. В рекомендациях The North American Menopause Society (2022) также отмечается, что на сегодняшний день неизвестно, связан ли непероральный путь применения препаратов МГТ с более низким риском ВТЭО, РМЖ и сердечно-сосудистых осложнений, при этом выбор прогестагена также может повлиять на риск развития ВТЭО [68].
В целом современная низкодозированная и ультранизкодозированная комбинированная пероральная МГТ с использованием эстрадиола представляется безопасной в отношении ВТЭО и по риску венозных тромбозов сопоставимой с трансдермальной МГТ [68, 71]. Однако оценка пользы и риска назначения МГТ, выбор лекарственного препарата, его состава, и пути введения должны проводиться индивидуально, с учетом особенностей клинической картины и наличия факторов риска ВТЭО.
По данным ретроспективного анализа баз данных QResearch и CPRD, выполненного с использованием метода «случай-контроль», не было отмечено увеличения риска ВТЭО для тиболона [71].
Локальная терапия эстрадиолом симптомов ГУМС и прастероном (ДГЭА) симптомов ВВА не приводит к увеличению риска венозных тромбозов и может использоваться у всех категорий пациенток [63, 77]. ЛНГ-ВМС, содержащая 52 мг микронизированного левоноргестрела, также может быть использована как компонент МГТ. По данным исследований, применение ЛНГ-ВМС не приводило к повышению риска ВТЭО [78, 79].
При принятии решения о возможности и составе МГТ следует учитывать, что риск ВТЭО нельзя рассматривать отдельно от других тромботических рисков. Так что даже в случаях, когда не исключено некоторое повышение риска ВТЭО, этот эффект может нивелироваться снижением частоты артериальных тромбозов и других сердечно-сосудистых осложнений, что в итоге обеспечит нейтральное или положительное воздействие на смертность [69, 79, 80].
Ключевые положения
- Современная трансдермальная, содержащая эстрадиол, как в монорежиме, так и в комбинации с гестагеном, а также низкодозированная и ультранизкодозированная комбинированная пероральная МГТ с использованием эстрадиола безопасна в отношении ВТЭО.
- МГТ обеспечивает положительный баланс между снижением и повышением рисков различных тромботических событий в пользу снижения частоты сердечно-сосудистых осложнений, что обеспечивает нейтральное или положительное воздействие на смертность.
5.2. МГТ в различных клинических ситуациях, связанных с тромбозами
Венозные тромбозы
При остром ТГВ и/или ТЭЛА МГТ противопоказана.
Большинство экспертов рекомендуют отказаться от МГТ и у пациенток с ВТЭО в анамнезе [63, 81, 82]. Есть свидетельства отсутствия увеличения риска рецидива ВТЭО при трансдермальной МГТ на фоне лечения антикоагулянтами, однако данные о безопасности такого подхода после ВТЭО ограничены [74, 76].
При тяжелых менопаузальных симптомах помимо локального применения эстрогенов возможно применение минимальной эффективной дозы трансдермального эстрадиола (<50 мкг/сут). Не исключается возможность применения ультранизкодозированной (0,5 мг эстрадиола) пероральной комбинированной МГТ при соответствующей антикоагулянтной терапии [73, 74, 81, 82]. Также не исключено, что современная МГТ достаточно безопасна после планового прекращения использования антикоагулянтов у отдельных категорий больных с низким риском рецидива венозных тромбозов [74].
Имеющиеся данные не позволяют однозначно судить о риске МГТ при остром ТПВ и ТПВ в анамнезе [83]. Решение о возможности применения современной пероральной и трансдермальной МГТ при ТПВ должно приниматься индивидуально, с учетом особенностей клинической ситуации, наличия факторов риска ВТЭО, а также наличия ТПВ в анамнезе как противопоказания к применению в инструкции к конкретному препарату.
В исследованиях по оценке риска ТГВ и/или ТЭЛА после перенесенного ТПВ не проводится разделение между тромбозом неварикозных и тромбозом варикозных поверхностных вен (варикотромбофлебитом). Варикотромбофлебит, в первую очередь, обусловлен наличием варикозного расширения вен, которое может быть устранено задолго до назначения МГТ.
Варикотромбофлебит в анамнезе следует считать ограничением для назначения МГТ при прямом указании на ТПВ в анамнезе как на противопоказание к применению в инструкции к конкретному препарату для МГТ.
Варикозное расширение вен. Наличие варикозного расширения вен не является противопоказанием к МГТ и не должно влиять на принятие решения о назначении МГТ. На сегодняшний день нет данных, что МГТ увеличивает риск развития тромбоза варикозно измененных вен (варикотромбофлебита). Проведение ультразвукового исследования вен нижних конечностей перед назначением МГТ не требуется.
Тромбофилии. Данных о безопасности МГТ при антифосфолипидном синдроме очень мало [76]. Из-за высокого риска венозных и/или артериальных тромбозов пероральная и трансдермальная МГТ у больных с антифосфолипидным синдромом не рекомендуется. Потенциально ее возможность не исключена у женщин с невысокой активностью заболевания или бессимптомными изменениями отдельных лабораторных показателей, не имеющих дополнительных факторов риска тромбозов [83].
Данные о безопасности МГТ при бессимптомных тромбофилиях ограничены. В некоторых исследованиях установлен повышенный риск развития ВТЭО при пероральной МГТ на фоне ряда тромбофилий (дефицит протеина С, дефицит протеина S, дефицит антитромбина, фактор V Лейден, мутация гена протромбина G20210A, высокий уровень фактора свертывания крови VIII) [84, 85]. Однако этого недостаточно для однозначного запрета на проведение пероральной МГТ на фоне бессимптомной тромбофилии, требуются дополнительные исследования данного вопроса.
Трансдермальные эстрогены не имеют дополнительного риска для женщин-носителей генов протромботических мутаций (полиморфизмов фактора V Лейден и гена протромбина G20210A) [76, 84, 85]. Решение о возможности назначения и составе МГТ следует принимать индивидуально с учетом сведений о наличии ранее выявленной бессимптомной тромбофилии, тяжести менопаузальных симптомов, наличия дополнительных факторов риска ВТЭО, а также указания определенных тромбофилий в перечне противопоказаний в инструкции к конкретному препарату для МГТ [68, 74]. Обследование на наличие тромбофилий перед началом МГТ не рекомендуется.
Семейный анамнез тромбозов (венозный или артериальный тромбоз у родственников 1 степени родства в возрасте до 50 лет) указывает на повышенный риск ВТЭО, однако не является основанием для запрета МГТ [17, 68]. В рекомендациях NAMS (2022) и согласительном документе MHT Eligibility Criteria Group (2022) нет ограничений по семейному анамнезу в отношении какой бы то ни было формы МГТ [63, 68].
В рекомендациях ASH (2023) в вопросе принятия решения о возможности назначения МГТ выделяются тромбофилии высокого риска развития ВТЭО (дефицит протеинов С, S или антитромбина), рассматриваются сценарии необходимости тестирования на указанные тромбофилии и рекомендуется воздержаться от назначения МГТ при их выявлении [86].
Для пациентки, имеющей родственников 1 или 2 степени с лабораторно подтвержденным дефицитом протеинов С, S или антитромбина, целесообразно проведение анализа на установленную в семье тромбофилию. При подтверждении наличия этих тромбофилий у обследуемой следует воздержаться от назначения эстроген-содержащих препаратов. При исключении этих тромбофилий противопоказаний к проведению какой бы то ни было МГТ нет.
Для пациентки с семейным анамнезом тромбозов, при отсутствии в личном анамнезе ситуаций повышенного риска развития ВТЭО, связанных с изменением баланса женских половых гормонов (беременность, прием КОК), целесообразно тестирование на дефицит протеинов С, S и антитромбина для принятия решения о возможности проведения МГТ. При выявлении этих тромбофилий следует воздержаться от назначения эстроген-содержащих препаратов. При исключении этих тромбофилий противопоказаний к проведению какой бы то ни было МГТ нет. Принятие решения о целесообразности тестирования является прерогативой лечащего врача.
По имеющимся данным трансдермальная МГТ не увеличивает риск ВТЭО у женщин с бессимптомной тромбофилией, однако свидетельства в пользу ее безопасности в этой клинической ситуации ограничены [74, 76, 84].
Ограничением для применения конкретного препарата является указание на семейный тромботический анамнез и/или наличие определенных тромбофилий как противопоказание к применению в инструкции.
Ключевые положения
- Хронические заболевания вен, в том числе варикозное расширение вен нижних конечностей, не являются противопоказанием или ограничением для проведения МГТ.
- Абсолютным противопоказанием к проведению пероральной комбинированной МГТ является острый ТГВ или ТЭЛА.
- Семейный анамнез тромбозов не является противопоказанием к проведению МГТ. Наличие семейного анамнеза тромбозов может быть основанием для проведения тестирования на дефициты протеинов С, S и антитромбина. Принятие решения о целесообразности тестирования является прерогативой лечащего врача.
- Наличие бессимптомной тромбофилии (без тромботического события в личном анамнезе), за исключением дефицита протеинов С, S и антитромбина, не является противопоказанием к проведению МГТ.
5.3. МГТ при хирургических вмешательствах и госпитализации с острым нехирургическим заболеванием
В настоящее время нет доказательств пользы от отмены МГТ перед хирургическими вмешательствами или при госпитализации по поводу острого нехирургического заболевания (кроме тех, при которых МГТ противопоказана) [87].
При стратификации риска ВТЭО у подобных больных с помощью соответствующих шкал (например, шкала Каприни для оценки риска послеоперационных ВТЭО, шкалы Падуа (Padua) или IMPROVE VTE у госпитализированных нехирургических пациентов) продолжение МГТ рекомендуется рассматривать как дополнительный фактор риска ВТЭО. Тромбопрофилактика проводится в соответствии с рассчитанным риском и, при необходимости, обеспечивается назначением антикоагулянтов, которые полностью нивелируют протромботический эффект гормональных препаратов. Отмена МГТ при хирургических вмешательствах не требуется.
Ключевые положения
- При госпитализации по поводу острого нехирургического заболевания или при проведении планового или экстренного хирургического вмешательства отмена МГТ не требуется.
Раздел 6. МГТ у пациенток с атеросклеротическими сердечно-сосудистыми заболеваниями
В 1998 г. исследование HERS, первое рандомизированное плацебо-контролируемое исследование ГТ эстрогенами и прогестином для вторичной профилактики ИБС среди женщин в постменопаузе с установленной ИБС, не выявило пользы в отношении развития сердечно-сосудистых осложнений и общей смертности при использовании ГТ. Результаты этого исследования являются аргументом против начала ГТ для вторичной профилактики ИБС [88].
Более поздний метаанализ 19 РКИ с участием 40 410 женщин в постменопаузе, получавших МГТ, не выявил значительного увеличения смертности от всех причин, смертности от ССЗ или ИМ на фоне МГТ как в рамках первичной, так и в рамках вторичной профилактики сердечно-сосудистых осложнений. Анализ подгрупп, основанный на сроках начала МГТ, показал [70]:
- у женщин, начавших МГТ в течение 10 лет после менопаузы, была более низкая смертность (ОР=0,70; 95% ДИ 0,52–0,95) и меньшее количество сердечно-сосудистых событий (комбинация сердечно-сосудистой смерти и несмертельного ИМ) (ОР=0,52; 95% ДИ 0,29–0,96).
- у женщин, начавших МГТ >10 лет от начала менопаузы, риск инсульта повышался без какого-либо влияния на смертность или другие исходы ССЗ.
Сравнительных исследований в отношении безопасности тех или иных видов МГТ очень немного. В наблюдательном исследовании EURAS-HRT (более 30 000 женщин) при приеме МГТ с дроспиреноном риск острого ИМ и ишемического инсульта был достоверно ниже, чем при приеме другой МГТ. Однако детального сопоставления по составу и путям введения МГТ не проводилось [75]. В ретроспективном когортном исследовании с участием 268 596 корейских женщин показано увеличение риска ССЗ при приеме тиболона; прием эстрогена как отдельно, так и в комбинации с прогестагеном не увеличивал эти риски; дидрогестерон в составе комбинированной МГТ с эстрогеном был ассоциирован с достоверно более низким риском сердечно-сосудистых событий [89]. В настоящее время старт МГТ не рекомендован женщинам с установленным диагнозом ИБС, включая стенокардию [68], а ИМ является противопоказанием к МГТ. Манифестация ИБС на фоне приема МГТ, как правило, предполагает ее отмену. Хотя авторы уже упомянутого исследования HERS по его результатам заключают, что, учитывая благоприятную картину ишемических событий после нескольких лет приема МГТ, женщинам с ИБС, уже получающим это лечение, возможно его продолжить [90]. Метаанализ, включивший 5766 пациенток с уже имеющимися ССЗ, показал, что абсолютный риск смерти, ИМ, стенокардии или реваскуляризации у этой категории больных на фоне МГТ был низок (табл. 6.1). Таким образом, у пациенток с развившейся в процессе терапии ИБС, настроенных на продолжение МГТ, вопрос о ее отмене должен быть решен индивидуально совместно кардиологом и гинекологом.
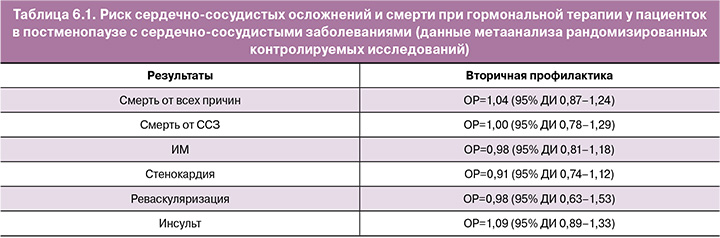
Пациенткам с инсультом в анамнезе рекомендуется избегать системной МГТ и требуется рассмотреть альтернативное (негормональное) лечение. В исследовании WHI повышенный риск ишемического инсульта был отмечен как в группе комбинированной МГТ (ОР=1,37; 95% ДИ 1,07–1,76), так и в группе монотерапии эстрогенами (ОР=1,35; 95% ДИ 1,07–1,70), независимо от исходного риска пациента [90, 91]. В метаанализе 4 исследований, включивших 719 участниц без ССЗ, риск инсульта повышался (ОР=1,32; 95% ДИ 1,12–1,56) по сравнению с плацебо. В метаанализе исследований, выполненных в рамках вторичной профилактики ССЗ (5172 участниц в 5 исследованиях), была отмечена тенденция к увеличению риска инсульта (табл. 6.1 ) [70].
Неатеросклеротическая/нетромботическая ИБС чаще встречается у женщин, однако в настоящее время нет достаточно данных для стратификации риска применения МГТ по подтипам заболевания. Для женщин 50–59 лет с ИМ в анамнезе без обструктивной болезни коронарных артерий, спонтанной диссекции коронарных артерий, коронарной микрососудистой дисфункции или коронарного вазоспазма требуется индивидуальный подход к назначению МГТ. Рекомендуется избегать системной МГТ при спонтанной диссекции коронарных артерий из-за предполагаемой патофизиологической связи с уровнем женских половых гормонов. Эта рекомендация исходит из того факта, что >90% пациентов со спонтанной диссекцией коронарных артерий – женщины.
При симптомах ГУМС женщинам с ССЗ может применяться локальная терапия эстриолом [4, 21, 68]. Необходимо обратить внимание, что в инструкциях эстрогенов для локального применения содержатся те же противопоказания, что и у эстрогенов для системной МГТ. Это предупреждение основано не на данных научных исследований, а связано с международными требованиями обязательного указания единых противопоказаний для препарата, независимо от путей его введения [81]. Эстриол при локальном применении имеет минимальную системную абсорбцию и не метаболизируется в более активные формы эстрогенов (эстрадиол и эстрон), а уровни циркулирующего эстриола, эстрадиола и эстрона сохраняются в пределах нормальных значений для постменопаузы [92, 93]. Несколько крупных обсервационных исследований подтвердили отсутствие повышенного риска неблагоприятных последствий для здоровья, включая ССЗ, ВТЭО и рак при использовании локальной МГТ эстриолом [94, 95].
Ключевые положения
- МГТ не рекомендована пациенткам с ИБС, а также с перенесенным ОНМК или ТИА. Для лечения вазомоторных симптомов у этих пациенток должна применяться негормональная терапия.
- У пациенток, с ИБС, развившейся в процессе приема МГТ, настроенных на ее продолжение, вопрос об отмене МГТ должен быть решен индивидуально в рамках консилиума, включающего кардиолога и гинеколога.
- Отсутствуют ограничения при назначении локальной МГТ для лечения симптомов ГУМС.
Раздел 7. МГТ у пациенток с факторами сердечно-сосудистого риска
7.1. Дислипидемии
Клинические исследования показали, что по сравнению с плацебо или отсутствием лечения МГТ может значительно повысить уровень липопротеинов высокой плотности, а также снизить уровень ОХС, ХС-ЛПНП и Лп(а) [96–98]. Следует отметить, что Лп(а) является независимым фактором риска ССЗ и, в частности повторного ишемического инсульта [99, 100]. Статинотерапия оказывает слабое влияние на уровень этого проатерогенного липопротеида, в отношении влияния на него МГТ данные ограничены. В рамках анализа 90 000 пациенток в первичной профилактике не было обнаружено достоверных различий в снижении уровня ЛП(а) у пациенток, получавших и не получавших МГТ [101]. Противоречивые данные имеются в отношении действия МГТ на уровень ТГ. В части исследований имело место достоверное повышение уровня ТГ [102], а в других работах не было обнаружено существенной разницы в ТГ между двумя группами, принимающих плацебо и МГТ [96, 102–111].
В целом, МГТ рассматривается как терапия, связанная с благоприятными изменениями параметров липидов как при кратковременном, так и при длительном применении у женщин в постменопаузе. Однако есть особенности, связанные с дозами препаратов и способом их доставки.
Показано, что пероральная МГТ увеличивает концентрацию ТГ по сравнению с трансдермальной МГТ [98]. Умеренное, но достоверное повышение уровня ТГ даже на фоне терапии фенофибратом и/или полиненасыщенными жирными кислотами может оказать клинически значимое воздействие как на прогрессирование атеросклероза, так и на развитие панкреатита. Таким образом, для женщин с гипертриглицеридемией более безопасным выбором являются трансдермальная или низкодозированная МГТ, или тиболон.
В то же время пероральная МГТ связана с положительным влиянием на уровень ХС-ЛПНП, а концентрация именно этого проатерогенного фактора в наибольшей степени влияет на развитие атеросклероза и дестабилизацию АСБ.
Вопрос о том, может ли МГТ в низких дозах оказывать такое же влияние на липидный профиль, как и стандартные дозы МГТ, все еще остается неясным. Одно исследование показало, что низкие дозы МГТ были связаны с более высокими уровнями ОХС и ХС-ЛПНП, более низким уровнем ТГ, чем стандартные дозы [112]. Другие исследования показали аналогичное преимущество в отношении ТГ в группе низких доз эстрогенов в составе МГТ, но не выявили существенных различий в уровнях ОХС и ХСЛПНП между двумя группами (высоких и низких доз).
Кроме того, было обнаружено, что низкие дозы эстрадиола в составе МГТ могут снижать уровень ХС-ЛПВП. Эпидемиологически низкий уровень ХС-ЛПВП в плазме был связан с повышенным риском ишемических ССЗ [113]. В совокупности преимущество низких доз МГТ и трансдермального пути введения эстрадиола в отношении липидного профиля, возможно, ограничивается только уровнем ТГ.
Существуют противоречивые данные в отношении влияния тиболона на липидный профиль. Метаанализ, проведенный в 2021 г., показал, что тиболон снижает уровни ОХС, ХС-ЛПВП и ТГ. Концентрации липопротеинов низкой плотности значительно снижаются, если прием тиболона длится ≥26 недель [114]. В отношении влияния на Лп(а) различий между обычной МГТ и тиболоном не наблюдалось [115].
Имеются данные о повышенном риске ИБС у женщин, получавших комбинированную эстрогенгестагенную терапию, но не у женщин, получавших монотерапию эстрогенами [116]. К сожалению, ни в одном крупномасштабном РКИ липидный профиль не оценивался в зависимости от типа используемого прогестагена. Одно из обсервационных исследований показало, что добавление прогестагенов ослабляет благоприятный эффект эстрогена на липидный профиль [117], а метаанализ, проведенный в 2017 г., показал, что не было существенной разницы в снижении концентрации Лп(a) [114].
Хотя результаты ряда исследований продемонстрировали положительное влияние МГТ на липидный профиль, необходимо подчеркнуть, что МГТ не рекомендуется для терапии дислипидемии и снижения риска ССЗ [118].
Ключевые положения
- МГТ положительно влияет на липидный профиль у женщин в перии постменопаузе.
- МГТ не рекомендуется в качестве терапии дислипидемии, поскольку изменения липидного профиля на фоне МГТ минимальны и не сопоставимы с эффектами гиполипидемических препаратов.
- Пероральная МГТ может быть предпочтительным выбором у женщин с повышенным уровнем ХС-ЛПНП.
- Для женщин с гипертриглицеридемией более безопасным выбором являются трансдермальная, ультранизкодозированная МГТ или тиболон.
7.2. Артериальная гипертензия
Специфичные для женщин факторы риска АГ и ССЗ в более позднем возрасте включают время наступления менархе, указания в анамнезе на нарушения менструального цикла и репродуктивной функции, миому матки, СПЯ, эндометриоз, неблагоприятные исходы беременности, ПНЯ и менопаузу. Повышенный риск в течение репродуктивного периода жизни может способствовать более значительному увеличению риска ССЗ в перии постменопаузе [119–123].
При АГ, как и при других заболеваниях, выделяют половые и гендерные различия, которые оказывают влияние на эпидемиологию, патофизиологию и клиническое ведение.
В 2019 г. стандартизированная по возрасту распространенность АГ (САД≥140 мм рт.ст., и/или ДАД≥90 мм рт.ст., или прием антигипертензивной терапии) во всем мире составила у женщин 32% [124]. При этом в Восточной Европе распространенность АГ у женщин в возрасте 30–79 лет колебалась между 34 и 46% [124]. Распространенность АГ увеличивается с возрастом [125], но имеет более выраженную тенденцию к снижению до наступления менопаузы у женщин, чем у мужчин того же возраста, с заметным повышением у женщин после наступления менопаузы [14]. После 65 лет распространенность АГ у женщин выше, чем у мужчин [124–126].
Траектории АД в течение жизни у мужчин и женщин объясняются различиями механизмов регуляции АД, сочетанием половых и гендерных факторов [124, 125]. У женщин до наступления менопаузы эстрогены способствуют снижению АД в контексте их общего вазопротекторного действия. Защита опосредована различными механизмами, в том числе эндотелиальной вазодилатацией за счет усиления пути выработки оксида азота и ингибирования активности симпатической нервной системы и ренин-ангиотензиновой системы. Более того, эстрогены уменьшают выработку эндотелина, окислительный стресс и воспаление [123]. Прекращение функции яичников в результате естественного старения или хирургической менопаузы связано с повышенным бременем кардиометаболических факторов риска, включая увеличение массы тела, уровней глюкозы и холестерина в плазме крови, АД, что приводит к повышению риска ССЗ [122, 123, 127, 128]. После менопаузы заметное снижение уровня эстрогенов частично объясняет, почему уровень АД и риск АГ увеличиваются [123, 124]. Также, в связи с резким снижением уровня прогестерона (природного антагониста альдостерона) происходит реактивация ренин-ангиотензин-альдостероновой системы с такими последствиями, как задержка жидкости, повышение АД [129].
Выделяют следующие специфичные для женщин патофизиологические характеристики АГ [130].
- Тесная связь ожирения с АГ.
- Связь гинекологических нарушений (ановуляция, пролиферативные гинекологические заболевания) и неблагоприятного течения беременности (преэклампсия, гестационный СД) с кардиометаболическим риском и АГ.
- Кардиовазопротективный эффект (в том числе вазодилатирующий) физиологического для репродуктивного возраста уровня эстрогена.
- Фармакологическое использование эстрогена при наличии сформировавшейся эндотелиальной дисфункции может способствовать увеличению АД и риска ССЗ, введение экзогенных эстрогенов в дозировках, применяемых для МГТ, не оказывает негативное влияние на АД.
- Прогестерон способствует лептин-опосредованной эндотелиальной дисфункции у женщин с ожирением до наступления менопаузы.
- Более выражена чувствительность к натрию.
- Более высокая частота воспалительных заболеваний, связанных с АГ и ССЗ.
В постменопаузе у женщин наблюдается более быстрое (по сравнению с мужчинами такого же возраста) увеличение артериальной жесткости. У женщин пожилого возраста отмечается более высокая ригидность аорты, чем у мужчин, что, по-видимому, способствует развитию изолированной систолической АГ, неконтролируемой АГ, сердечной недостаточности с сохраненной фракцией выброса левого желудочка, аортальному стенозу, что чаще встречается у женщин [131, 132].
Установлено, что менопауза удваивает риск развития АГ даже после поправки на возраст и ИМТ [133]. Хотя МГТ содержит эстрогены, нет убедительных доказательств того, что АД будет значительно повышаться у женщин в менопаузе с АГ или без нее [134]. Однако, после начала МГТ необходимо рекомендовать регулярное измерение АД для подтверждения сохраняющегося нормального АД или контроля уровня АД при антигипертензивной терапии [135, 136]. В случае неконтролируемой АГ МГТ следует прекратить. Решение об отмене МГТ целесообразно принимать совместно с кардиологом.
Ключевые положения
- МГТ может быть назначена при условии контроля АД.
- МГТ не назначается для первичной или вторичной сердечно-сосудистой профилактики.
7.3. Курение
Курение значительно увеличивает опасность артериальных сердечно-сосудистых событий и является фактором риска злокачественных новообразований.
Курение не является фактором риска ВТЭО при МГТ (включая комбинированную пероральную МГТ). Несмотря на то, что курение само по себе не является основанием для отказа от МГТ, в том числе комбинированными пероральными препаратами, необходимо соблюдать осторожность при назначении МГТ курильщицам, информировать их о рисках для здоровья, связанных с курением, и настаивать на прекращении курения. Женщинам, продолжающим курить, несмотря на все предостережения, следует сообщить, что курение, помимо всех своих других негативных последствий, может также поставить под угрозу успех МГТ [57, 137–139].
Ключевые положения
- Необходимо информировать женщин о рисках для здоровья, связанных с курением, и настаивать на его прекращении.
- У курящих женщин решение о возможности применения МГТ следует принимать с учетом совокупности всех факторов риска.
Раздел 8. МГТ в особых клинических ситуациях
8.1. Атеросклероз периферических артерий
Среди женщин в возрасте 45–49 лет распространенность атеросклероза периферических артерий составляет 4,89%, в возрасте 50–55 лет – 5,73%, в возрасте 56–60 лет – 6,73%. Менопауза увеличивает риск развития каротидного атеросклероза в 2 раза [140]. Преждевременная и ранняя менопауза связана с увеличением объема и распространенности АСБ [141].
Применение монотерапии эстрогенами у женщин в постменопаузе в течение года снижает риск атеросклероза периферических артерий на 52%, как было показано в наблюдательном исследовании Rotterdam study [142]. В другом наблюдательном исследовании было определено, что МГТ независимо от ее выбора снижает риск развития атеросклероза периферических артерий на 20% [143]. В последних наблюдательных исследованиях показан положительный эффект эстрогенов на толщину комплекса интима-медиа сонных артерий только в ранний период после менопаузы (до 6 лет), в более поздний период, особенно после 10 лет, эстрогены способствуют прогрессированию атеросклероза [144, 145].
МГТ не снижает риск прогрессирования атеросклероза у женщин с установленными атеросклеротическими ССЗ [146].
У больных ИБС в РКИ HERS и HERSII комбинированная пероральная МГТ не обеспечила статистически значимого снижения количества событий, связанных с атеросклерозом периферических артерий [147, 148].
В описательном обзоре Davies R.S. et al. в качестве механизма, положительного влияния МГТ на течение периферического атеросклероза, обсуждается снижение уровня циркулирующих липопротеинов низкой плотности, повышение уровня липопротеинов высокой плотности и положительное воздействие на функцию эндотелия [149].
8.2. Хроническая сердечная недостаточность
В Российской Федерации, по данным популяционного исследования ЭПОХА-ХСН, распространенность ХСН у женщин в возрасте 50 лет составляет 12,2%, в возрасте 60 лет – 26,2%, преимущественно с сохраненной ФВ ЛЖ [150]. Пятилетняя выживаемость больных с ХСН составляет не более 50% [151]. Ранняя постменопауза увеличивает риск развития ХСН на 33%, как было выявлено в метаанализе 3 наблюдательных исследований [152].
В РКИ после 10 лет лечения было выявлено, что женщины, получающие пероральную терапию эстрогенами или комбинированную МГТ, назначенную в первые 7 месяцев в среднем после менопаузы, имели значительно ниже риск смерти, ХСН, ИМ без какого-либо увеличения риска рака, ВТЭО или инсульта [153].
Пероральная и трансдермальная терапия эстрогенами, а также комбинированная МГТ у пациенток 50 лет и старше с ХСН III–IV функционального класса и ФВ ЛЖ <35% неишемической этиологии обеспечила статистически значимое снижение риска общей смертности на 40%, как было продемонстрировано в субанализе РКИ BEST (BetaBlocker Evaluation of Survival Trial) [154].
Последний метаанализ 6 РКИ и наблюдательных исследований, в который было включено 25 047 женщин, не показал статистической связи между любым вариантом МГТ и риском развития ХСН у женщин в постменопаузе. При этом снижение смертности от всех причин на 35% наблюдалось среди пациенток с ХСН, которые получали МГТ. В анализе возрастных подгрупп не было замечено существенного изменения риска развития ХСН [155].
Субанализ РКИ WHI (Women’s Health Initiative) показал, что монотерапия пероральными эстрогенами и комбинированная МГТ не увеличивает риск госпитализаций, связанных с ХСН, независимо от ФВ ЛЖ и возраста женщины при назначении МГТ [156]. По данным мониторинга за выпиской рецептов и визитами к врачу системы Medicare среди 10 млн женщин в возрасте 65 лет и старше, монотерапия эстрогенами статистически значимо снижала риск развития ХСН на 5%, комбинированная МГТ – на 4% [157].
8.3. Фибрилляция предсердий
Известно, что женщины во всех возрастных группах имеют более низкую распространенность ФП по сравнению с мужчинами, но смертность от всех причин у женщин выше: ФП независимо связана с 2-кратным увеличением риска смерти у женщин по сравнению с 1,5-кратным увеличением риска смерти у мужчин [158]. В наблюдательном исследовании ATRIA ежегодная частота тромбоэмболических осложнений у пациентов с ФП, не принимающих варфарин, составила 3,5% для женщин по сравнению с 1,8% для мужчин [159]. До 2024 г. считалось, что женщины с дополнительными факторами риска инсульта, особенно в старшем возрасте (>65 лет), подвергаются большему риску, даже если они принимают антикоагулянтную терапию, в то время как риск кровотечения при антикоагуляции был одинаков у представителей обоих полов [160]. В новых рекомендациях Европейского общества кардиологов принято решение о том, что женский пол является лишь возрастным модификатором риска инсульта, а не независимым биологическим фактором риска [161]. При этом у женщин с ФП более выражена симптоматика и тяжесть инсультов.
В постменопаузе на 82% увеличивается риск ФП [162]. Было показано, что эстроген оказывает как защитное, так и проаритмическое действие на сердце [163].
Данные наблюдательного исследования BiomarCaRE Consortium в Европе продемонстрировали, что у женщин в постменопаузе (средний возраст 49,2 года) распространенность ФП составила 4,4%, что было взаимосвязано с увеличением риска инсульта на 42%, ИМ – на 78%, а частота смертельных исходов возрастала более, чем в 3,5 раза [164].
По данным субанализа РКИ WHI и наблюдательных исследований, комбинированная МГТ, монотерапия пероральными эстрогенами, применение тиболона увеличивает риск развития ФП [162, 165–167].
Результаты последних лет демонстрируют противоречивые данные в этом вопросе. В ретроспективном наблюдательном исследовании было показано, что применение МГТ, за исключением использования монотерапии эстрадиолом в комбинации его с прогестином, увеличивало риск развития ФП у женщин в менопаузе [168]. У женщин, принимающих ранее эстрадиол в сочетании с прогестином, отмечалось снижение риска ФП с поправкой на факторы риска (p=0,027). Продолжающаяся МГТ представляла повышенный риск развития ФП. Степень риска варьировалась в зависимости от конкретного типа эстрогена и прогестинов при совместном назначении. Результаты исследования указывают на то, что в отношении риска ФП пероральная эстрадиолсодержащая МГТ превосходит МГТ, содержащую пероральный лошадиный конъюгированный эстроген или тиболон.
Появились новые сведения мониторинга за выпиской рецептов и визитами к врачу системы Medicare среди 10 млн женщин в возрасте 65 лет и старше, в которых было определено, что монотерапия эстрогенами и пероральная комбинированная МГТ статистически значимо снижали риск развития ФП на 4% независимо от вида МГТ [157].
Вклад локальных форм эстрогенов в развитие ФП у женщин в период менопаузы не определен.
8.4. Патология клапанов сердца
Возможность назначения пероральной МГТ у женщин в перии постменопаузе с патологией клапанов определяется наличием осложнений:
- при фибрилляции предсердий и тромбах в камерах сердца МГТ противопоказана.
- при ХСН неишемической этиологии и отсутствии осложнений МГТ может быть назначена в рамках междисциплинарного консилиума [169].
8.5. Легочная гипертензия
Половые различия влияют не только на распространенность легочной гипертензии независимо от ее патогенеза, но и на тяжесть, реакцию на лечение и результаты выживаемости [170]. Хотя женщины более восприимчивы к развитию легочной гипертензии, они также демонстрируют лучшую реакцию на лечение и более высокие показатели выживаемости по сравнению с мужчинами [170]. Эти различия были названы «эстрогенным парадоксом» с положительным влиянием эстрогена на течение и прогноз [171].
Результаты исследований, касающиеся использования МГТ при легочной гипертензии, противоречивы. В экспериментальных исследованиях выявлено, что МГТ может улучшить состояние правых отделов сердца и снизить давление в легочной артерии [172]. Тем не менее, крупное одноцентровое исследование, проведенное в 2020 г., не выявило существенных различий в эндогенном или экзогенном воздействии половых гормонов в отношении развития и прогрессирования легочной гипертензии [173].
Раздел 9. Мигрень
Мигрень в популяции стран Европы и США встречается у 17% женщин и 8% мужчин. Взрослые женщины болеют в 2,5–3 раза чаще, чем мужчины [174]. Установлена зависимость частоты приступов мигрени от колебаний уровней половых стероидных гормонов.
Выделяют две основные формы мигрени: без ауры (до 80% всех случаев) и с аурой (20% всех случаев); аура представляет собой преходящие неврологические нарушения (зрительные, чувствительные и/ или речевые симптомы), предшествующие головной боли [174]. Мигрень с аурой сопряжена с 2-кратным увеличением риска инсульта [175].
При подозрении на мигрень у женщин в постменопаузе необходима консультация невролога для исключения другой патологии.
Поскольку данные о взаимосвязи между МГТ и мигренью отсутствуют, нельзя сделать вывод, что мигрень является противопоказанием для МГТ [176].
Мигрень без ауры совместима практически с любыми вариантами и режимами МГТ. Непрерывная комбинированная МГТ в меньшей степени провоцирует головную боль, чем циклический режим, особенно при использовании низких доз эстрогена [177]. Мигрень с аурой не является противопоказанием для МГТ. При мигрени с аурой следует использовать минимальную дозу эстрогенного компонента, биодентичного натуральному, которая эффективно контролирует вазомоторные симптомы [178]. Возможно использование в качестве монотерапии трансдермальных эстрогенов, которые обеспечивают стабильную плазменную концентрацию эстрадиола без резких пиковых суточных колебаний в сыворотке крови и позволяют минимизировать риски возникновения приступов мигрени, или в комбинации с внутриматочной системой, содержащей 52 мг левоноргестрела микронизированного (ЛНГ-ВМС) [178, 179].
Заключение
- Показания и противопоказания к назначению МГТ определяются актуальными Клиническими рекомендациями и инструкциями к конкретным препаратам.
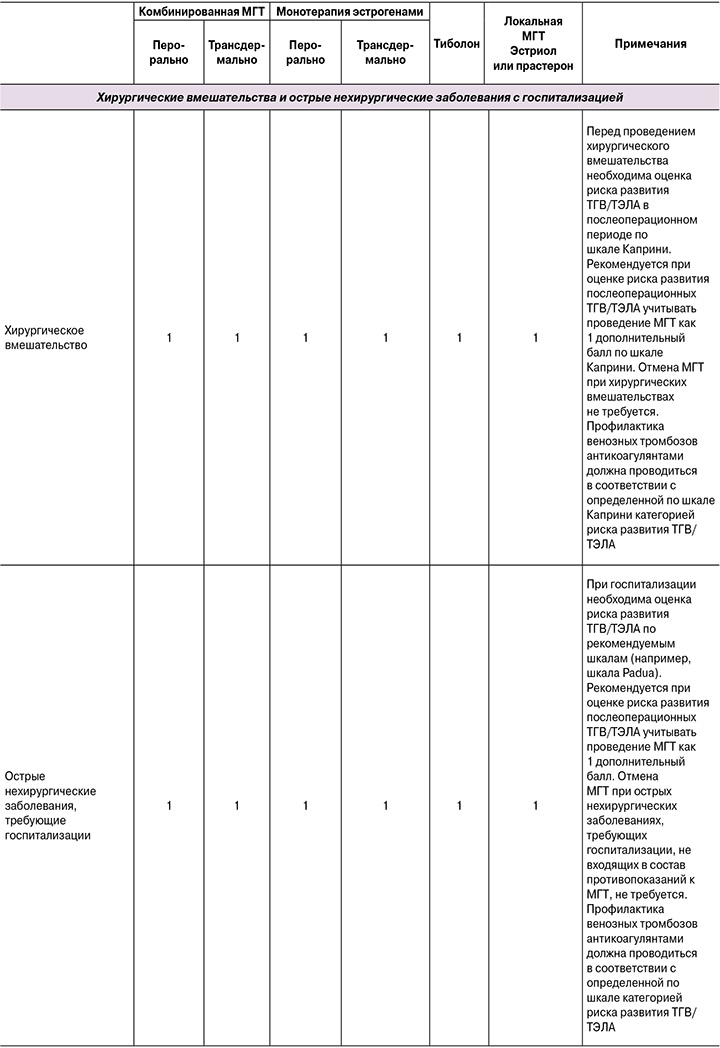
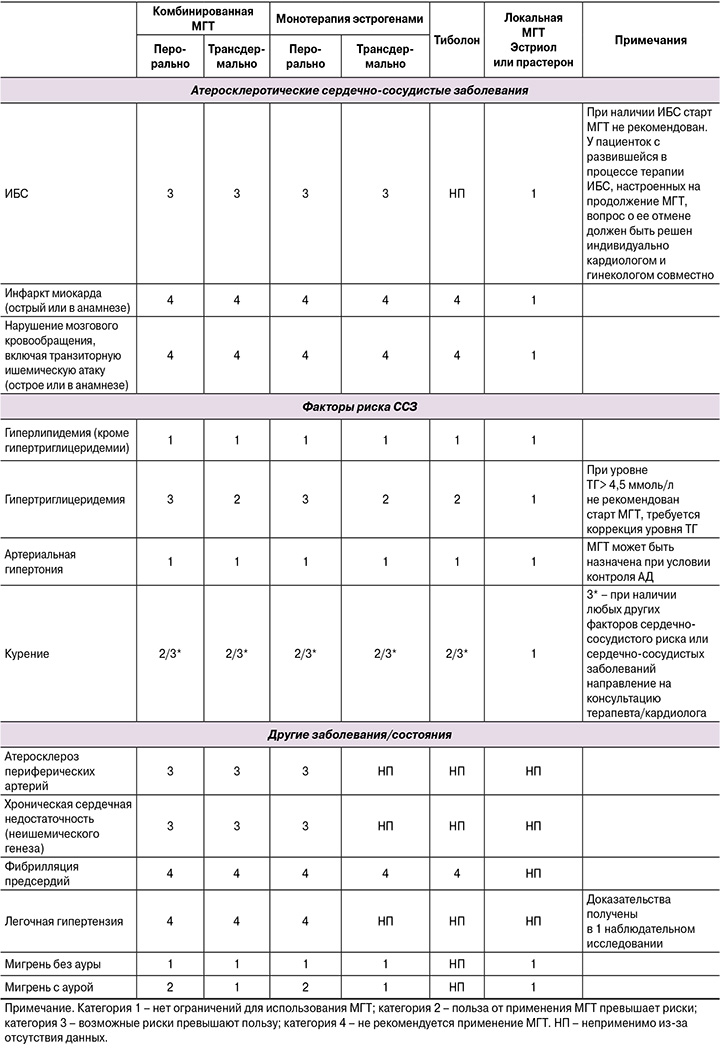
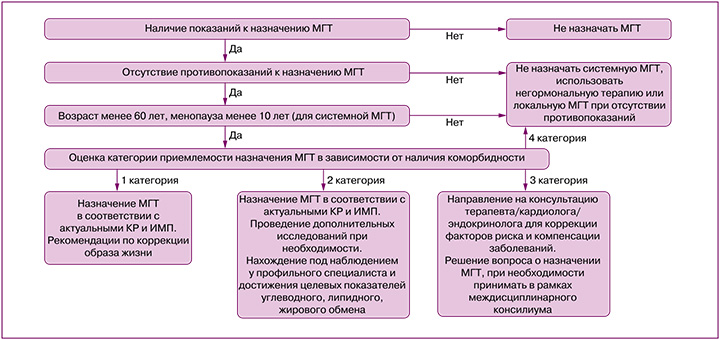
- Свод критериев приемлемости назначения МГТ пациенткам с сердечно-сосудистыми и метаболическими заболеваниями приведен в Приложении 1. Для унификации рекомендаций были определены следующие категории в соответствии с международной номенклатурой ВОЗ [31]:
- КАТЕГОРИЯ 1 – нет ограничений для использования МГТ;
- КАТЕГОРИЯ 2 – польза от применения МГТ превышает риски;
- КАТЕГОРИЯ 3 – возможные риски превышают пользу;
- КАТЕГОРИЯ 4 – не рекомендуется применение МГТ.
- При обращении женщины с жалобами на приливы, потливость, сердцебиения, врачу-интернисту необходимо провести опрос с целью выявления взаимосвязи жалоб с возможными климактерическими нарушениями. Опрос должен включать сведения о дате последней самостоятельной менструации, нарушении регулярности менструального цикла и текущем приеме гормональной контрацепции или МГТ. В случае подозрения на связь жалоб с климактерическими расстройствами необходимо направить женщину на консультацию к акушеру-гинекологу.
- Назначение МГТ, коррекция дозы, смена ЛС, прекращение МГТ, ежегодный динамический контроль за эффективностью/переносимостью лечения, актуализацию целей терапии и оценку баланса польза/риск проводит врач акушергинеколог (Приложения 2 и 3).
- При выявлении/подозрении на наличие нежелательных явлений, ассоциированных с приемом МГТ, врачом негинекологического профиля пациентке должна быть рекомендована консультация акушера-гинеколога.
- При выявлении/подозрении на наличие факторов сердечно-сосудистого риска и сердечно-сосудистых и метаболических заболеваний врачами акушерами-гинекологами пациентке должна быть рекомендована консультация врачатерапевтического профиля.
Приложение 1. Критерии приемлемости назначения МГТ
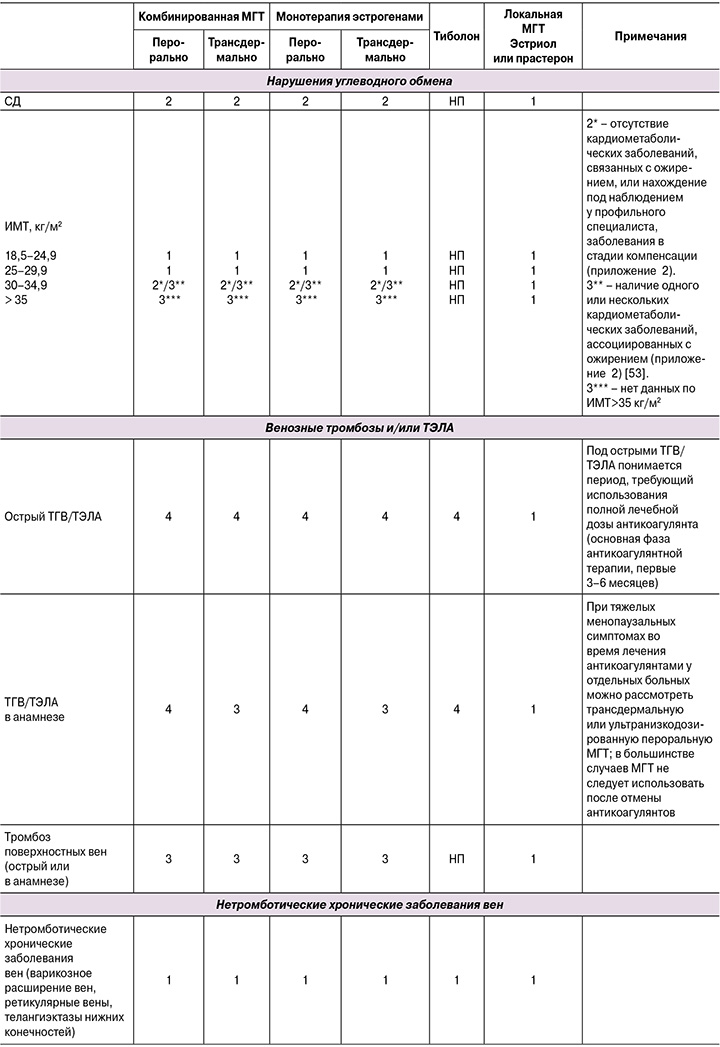
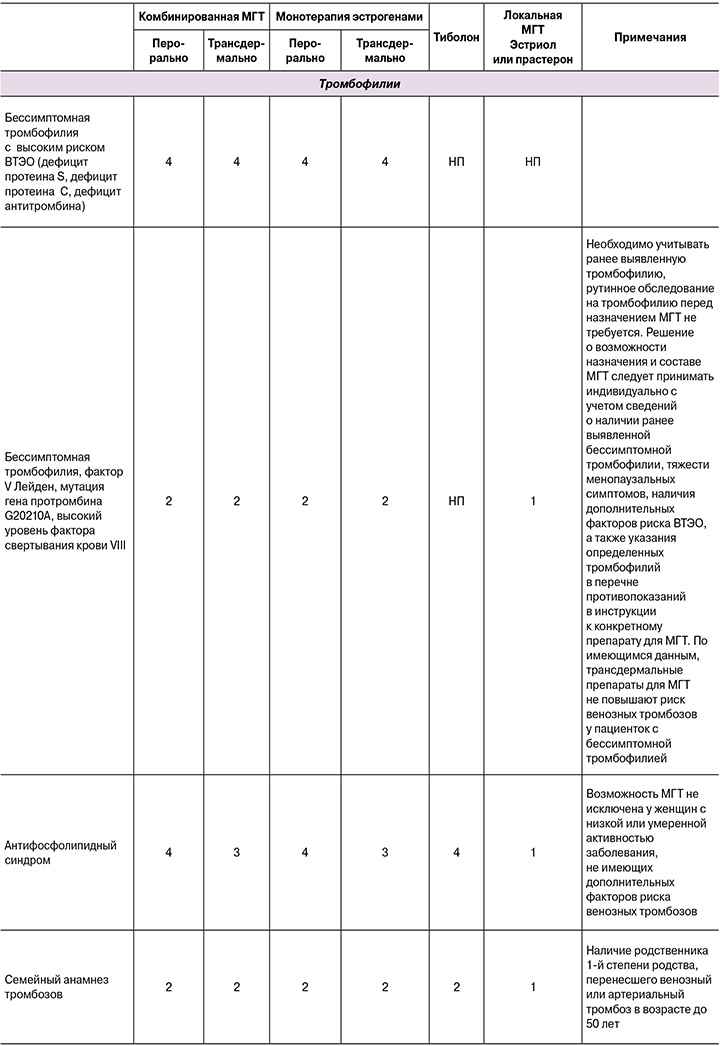
Приложение 2. Кардиометаболические заболевания, связанные с ожирением (адаптировано по [180])

Приложение 3. Алгоритм принятия решения о назначении МГТ
Приложение 4. Алгоритм принятия решения об отмене МГТ