«Первая линия» защиты от инфицирования осуществляется эффекторами врожденного иммунитета, обеспечивающими своевременное выявление чужеродных инфекционных агентов и их быструю элиминацию за счет формирования локальной воспалительной реакции с последующей репарацией поврежденной ткани, что необходимо для предотвращения генерализации инфекции [1].
Среди сигнальных рецепторов врожденного иммунитета Toll-like рецепторы (TLRs) являются наиболее древними, генетически детерминированными структурами (трансмембранными белками, содержащими множество остатков лейцина во внеклеточной части). TLRs играют центральную роль в инициации врожденного иммунного ответа, осуществляя непосредственное взаимодействие рецептора с паттернами микробных агентов (липополисахаридами, белками бактериальных жгутиков, вирусной двухцепочечной РНК и др.) [2, 3]. TLRs экспрессируются на поверхности макрофагов, нейтрофилов, естественных киллеров, дендритных клеток, покровного эпителия, эндотелия сосудов и др. [1, 4], и, связываясь с различными лигандами, индуцируют экспрессию цитокинового каскада, формируя воспалительную реакцию, направленную на эрадикацию инфекционного агента [1–3, 5].
Открытие TLRs удостоено многочисленных признаний. В 2010 году Р. Меджитов и J. Hoffmann получили «Премию Розенстилаза» за разъяснение механизмов врожденного иммунитета, в 2011 году C. Janeway и Р. Меджитов – «Премию Шао» за революционную идею о ведущей роли TLRs в активации адаптивного иммунного ответа. Итогом этих инновационных исследований явилось присуждение в 2011 году «Иммунологической Нобелевской премии» по физиологии и медицине B. Beutler и J. Hoffmann за открытия активаторов врожденного иммунитета и R. Steinman за изучение роли дендритных клеток в механизмах приобретенного иммунитета [6].
Открытие TLRs послужило основанием для пересмотра устоявшихся воззрений на некоторые патогенетические механизмы развития хронического эндометрита (ХЭ) и возникновения на его фоне привычного невынашивания беременности, преждевременных родов и внутриутробной задержки развития плода [7]. Представленность TLRs в разных отделах репродуктивного тракта строго специфична [8]: эпителиальные клетки влагалища и эндоцервикса экспрессируют TLR 1-3, TLR5 и TLR6 [9], эндометриальные клетки – TLRs 1–10-го типов, что обусловлено необходимостью ответа на широкий диапазон микробных агентов [10].
Из всех идентифицированных TLRs наиболее широким спектром специфичности обладает TLR2, который располагается на поверхности клетки и связывается с различными лигандами бактерий, вирусов, грибов, простейших [10]. TLR4 также экспрессируется преимущественно на поверхности клетки и распознает, помимо паттернов микроорганизмов, белки теплового шока 60 и 70, полисахаридные фрагменты гепарина сульфата, гиалуроновую кислоту, фибриноген и фибронектин хозяина [10]. TLR9, располагаясь внутриклеточно на поверхности эндосом, распознает неметилированные повторы CpG ДНК бактерий, вирусов, простейших, гемозоин простейших, комплекс хроматина и иммуноглобулин G хозяина [8, 10, 11].
Цель исследования: изучение экспрессии TLRs 2, 4, 9-го типов в эндометрии при ХЭ.
Материал и методы исследования
В исследование включены 60 пациенток репродуктивного возраста (средний возраст 32,1±5,2 года), обратившихся в Научный центр акушерства, гинекологии и перинатологии им. академика В.И. Кулакова с различными жалобами (табл. 1). На 7–10-й день менструального цикла 35 пациенткам произведена гистероскопия, диагностическое выскабливание слизистой оболочки полости матки, а 25 – аспирационная биопсия эндометрия с помощью кюретки Pipelle de Cornie. Для изучения врожденного локального иммунного ответа в эндометрии были выбраны 3 рецептора (TLRs 2, 4, 9). Изучение экспрессии TLRs проводилось методом иммуногистохимии (ИГХ) (n=60) и с помощью реакции обратной транскрипции полимеразной цепной реакции в реальном времени (ОТ-ПЦР) (n=60).
Морфологическое исследование эндометрия (n=60) включало верификацию ХЭ на основе следующих морфофункциональных его характеристик: наличие воспалительных лимфоплазмоклеточных инфильтратов и очагового фиброза в строме эндометрия, склеротических изменений стенок спиральных сосудов слизистой оболочки полости матки.
На основе результатов гистологического исследования эндометрия пациентки были разделены на 2 группы: I (n=45) – женщины с морфологически подтвержденным ХЭ, II (n=15) – группа сравнения, условно здоровые женщины (эндометрий ранней, средней и поздней стадий пролиферации). При этом I группа пациенток на основании морфологической характеристики эндометрия и обязательного наличия клинических проявления ХЭ (аномальные маточные кровотечения и/или нарушения репродуктивной функции) была разделена на 3 подгруппы. Iа подгруппа (n=15) – полный симптомокомплекс ХЭ, который верифицировался при одновременном выявлении воспалительных лимфоплазмоклеточных инфильтратов и очагового фиброза в строме эндометрия, склеротических изменений стенок спиральных сосудов эндометрия; Ib подгруппа (n=15) – неполная форма ХЭ с инфильтрацией, которую диагностировали при наличии очаговой или рассеянной инфильтрации стромы лимфоцитами. Iс подгруппа (n=15) – неполная форма ХЭ с фиброзом (склерозом), которая верифицировалась при наличии фиброзирования стромы эндометрия и/или склеротических изменений сосудов слизистой оболочки полости матки.
Микробиологическое исследование (n=60) включало оценку микробиоценоза биоптата эндометрия в аэробных, микроаэрофильных и анаэробных условиях культивирования по общепринятой методике. При этом в I группе (n=45) у 20 пациенток обнаружен рост условно-патогенных микроорганизмов (УПМ), у 25 женщин возбудители не выявлены. Во II группе у всех пациенток (n=15) УПМ не были выявлены.
ИГХ-реакции (n=60) проводились на депарафинированных срезах, фиксированных на предметных стеклах. Неокрашенные срезы обрабатывались в соответствии со стандартным протоколом ИГХ с демаскировкой антигенов в ретривере (диаминабензидин). В качестве первичных антител использовались моноклональные антитела TLR 2, 4, 9 (Abbiotec, 1:100).
В соответствии с рекомендациями фирмы-производителя выбирались положительные контроли для каждого антитела. Далее проводилась полуколичественная и количественная оценка результатов реакции по проценту позитивно окрашенных клеток в баллах: 0 баллов – отсутствие окрашенных клеток; 2 балла – менее 20% окрашенных клеток; 4 балла – от 20 до 40% окрашенных клеток; 6 баллов – 40 и более процентов окрашенных клеток.
Определение мРНК генов TLR 2, 4, 9 (n=60) осуществлялось методом количественной ОТ-ПЦР в реальном времени (реактивы ДНК-технология, Россия). Выделение РНК осуществлялось методом фенольной депротеинизации с последующим спиртовым осаждением. В реакции обратной транскрипции использовали специфические олигонуклеотиды, в ПЦР-реакции – праймеры, не отжигающиеся на матрице геномной ДНК. В реакции использовали флюоресцентно-меченные олигонуклеатиды, идентификацию сигнала проводили на каждом цикле по каналу FAM. Реакцию ставили в двух повторах на каждой точке. Нормировка значения уровня экспрессии осуществлялась по трем референсным генам TBP, B2M, GUSB и значению медианы в контрольной группе (метод сравнения пороговых циклов Δ∆Cq). За 1 было принято значение медианы (Ме) в группе сравнения.
Полученные данные ИГХ и ОТ-ПЦР обрабатывались математически на персональном IBM-РС. При оценке значимости межгрупповых различий применялся непараметрический U-критерий Манна–Уитни для несвязанных совокупностей, а также корреляционный анализ методом Спирмена. Для всех видов анализа статистически значимым считали значения р<0,05. Статистическая обработка проведена с применением пакета прикладных программ Statistica 7.0, построение гистограмм проводилось в программе Microsoft Excel 2000.
Результаты
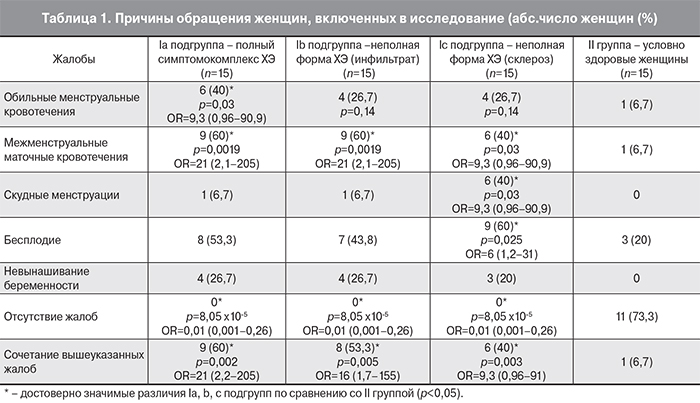
У всех пациенток проведен детальный анализ анамнестических данных, результатов микробиологического, морфологического, ИГХ исследований и ОТ-ПЦР диагностики биоптатов эндометрия. В группах обследованных женщин по возрасту, массе тела, росту, возрасту менархе, числу родов статистически значимых различий выявлено не было (р>0,05). Основные причины обращения пациенток представлены в табл. 1.
Наиболее часто пациентки с ХЭ (I группа) предъявляли жалобы на различные нарушения менструального цикла, ведущими среди них были межменструальные маточные кровотечения (53,3%), продолжительность которых варьировала от 4 до 10 дней, что согласуется с данными литературы [12]. При этом по частоте выявления данного клинического проявления ХЭ отмечены достоверно значимые различия в Ia, Ib, Ic подгруппах по сравнению со II группой (р=0,0019, р=0,0019, р=0,03 соответственно). Также выявлены статистически значимая разница по частоте встречаемости обильных менструальных кровотечений в Iа подгруппе (40%) по сравнению со II группой (6,7%) (р=0,03). Гипоменструальный синдром чаще диагностировали у женщин Ic подгруппы (40%), в сравнении с Ib (6,7%), Ic (6,7%) подгруппами и II группой (р=0,03). При этом у 66,7% (у 4 из 6) пациенток Ic подгруппы на основании результатов гистероскопии подтверждено наличие внутриматочных синехий различной степени выраженности.
Морфологическая верификация диагноза ХЭ была основана на современных критериях оценки воспалительного процесса в эндометрии: наличие воспалительных лимфоплазмоклеточных инфильтратов в строме эндометрия, неоангиогенеза, очагового фиброза стромы и склеротических изменений стенок спиральных сосудов эндометрия (рис. 1 см. на вклейке).
Для оценки локального иммунного ответа в эндометрии были выбраны 3 рецептора (TLRs 2, 4, 9-го типов), реагирующие на широкий спектр микроорганизмов и эндогенных лиганд.
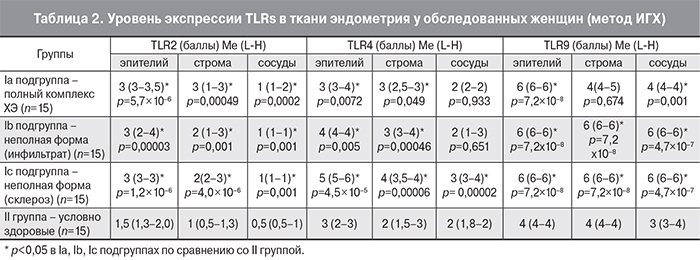
При ИГХ экспрессия TLRs 2, 4, 9-го типов выявлялась в виде коричневого окрашивания цитоплазматической мембраны и цитоплазмы в покровном и железистом эпителии, в стромальных клетках, а также в эндотелии сосудов эндометрия (рис. 2 см. на вклейке). В I группе пациенток отмечена достоверно повышенная экспрессия TLRs 2, 4, 9-го типов почти во всех структурах слизистой оболочки полости матки по сравнению со II группой (р<0,05) (табл. 2). Экспрессия рецепторов врожденного иммунитета в эпителиальных клетках эндометрия максимальна, так как эпителий первый контактирует с инфекционным агентом (табл. 2).
Выявлены умеренные прямые корреляционные связи изменения уровней экспрессии TLR2 между эпителиальными и стромальными клетками (r=0,5, p=0,0001), эпителием и эндотелием сосудов (r=0,5, p=6,2х10-6), стромой и эндотелием сосудов эндометрия (r=0,4, p=0,0005). Умеренные прямые корреляционные связи изменения уровней экспрессии TLR4 выявлены между эпителиальными и стромальными клетками (r=0,5, p=0,000007), эпителием и эндотелием сосудов (r=0,6, p=2,5×10-6), стромой и эндотелием сосудов эндометрия (r=0,5, p=8,2×10-6). Установлены умеренные и сильные прямые корреляционные связи изменения уровней экспрессии TLRs 9 между эпителиальными и стромальными клетками (r=0,6,p=9,2×10-7), эпителием и эндотелием сосудов (r=0,7, p=1,0×10-11), стромальными клетками и эндотелием сосудов слизистой оболочки матки (r=0,8, p=1,4×10-13).
При микробиологическом исследовании биоптатов эндометрия в I группе с ХЭ у 25 женщин (55,6%) возбудители не выявлены (посевы были стерильны или выделялись представители Lactobacillus spp.(в концентрации ≤3lg Кое/мл); у 20 пациенток (44,4%) обнаружен рост возбудителей. При этом в 100% случаях среди инфекционных агентов в эндометрии выявлялись представители условно-патогенной флоры, наиболее часто встречались следующие УПМ: Streptococcus spp., Gardnerella vaginalis, Enterococcus faecalis, Staphylococcus spp.
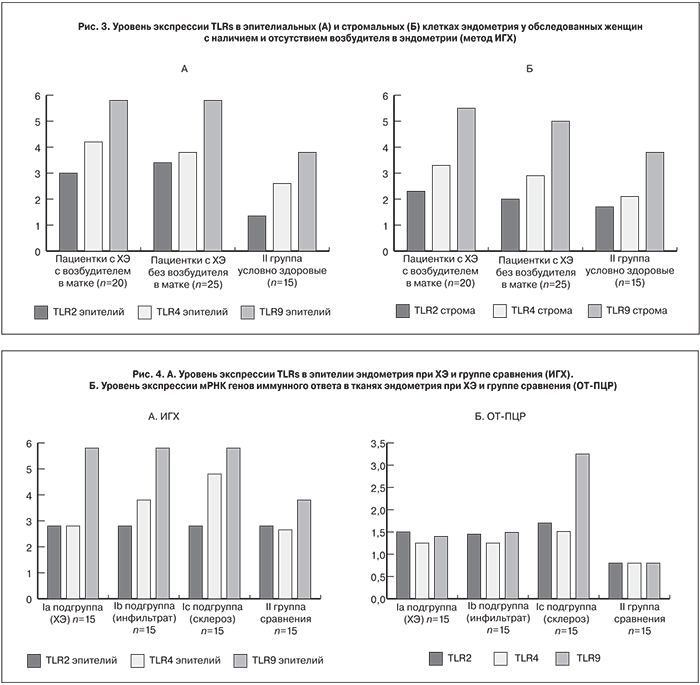
Результаты сравнительного анализа экспрессии TLRs в зависимости от наличия микробного фактора показаны на рис. 3.
Во II группе пациенток экспрессия TLRs была достоверно ниже, чем у пациенток в I группе (p<0,05).
Установлено, что частота представленности TLRs в слизистой оболочке полости матки у пациенток с ХЭ была одинаково высока независимо от наличия или отсутствия возбудителя в эндометрии (р>0,05). Таким образом, качественная и количественная характеристика микробиоты эндометрия не влияла на выраженность экспрессии TLRs 2,4, 9 типов в ткани эндометрия.
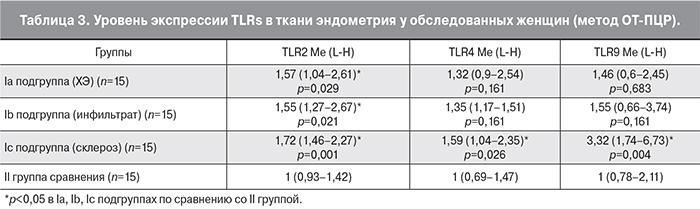
Результаты экспрессии TLRs в ткани эндометрия у обследованных женщин, полученные методом ОТ-ПЦР, представлены в табл. 3.
Сопоставление данных экспрессии TLRs методами ИГХ и ОТ-ПЦР
Проанализированы результаты двух параллельно проведенных исследований экспрессии TLRs 2, 4, 9 типов: методами ИГХ и ОТ-ПЦР в реальном времени (рис. 4 А, Б). Качественный сравнительный анализ показал, что независимо от используемых методов экспрессия TLRs 2, 4, 9 во II группе была достоверно ниже, чем в Ia, Ib, Ic подгруппах с ХЭ (р<0,05).
Проведен корреляционный анализ уровней экспрессии TLRs, полученных двумя методами ИГХ и ОТ-ПЦР, установивший прямую слабую связь экспрессии TLR2 между эпителиальными клетками эндометрия методом ИГХ и эндометрия в целом методом ОТ-ПЦР (r=0,3, p=0,024). Также установлены слабые прямые корреляционные зависимости экспрессии TLR9 между стромальными клетками слизистой оболочки полости матки методом ИГХ и эндометрия в целом методом ОТ-ПЦР (r=0,3, p=0,028); экспрессии TLR9 между сосудами слизистой оболочки полости матки методом ИГХ и эндометрия в целом методом ОТ-ПЦР (r=0,3, p=0,023).
Важно подчеркнуть, что данные, полученные с помощью ИГХ, дополняют результаты ОТ-ПЦР, уточняя структурный клеточный элемент наиболее выраженной экспрессии TLR 2, 4-го типов – эпителий эндометрия.
Обсуждение
Полученные нами результаты совпадают с данными ряда авторов, также подчеркивающих важную роль TLRs в патогенезе развития острых и хронических воспалительных поражений нижних отделов полового тракта [7, 8, 13]. В современной литературе обсуждаются лиганды, связывающие типоспецифические TLRs и тонкие механизмы их взаимодействия [5, 8, 10, 13]. Перспективным направлением является изучение роли системы сигнальных рецепторов в поддержании микробиоценоза полового тракта женщин и их невосприимчивости к воспалительным заболеваниям органов малого таза. Нами не найдено доступных клинических работ, посвященные экспрессии рецепторов врожденного иммунитета в эндометрии при ХЭ. Однако имеется ряд исследований, в которых на клеточных культурах человека или на животных моделях продемонстрировано увеличение экспрессии TLRs в ответ на экзогенно вводимые паттерны инфекционных агентов [14, 15].
Полученные в нашем исследовании результаты свидетельствуют об активации рецепторов врожденного иммунитета (TLRs 2, 4, 9), ограничивающих распространение воспалительной реакции в эндометрии. Экспрессия TLRs 2, 4, 9 при ХЭ была достоверно выше, чем в группе условно здоровых женщин (р<0,05). При сравнительном анализе уровней экспрессии TLRs метом ИГХ и ОТ-ПЦР было показано, что эти методы дополняют друг друга. В ходе проведенного корреляционного анализа установлена слабая прямая связь экспрессии TLR2 только между эпителиальными клетками эндометрия методом ИГХ и в целом в ткани эндометрия методом ОТ-ПЦР (r=0,3, p=0,024), что подтверждает более выраженную представленность TLR2 на поверхностных структурах эндометрия, то есть на эпителиальных клетках. Вероятно, это связано с тем, что наиболее широким спектром специфичности из всех идентифицированных TLRs является именно TLR2, экспрессирующий ранние продукты провоспалительных медиаторов и участвующий в развитии хронического воспаления [10]. В исследовании также установлены слабые прямые корреляционные зависимости изменений уровней TLR9 между стромальными клетками, сосудами слизистой оболочки полости матки методом ИГХ и в целом эндометрия методом ОТ-ПЦР (r=0,3, p=0,028; r=0,3, p=0,023 соответственно). Вышеописанные корреляции демонстрируют более выраженный синтез TLR9 в более глубоких слоях эндометрия, что, вероятно, связано с внутриклеточной экспрессией TLR9, а также с его активацией в процессе фиброзирования тканей [16, 17].
Выявленные нами умеренные и сильные корреляционные зависимости изменений уровней экспрессии TLRs 2, 4, 9-го типов между различными структурными компонентами эндометрия (эпителиальные, стромальные клетки и эндотелий сосудов эндометрия) при использовании метода ИГХ свидетельствуют о скоординированном иммунном ответе на воспалительный процесс, затрагивающий все структуры эндометрия, что объективно подтверждается результатами, полученными методом ОТ-ПЦР, оценивающим экспрессию TLRs в структурах эндометрия в целом.
Особую научную ценность представляют полученные нами результаты, указывающие на то, что уровень экспрессии TLRs в слизистой оболочке полости матки у пациенток с ХЭ оставался высоким независимо от наличия или отсутствия возбудителя в эндометрии (р>0,05). Это на первый взгляд парадоксальное явление, согласно мнению C. Janeway и Р. Меджитова [1], объясняется тем, что эффекторами активации TLRs могут быть не только молекулярные паттерны, синтезируемые микроорганизмами, но и продукты деструкции эндометрия, образующиеся в результате воспалительного процесса. На первом этапе инфекционный агент, попавший в эндометрий, запускает активацию TLRs с развитием воспалительного ответа, необходимого для элиминации инфекта. Длительная персистенция возбудителя и гиперактивация иммунной системы могут приводить к повреждению ткани. Продукты деструкции эндометрия являются лигандом для поддержания гиперактивности TLRs в слизистой оболочке матки даже после элиминации возбудителя, возможно, являясь патогенетической основой формирования в дальнейшем аутоиммунного поражения эндометрия. Описанный выше механизм способствует развитию чрезмерного воспалительного ответа, приводящего к склерозированию стенок сосудов и образованию периваскулярного склероза вокруг спиральных артерий и в базальном слое эндометрия, в результате чего развивается ишемия и, как следствие, формирование внутриматочных синехий различной степени выраженности [18]. Согласно полученным нами результатам у пациенток Ic подгруппы обнаружено более значимое повышение экспрессии TLRs 2, 4, 9 в сравнении с Ia и Ib подгруппами, которое, вероятно, способствовало выраженному снижению функциональной активности эндометрия, что клинически характеризовалось наличием гипоменструального синдрома у ряда пациенток Ic подгруппы.
Заключение
Таким образом, изучение экспрессии рецепторов врожденного локального иммунного ответа (TLRs 2, 4, 9) при ХЭ показало:
- Внедрение инфекционного агента в эндометрий является инициирующей причиной развития воспалительного процесса;
- Активатором TLRs помимо микробных паттернов могут быть эндогенные лиганды (продукты деструкции ткани), образующиеся в результате воспалительных изменений эндометрия и поддерживающие «порочный» круг хронизации воспалительного процесса;
- Для предотвращения гиперпродукции TLRs и ограничения в дальнейшем развития воспалительных и аутоиммунных процессов необходимы не только быстрая элиминация возбудителя, но и восстановление нормальной морфологической структуры эндометрия.
Таким образом, изучение экспрессии TLRs 2, 4, 9-го типов в эндометрии позволило глубже понять патогенетические механизмы, лежащие в основе развития ХЭ. Согласно нашим результатам, для предотвращения хронизации воспалительного процесса в эндометрии необходимо: быстрая элиминация возбудителя, предупреждение его персистенции, подавление гиперпродукции экспрессии TLRs, а также восстановление нормальной архитектоники слизистой оболочки полости матки. В связи с вышеизложенным, помимо проведения традиционной этиологически обоснованной антибактериальной терапии при ХЭ, необходим поиск новых лечебных подходов. В то же время можно полагать, что у некоторых женщин наблюдается повышенная предрасположенность к развитию хронического воспалительного процесса в эндометрии, что, вероятно, имеет генетическую природу и выражается в нарушении представленности TLRs в слизистой оболочке полости матки. Однако для подтверждения этого тезиса требуется углубленные генетические исследования, направленные на выявление мутации генов TLRs.



